
【題目】類比法是常見的研究物質性質的方法之一,可用來預測很多物質的性質,但類比是相對的,必須遵循客觀實際,下列說法中正確的是( )
A. ![]() 通入
通入![]() 溶液中沒有現象,
溶液中沒有現象,![]() 通入
通入![]() 溶液中也無明顯現象
溶液中也無明顯現象
B. ![]() 與
與![]() 會因為水解相互促進而完全反應生成
會因為水解相互促進而完全反應生成![]() 和
和![]() ,
,![]() 與
與![]() 也可以水解相互促進至完全反應生成
也可以水解相互促進至完全反應生成![]() 和
和![]()
C. 偏鋁酸是一元酸,因此,![]() 也是一元酸
也是一元酸
D. ![]() 在標準狀況下為氣體,所以
在標準狀況下為氣體,所以![]() 在標準狀況下同樣為氣體
在標準狀況下同樣為氣體
科目:高中化學 來源: 題型:
【題目】在一定溫度和體積固定的密閉容器中,可逆反應H2(g)+I2(g) ![]() 2HI(g) (無色)達平衡狀態,該狀態下,說法不正確的是( )
2HI(g) (無色)達平衡狀態,該狀態下,說法不正確的是( )
A. 可逆反應停止 B. I2濃度不再變化
C. HI濃度不再變化 D. 混合氣體顏色不再變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2Cu(IO3)2+24KI+12H2SO4=2CuI![]() (碘化亞銅)+13I2+12K2SO4+12H2O,下列說法正確的是 ( )
(碘化亞銅)+13I2+12K2SO4+12H2O,下列說法正確的是 ( )
A.Cu(IO3)2作氧化劑,Cu(IO3)2中只有碘元素被還原
B.CuI既是氧化產物又是還原產物
C.每生成1mol CuI,有11mol KI發生氧化反應
D.每轉移1.1mol電子,有0.2mol IO3-被氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應A(g)+B(g) ![]() C(g)+D(g)過程中的能量變化如圖所示,回答下列問題。
C(g)+D(g)過程中的能量變化如圖所示,回答下列問題。
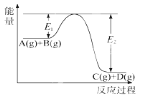
(1)該反應是________反應(填“吸熱”、“放熱”)。
(2)當反應達到平衡時,升高溫度,A的轉化率________(填“增大”、“減小”或“不變”),原因是________。
(3)反應體系中加入催化劑對反應熱是否有影響_______(填“有”、“無”)。
(4)在反應體系中加入催化劑,反應速率增大,此時E1______,E2_______(填“增大”、“減小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】處理含氰![]() 廢水可以用以下兩種方法:
廢水可以用以下兩種方法:
Ⅰ:![]() (未配平),其中A為參與大氣循環的氣體
(未配平),其中A為參與大氣循環的氣體
Ⅱ:①![]() (未配平)
(未配平)
②![]() 下列說法正確的是( )
下列說法正確的是( )
A. ![]() 和
和![]() 的電子式分別為
的電子式分別為![]()
![]()
B. 方法Ⅰ中,每生成![]() ,轉移
,轉移![]() 個電子
個電子
C. 方法Ⅱ中,![]() 是反應②的氧化產物
是反應②的氧化產物
D. 方法Ⅱ的反應①中,![]() 與
與![]() 的物質的量之比為1∶1
的物質的量之比為1∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、R、Q、M是六種原子序數依次增大的短周期主族元素,X是原子半徑最小的元素,Y的氣態氫化物能使濕潤的紅色石蕊試紙變藍,Z的單質是空氣的主要成分之一,R、Q、M三種元素的最高價氧化物對應的水化物相互之間均可反應,M的單質是黃綠色氣體。請回答下列問題:
(1)Z和M的非金屬性強弱Z_________M(填“<”“>”或“=”)。
(2)Z、Q、M簡單離子半徑由大到小的順序為__________________(用離子符號表示)。
(3)X和Z兩元素形成的原子個數比為1∶1的化合物電子式為___________。
(4)Y元素的氣態氫化物與其最高價氧化物對應的水化物反應的化學方程式為______________,所生成的物質水溶液中離子濃度由大到小的順序為_______________。
(5)![]() 是一種高效安全的殺菌消毒劑,它能將電鍍廢水中的
是一種高效安全的殺菌消毒劑,它能將電鍍廢水中的![]() 氧化為兩種無毒的氣體,自身還原成最低價的簡單離子,寫出該反應的離子方程式___________________________。
氧化為兩種無毒的氣體,自身還原成最低價的簡單離子,寫出該反應的離子方程式___________________________。
(6)用電解法可制備![]() ,電解總反應為
,電解總反應為![]() 。已知陽極產物為
。已知陽極產物為![]() ,該物質在水中水解生成
,該物質在水中水解生成![]() 和
和![]() ,則該電極生成
,則該電極生成![]() 的電極反應為________________。
的電極反應為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA為阿伏加德羅常數,下列說法正確的是
A. 28g乙烯所含共用電子對數目為2NA
B. 14g乙烯、丙烯、丁烯的混合氣體中,所含原子數為3NA
C. 標準狀況下,11.2L氟化氫所含分子數為0.5NA
D. 1.5g甲基所含電子數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸(分子式為 H2C2O4,沸點:150℃)是生物體的一種代謝產物,廣泛分布于植物、動 物和真菌體中。下列有關判斷不正確的是
A.草酸的摩爾質量是 90 g/mol
B.草酸中碳元素的質量分數為 13.3%
C.1 mol 草酸中約含有 6.02×1023 個分子
D.1 mol 草酸在標準狀況下的體積約為 22.4 L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B均是由兩種元素組成的化合物,A中某種元素的質量分數為75% ,B是一種淡黃色固體,C、J是同周期元素的氣態氫化物,其中C是含氫量最高的烴,X為無色液體。反應生成的水均已略去。它們有如下圖所示的關系。

(1)寫出化學式:A___________B____________J_____________。
(2)反應③中每生成1molF,轉移電子的數目為:___________。
(3)反應④的化學方程式為:________________________________________________。
(4)離子方程式分別為:反應②__________________________________________;
⑤__________________________________________________________。
(5)反應①中,每1.00gC與足量的F作用,恢復到25℃放出55.6kJ熱量,寫出反應①的熱化學方程式__________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com