
�_�l(f��)ʹ���坍��Դ���l(f��)չ����̼��(j��ng)��(j��)�����ɞ�ƌW(xu��)���о�����Ҫ�n�}����⡢�״��ǃ�(y��u)�|(zh��)���坍ȼ�ϣ�������ȼ��늳ء�
��1������ˮ�����D(zhu��n)������H2����Ҫ�D(zhu��n)������(y��ng)���£�
CH4(g) + H2O(g) CO(g) + 3H2(g) ��H=+206��2 kJ��mol��1
CO(g) + 3H2(g) ��H=+206��2 kJ��mol��1
CH4(g) + 2H2O(g) CO2(g) + 4H2(g) ��H=+165��0 kJ��mol��1
CO2(g) + 4H2(g) ��H=+165��0 kJ��mol��1
��������(y��ng)����ԭ�Ϛ��е�CO��ʹ�ϳɰ��Ĵ����ж�����횳�ȥ�����I(y��)�ϳ����ô���������CO�cˮ���ⷴ��(y��ng)�����׳�ȥ��CO2��ͬ�r(sh��)���Ƶõ��w�e�Ě��ķ������˷���(y��ng)�Q��һ����̼׃�Q����(y��ng)��ԓ����(y��ng)�ğữ�W(xu��)����ʽ�� ��
��2�����a(ch��n)�״���ԭ��CO��H2��Դ�ڣ�CH4(g) + H2O(g)  CO(g) + 3H2(g) ��H>0
CO(g) + 3H2(g) ��H>0
��һ���l����CH4��ƽ���D(zhu��n)�����c�ضȡ�����(qi��ng)���P(gu��n)ϵ��Da���tA��B��C���c(di��n)̎��(du��)��(y��ng)ƽ�ⳣ��(sh��)��KA��KB��KC���Ĵ�С�P(gu��n)ϵ��___________��(�<������>������="��" )��
��100��r(sh��)����1 mol CH4��2 mol H2Oͨ���ݷe��1 L�Ķ����ܷ������У��l(f��)������(y��ng)�����f��ԓ����(y��ng)�ѽ�(j��ng)�_(d��)��ƽ���B(t��i)����__________
a��������(n��i)���w�ܶȺ㶨
b����λ�r(sh��)�g��(n��i)����0��1 mol CH4ͬ�r(sh��)����0��3 mol H2
c�������ĉ���(qi��ng)�㶨
d��3v��(CH4) = v��(H2)
��3��25��r(sh��)����20mL0��1mol/L������м���VmL0��1mol/LNaOH��Һ���y(c��)�û����Һ��pH׃��������D��ʾ�������f�����_����_____��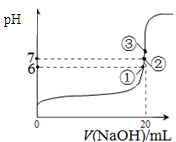
A��pH��3��HF��Һ��pH��11��NaF��Һ�У� ��ˮ��x����c(H+)���
B�����c(di��n)�r(sh��)pH��6���˕r(sh��)��Һ�У�c(F��)��c(Na+)��9��9��10-7mol/L
C�����c(di��n)�r(sh��)����Һ�е�c(F��)��c(Na+)
D�����c(di��n)�r(sh��)V��20mL���˕r(sh��)��Һ��c(Na+)��0��1mol/L
��4���L(zh��ng)���ԁ���һֱ�J(r��n)����ĺ�������ڡ�1971�������ƌW(xu��)���÷���ͨ�^��(x��)��ĩ�r(sh��)�@��HFO����Y(ji��)��(g��u)ʽ��H��O��F��HFO�cˮ����(y��ng)�õ�HF�ͻ�����A��ԓ����(y��ng)�Ļ��W(xu��)����ʽ�� ��
��1�� CO(g) + H2O(g) CO2(g) + H2(g) ��H=��41��2 kJ��mol��1 ��2�֣�
CO2(g) + H2(g) ��H=��41��2 kJ��mol��1 ��2�֣�
��2���� KC = KB >KA ��2�֣�
�� cd ��2�֣�
��3��BC ��2�֣�
��4��H2O��HFO=HF��H2O2 ��2�֣�
����ԇ�}��������1�� �Ȍ�(du��)��֪�ữ�W(xu��)����ʽ��̖(h��o)��٢ڣ��^��l(f��)�F(xi��n)��-�ٿɵã�CO(g) + H2O(g) CO2(g) + H2(g) ��H=��41��2 kJ��mol��1��
CO2(g) + H2(g) ��H=��41��2 kJ��mol��1��
��2���� ƽ�ⳣ��(sh��)ָ���������ȵĻ��W(xu��)Ӌ(j��)����(sh��)��ij˷e���Ը�����(y��ng)���ȵĻ��W(xu��)Ӌ(j��)����(sh��)��ij˷e���õı�ֵ�����W(xu��)ƽ�ⳣ��(sh��)ֻ�c�ض����P(gu��n)������B��C���c(di��n)����ͬ�Ĝضȣ�����KC = KB��Ȼ��A��B���c(di��n)��ȣ���A��B��������D(zhu��n)����׃���f���������Ƅ�(d��ng)�����W(xu��)ƽ�ⳣ��(sh��)׃������KB>KA �����Դ���KC = KB >KA��
�� ԓ�������w�e���ֲ�׃������(j��)�|(zh��)���غ㶨��֪������(y��ng)ǰ���Ϛ��w���|(zh��)����׃������������(n��i)���w���ܶȲ�׃�����Բ��ܱ����_(d��)�����W(xu��)ƽ���B(t��i)����a�e(cu��)�`����λ�r(sh��)�g��(n��i)����0��1 mol CH4ͬ�r(sh��)����0��3 mol H2��������v�������Բ��ܱ����_(d��)�����W(xu��)ƽ���B(t��i)����b�e(cu��)�`���S����(y��ng)�M(j��n)�л�Ϛ��w�����|(zh��)�������������ݷe��׃������(qi��ng)����(d��ng)�����ĉ���(qi��ng)�㶨�r(sh��)���f�����_(d��)ƽ�⣬��c���_��3v��(CH4) = v��(H2)�����|(zh��)����������֮�ȵ��ڻ��W(xu��)Ӌ(j��)����(sh��)֮�ȣ�����(y��ng)���_(d��)ƽ�⣬��d���_�������xcd��
��3��pH��3��HF��Һ����ˮ��x����c(H+)�� ��10-11mol��L��1��pH��11��NaF��Һ�У���ˮ��x����c(H+)��10-14/10-11��10-3mol��L��1��A�e(cu��)�����c(di��n)�r(sh��)������(j��)����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)��c(F��)��c(Na+)��c(H��)��c(OH��)��10-6��
��10-11mol��L��1��pH��11��NaF��Һ�У���ˮ��x����c(H+)��10-14/10-11��10-3mol��L��1��A�e(cu��)�����c(di��n)�r(sh��)������(j��)����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)��c(F��)��c(Na+)��c(H��)��c(OH��)��10-6�� ��9��9��10-7mol/L��B��(du��)������(j��)����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)�����c(di��n)�r(sh��)pH=7����Һ�е�c(H��)��c(OH��)������c(F��)��c(Na+)��C��(du��)�����c(di��n)�r(sh��)V��20mL���˕r(sh��)��Һ��c(Na+)��
��9��9��10-7mol/L��B��(du��)������(j��)����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)�����c(di��n)�r(sh��)pH=7����Һ�е�c(H��)��c(OH��)������c(F��)��c(Na+)��C��(du��)�����c(di��n)�r(sh��)V��20mL���˕r(sh��)��Һ��c(Na+)�� ��0��05mol/L�������xBC��
��0��05mol/L�������xBC��
��4���ؓ(f��)��F��O����H-O-F��FԪ�ر��F(xi��n)-1�r(ji��)���cˮ����(y��ng)����HF���l(f��)��ˮ�ⷴ��(y��ng)������֪A��H-O-O-H��ԓ����(y��ng)�Ļ��W(xu��)����ʽ�飺H2O+HFO=HF+H2O2��
���c(di��n)������ữ�W(xu��)����ʽ�����W(xu��)ƽ��D��Ӱ����ء�ƽ�ⳣ��(sh��)��ƽ���B(t��i)�Дࡢ��늽��|(zh��)����x���x�ӝ�ȱ��^�ȡ�


 �Ͻ�ƽС�W(xu��)�L��(d��ng)�y(c��)ԇϵ�д�
�Ͻ�ƽС�W(xu��)�L��(d��ng)�y(c��)ԇϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
X��Y��Z��W����10��ӵķ��ӻ��x�ӡ�X��5��(g��)ԭ�Ӻˡ�ͨ����r�£�W��oɫҺ�w������֮�g�D(zhu��n)���P(gu��n)ϵ��D��ʾ��Ո(q��ng)�ش�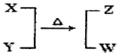
��1�����I(y��)��ÿ��ȡ1molZҪ�ų�46.2 kJ�ğ���������ԓ����(y��ng)�ğữ�W(xu��)����ʽ�� ��
��2�����I(y��)��ȡZ�Ļ��W(xu��)ƽ�ⳣ��(sh��)K�cT���P(gu��n)ϵ���±���
| T/K | 298 | 398 | 498 | ���� |
| K/(mol��L��1)��2 | 4.1��106 | K1 | K2 | ���� |

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
����̼ѭ�h(hu��n)����������ĸ߶���ҕ������ν��ʹ����CO2�ĺ�������Ч���_�l(f��)����CO2��������ȫ������ձ���ҕ�����ԡ���̼��(j��ng)��(j��)�����ɞ�ƌW(xu��)���о�����Ҫ�n�}��
��1������CO2�cH2����(y��ng)����CH4��H2O�ğữ�W(xu��)����ʽ ��
��֪�� �� CO(g)+H2O(g) H2(g)+CO2(g) ��H����41kJ��mol��1
H2(g)+CO2(g) ��H����41kJ��mol��1
�� C(s)+2H2(g) CH4(g) ��H����73kJ��mol��1
CH4(g) ��H����73kJ��mol��1
�� 2CO(g) C(s)+CO2(g) ��H����171kJ��mol��1
C(s)+CO2(g) ��H����171kJ��mol��1
��2����ȼú�U���е�CO2�D(zhu��n)��������ѵķ���(y��ng)ԭ��飺2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)����֪һ���l���£�ԓ����(y��ng)��CO2��ƽ���D(zhu��n)�����S�ضȡ�Ͷ�ϱ�[n(H2) / n(CO2)]��׃������������D��
CH3OCH3(g) + 3H2O(g)����֪һ���l���£�ԓ����(y��ng)��CO2��ƽ���D(zhu��n)�����S�ضȡ�Ͷ�ϱ�[n(H2) / n(CO2)]��׃������������D��
���������l����׃�r(sh��)��Ո(q��ng)?ji��n)��ψD�Ю���ƽ��r(sh��)CH3OCH3���w�e��?j��n)?sh��)�SͶ�ϱ�[n(H2) / n(CO2)]׃���������D��
��ij�ض��£���2.0molCO2(g)��6.0molH2(g)�����ݷe��2L�����]�����У�����(y��ng)���_(d��)ƽ��r(sh��)����׃����(qi��ng)�͜ضȣ�ƽ���wϵ��CH3OCH3(g)�����|(zh��)������?j��n)?sh��)׃����r��D��ʾ���P(gu��n)�ڜضȺ͉���(qi��ng)���P(gu��n)ϵ�Д����_���� ��
A. P3��P2��T3��T2 B. P1��P3��T1��T3 C. P2��P4��T4��T2 D. P1��P4��T2��T3
���ں������]�����ﰴ�w�e�Ȟ�1:3���������̼�͚� �⣬һ���l���·���(y��ng)�_(d��)��ƽ���B(t��i)����(d��ng)��׃����(y��ng)��ijһ��(g��)�l��������׃�����f��ƽ��һ�����淴��(y��ng)�����Ƅ�(d��ng)���� ��
A. ������(y��ng)�����������pС
B. �淴��(y��ng)�����������pС
C. ���W(xu��)ƽ�ⳣ��(sh��)Kֵ����
D. ����(y��ng)����w�e�ٷֺ�������
E. ��Ϛ��w���ܶȜpС
F. �����D(zhu��n)���ʜpС
��3������ƌW(xu��)���ٴ�������Gɫ���W(xu��)����(g��u)�룺�ѿ՚ⴵ��̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ��������(j��ng)���W(xu��)����(y��ng)��ʹ�՚��е�CO2�D(zhu��n)׃?y��u)������ȼ�ϼ״����״�������ȼ��늳أ�������ϡ�����늽��|(zh��)�״�ȼ��늳�ؓ(f��)�O����(y��ng)ʽ__ ���Դ�ȼ��늳���������Դ���D��ʾ늽������~��Һ�������ʼ�r(sh��)ʢ��1000mL pH��5�������~��Һ��25�棬CuSO4��������һ�Εr(sh��)�g����Һ��pH׃?y��u)?���˕r(sh��)���^�쵽�ĬF(xi��n)���� ����Ҫʹ��Һ�֏�(f��)����ʼ��ȣ��ضȲ�׃��������Һ�w�e��׃������������Һ�м��� �������|(zh��)���Q�������|(zh��)���s�� g��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
����(j��)���W(xu��)�W(xu��)���еĻ�����Փ��Ո(q��ng)�ش����І��}��
�����£�ȡpH��2���}��ʹ�����Һ��100 ml, �����зքe�����m����Zn��������(y��ng)�^���Ѓ���Һ��pH׃����D��ʾ���t�D�б�ʾ������Һ��pH׃����������_____ (�A����B��)��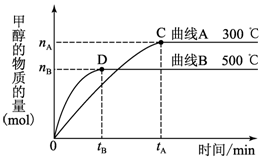
������ȼ���r(sh��)�ܷų������ğᣬ��Ҳ��Һ��ʯ�͚����Ҫ�ɷ֣�������Դ��(y��ng)�����˂����ճ����a(ch��n)�����
��֪����2C3H8��g��+7O2��g����6CO��g��+8H2O��l������H1����2741.8kJ/mol
��2CO��g��+O2��g����2CO2��g�� ��H2����566kJ/mol
��1�����������ȼ����ğữ�W(xu��)����ʽ�� ��
��2���F(xi��n)��1mol C3H8�ڲ�������������ȼ��������1mol CO��2mol CO2�Լ���B(t��i)ˮ�������еĮa(ch��n)��ͨ��һ��(g��)�̶��w�e��1L�����]�����У���һ���l���°l(f��)�����¿��淴��(y��ng)��
CO��g��+H2O��g����CO2��g��+ H2��g�� ��H1��+41.2kJ/mol
��������(sh��)���f��ԓ����(y��ng)�_(d��)��ƽ�����
a���wϵ�еĉ���(qi��ng)���l(f��)��׃�� b��v��(H2)��v��(CO)
c����Ϛ��w��ƽ������(du��)�����|(zh��)�����l(f��)��׃�� d��CO2�ĝ�Ȳ��ٷ���׃��
��5min���wϵ�_(d��)��ƽ�⣬��(j��ng)�y(c��)����H2��0.8mol���tv(H2)= ��
����ƽ���wϵ�г�������CO���tƽ�ⳣ��(sh��) ����������pС����׃������
��3������(j��)��1���еķ���(y��ng)�����O(sh��)Ӌ(j��)һ�N����ȼ��늳أ�һ�Oͨ��՚⣬��һ�Oͨ�������w��ȼ��늳�(n��i)�������ڵē��s������ᐣ�Y2O3��������䆣�ZrO2�����w�������(n��i)�����Ԃ���(d��o)O2-����늳�(n��i)��O2-���� �O���������ؓ(f��)������늳ص����O늘O����(y��ng)�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
(1)��֪��
��Fe(s)��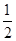 O2(g)=FeO(s)����H����272.0 kJ��mol��1
O2(g)=FeO(s)����H����272.0 kJ��mol��1
��2Al(s)�� O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
Al��FeO�l(f��)���X�ᷴ��(y��ng)�ğữ�W(xu��)����ʽ��____________________________________
(2)ij���淴��(y��ng)�ڲ�ͬ�l���µķ���(y��ng)�v�̷քe��A��B(���ψD��ʾ)��
�ٸ���(j��)�D�Д�ԓ����(y��ng)�_(d��)��ƽ��������l����׃�����ߜضȣ�����(y��ng)����D(zhu��n)����________(������pС����׃��)��
������B�v�̱����˷���(y��ng)���õėl����________(�x����̖(h��o))��
A�����ߜضȡ������� B������(y��ng)��ĝ�� C�����͜ض� D��ʹ�ô���
(3)1000 ��r(sh��)�������c�c���l(f��)�������(y��ng)��Na2SO4(s)��4H2(g) Na2S(s)��4H2O(g)
Na2S(s)��4H2O(g)
ԓ����(y��ng)��ƽ�ⳣ��(sh��)���_(d��)ʽ��________________________________��
��֪K1000 ��<K1200 �����������wϵ�ضȣ���Ϛ��w��ƽ������(du��)�����|(zh��)������(hu��)________(������pС����׃��)��
(4)�����£����ȡ0.1 mol��L��1 HA��Һ�c0.1 mol��L��1 NaOH��Һ���w�e���(��Ϻ���Һ�w�e��׃�����Բ�Ӌ(j��))���y(c��)�û��Һ��pH��8��
�ٻ��Һ����ˮ��x����OH������c0.1 mol��L��1 NaOH��Һ����ˮ��x����OH�����֮�Ȟ�________��
����֪NH4A��Һ�����ԣ���֪��HA��Һ�ӵ�Na2CO3��Һ���К��w�ų���ԇ�Ɣ�(NH4)2CO3��Һ��pH________7(�<����>������)����ͬ�ض��£������|(zh��)������ȵ������ķN�}��Һ��pH�ɴ�С���������?y��n)?����̖(h��o))________��
a��NH4HCO3 b��NH4A c��(NH4)2CO3 d��NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
ú��������ú��ԭ��,��(j��ng)�^���W(xu��)�ӹ�ʹú�D(zhu��n)������w��Һ�w�����wȼ���Լ����N�����a(ch��n)Ʒ�Ĺ��I(y��)�^�̡�
(1)��֪��25 �桢101 kPa�r(sh��),C(s)��H2(g)��CO(g)ȼ���ğữ�W(xu��)����ʽ�քe��:
C(s)+O2(g) CO2(g)����H1="-393.5" kJ/mol;
CO2(g)����H1="-393.5" kJ/mol;
H2(g)+ O2(g)
O2(g) H2O(g)����H2="-241.8" kJ/mol;
H2O(g)����H2="-241.8" kJ/mol;
CO(g)+ O2(g)
O2(g) CO2(g)����H3="-283.0" kJ/mol;
CO2(g)����H3="-283.0" kJ/mol;
�لtC(s)+H2O(g) CO(g)+H2(g)����H=��������,ԓ����(y��ng)ƽ�ⳣ��(sh��)�ı��_(d��)ʽ��K=��������������������;���ߜض�,�tKֵ��������(�׃����׃С����׃��)��
CO(g)+H2(g)����H=��������,ԓ����(y��ng)ƽ�ⳣ��(sh��)�ı��_(d��)ʽ��K=��������������������;���ߜض�,�tKֵ��������(�׃����׃С����׃��)��
������ٷ���(y��ng)���ݷe��׃�����]�������M(j��n)��,��(d��ng)����(y��ng)�_(d��)��ƽ��r(sh��)��������(�̖(h��o))��
a.v��(CO)��v��(H2)=1��1
b.̼���|(zh��)�����ֲ�׃
c.v��(CO)=v��(H2O)
d.�����еĉ���(qi��ng)��׃
�����ݷe��׃�����]�������M(j��n)�Тٷ���(y��ng),����ʹc(CO)�����������������
a.���ߜض�
b.����He(g),ʹ�wϵ����(qi��ng)����
c.��H2(g)���wϵ�з��x����
d.�������
(2)����ͬ����CO(g)��H2O(g)�քeͨ���w�e��2 L�ĺ������]������,�M(j��n)�з���(y��ng)CO(g)+H2O(g) CO2(g)+H2(g),�õ�����2�M��(sh��)��(j��):
CO2(g)+H2(g),�õ�����2�M��(sh��)��(j��):
| ��(sh��)�(y��n)�M | �ض�/�� | ��ʼ��/mol | ƽ����/mol | �_(d��)��ƽ���� ��r(sh��)�g/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�µġ��h(hu��n)���՚��|(zh��)����(bi��o)��(zh��n)������2016��1��1�����҇�ȫ�挍(sh��)ʩ����(j��)�ˣ��h(hu��n)���՚��|(zh��)��ָ��(sh��)(AQI)��?q��ng)?b��o)�͌�(sh��)�r(sh��)��(b��o)�������SO2��NO2��CO��O3��PM10��PM2.5��ָ��(bi��o)���鹫���ṩ����ָ��������(d��o)��(d��ng)?sh��)ؾ���������ų��к�����?br />(1)��܇�ų���β���к���CO��NO�Ț��w���û��W(xu��)����ʽ��ጮa(ch��n)��NO��ԭ��________________________________________
(2)��܇�Ś�܃�(n��i)���b�Ĵ��D(zhu��n)��������ʹ��܇β���е���Ҫ��Ⱦ���D(zhu��n)����o���Ĵ��ѭ�h(hu��n)���|(zh��)����֪��
N2(g)��O2(g)===2NO(g)����H����180.5 kJ��mol��1
2C(s)��O2(g)===2CO(g)����H����221.0 kJ��mol��1
C(s)��O2(g)===CO2(g)����H����393.5 kJ��mol��1
�t����(y��ng)2NO(g)��2CO(g)??N2(g)��2CO2(g)�Ħ�H��________kJ��mol��1��ԓ����(y��ng)�Ħ�S________0(�>����<������)��
(3)��0.20 mol NO��0.10 mol CO����һ��(g��)�ݷe�㶨��1 L�����]�����У��ڲ�ͬ�l���·���(y��ng)�^���в������|(zh��)�ĝ��׃����r��D��ʾ��
��Ӌ(j��)��a(ch��n)��N2��6��9 min�r(sh��)��ƽ������(y��ng)����v(N2)��________mol��L��1��min��1��
�ڵ�12 min�r(sh��)��׃�ķ���(y��ng)�l����________(����ء����ء�)��
��Ӌ(j��)�㷴��(y��ng)�ڵ�24 min�r(sh��)��ƽ�ⳣ��(sh��)K��________�������֜ضȲ�׃�����������г���CO��N2��0.060 mol��ƽ�⌢________�Ƅ�(d��ng)(�����������)��
(4)�h(hu��n)���O(ji��n)�y(c��)��߀���ó������y(c��)���՚��к����^�ߝ��SO2�ĺ�������(j��ng)���һЩ���|(zh��)��20 ��Ĕ�(sh��)��(j��)���±���
| �ܽ��(S)/g | �ܶȷe(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaSO3 | BaSO3 |
| 0.160 | 3.89 | 6.76��10��3 | 5.48��10��9 |
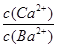 ��____________(�������_(d��)ʽ����)��
��____________(�������_(d��)ʽ����)���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�Ȼ��F��һ�N��Ҫ�Ļ���ԭ�ϣ��oˮ�Ȼ��F������՚�O����ˮ����FeCl3��nH2O��
��1����(sh��)�(y��n)���������b�ã����ּӟᡢ�A�ֵ��b������ȥ���Ƃ�oˮ�Ȼ��F���w��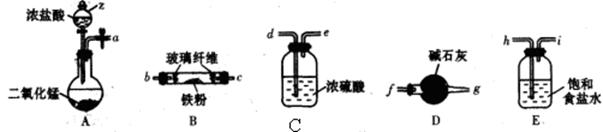
���b��A�Ѓx��z�����Q��___________��
�ں�(ji��n)���z�(y��n)�b��A�����ԵIJ�����______________________��
�۰����������B�Ӹ��x���ӿڣ����?y��n)�a��_________ ��__________ ��_________ ��__________��b��c��_________��__________���b��D��������______________________��
��2�����I(y��)���Ƃ�oˮ�Ȼ��F��һ�N��ˇ�������£�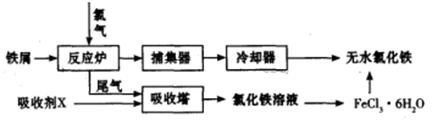
���������аl(f��)������(y��ng)���x�ӷ���ʽ��_________________________________________��
�ں�(ji��n)����FeCl3��6H2O���w�õ��oˮ�Ȼ��F�IJ�����________________________________��
���õ������y(c��)�����ßoˮ�Ȼ��F���|(zh��)����?j��n)?sh��)���Qȡm�˟oˮ�Ȼ��F��Ʒ������ϡ�}�ᣬ���D(zhu��n)�Ƶ�100 mL����ƿ�У������sˮ���ݣ�ȡ��10 mL���������^����KI��Һ����ַ���(y��ng)����ָʾ��_________����ԇ�����Q������c mol/L��Na2S2O3��Һ�M(j��n)�еζ����K�c(di��n)�r(sh��)����V mLNa2S2O3��Һ����֪��I2��2S2O32����2I����S4O62�������t��Ʒ���Ȼ��F���|(zh��)����?j��n)?sh��)��____________��
��3������֪��
Fe(OH)3(aq) Fe3��(aq)��3OH��(aq) ��H��a kJ/mol
Fe3��(aq)��3OH��(aq) ��H��a kJ/mol
H2O(l) H��(aq)��OH��(aq) ��H��b kJ/mol
H��(aq)��OH��(aq) ��H��b kJ/mol
Ո(q��ng)����Fe3���l(f��)��ˮ�ⷴ��(y��ng)�ğữ�W(xu��)����ʽ________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�҇��ǂ�(g��)��F���,��F�a(ch��n)���������һ,�ߠt���F������ձ�ğ��F������
I.��֪����(y��ng) 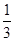 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
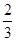 Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1��ԓ����(y��ng)��
Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1��ԓ����(y��ng)��
1000���ƽ�ⳣ��(sh��)����4����һ��(g��)�ݷe��10L�����]������,1000��r(sh��)����Fe��Fe2O3��CO��CO2��1. 0mol,����(y��ng)��(j��ng)�^l0min���_(d��)��ƽ�⡣
��1��CO��ƽ���D(zhu��n)����=____________
��2�������CO��ƽ���D(zhu��n)����,���M(j��n)Fe2O3���D(zhu��n)��,�ɲ�ȡ�Ĵ�ʩ��________
a����߷���(y��ng)�ض�
b������(y��ng)�wϵ�ĉ���(qi��ng)
c���xȡ���m�Ĵ���
d�����r(sh��)���ջ��Ƴ�����CO2
e������Vʯ,ʹ���cƽ���Ϛ��w��ֽ��|
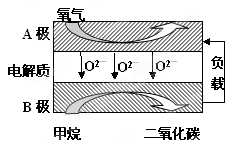
��.�ߠt���F�a(ch��n)���ďU���е�CO���M(j��n)�л���,ʹ����һ���l���º�H2����(y��ng)�Ƃ�״�:
CO(g)+ 2H2(g) CH3OH(g)��Ո(q��ng)����(j��)�Dʾ�ش����І��}:
CH3OH(g)��Ո(q��ng)����(j��)�Dʾ�ش����І��}: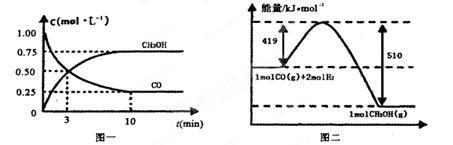
��1���ķ���(y��ng)�_ʼ��ƽ��,��H2���׃����ʾƽ������(y��ng)����v(H2)=________
��2�����ڜضȺ�������ͬ������(g��)���]������,����ͬ��ʽͶ�뷴��(y��ng)��,�y(c��)�÷���(y��ng)�_(d��)��ƽ�ⅼ�����P(gu��n)��(sh��)��(j��)���±���
| ���� | ����(y��ng)��Ͷ����� | ����(y��ng)��� �D(zhu��n)���� | CH3OH�ĝ�� | ����׃�� (Q1��Q2��Q3������0) |
| �� | 1mol CO��2mol H2 | ��1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | ��2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | ��3 | c3 | �ų�Q3kJ���� |
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com