
Ė▀┬╚╦ßĪó┴“╦ßĪóŽ§╦ß║═¹}╦ßČ╝╩ŪÅŖ╦ß,Ųõ╦ßąįį┌╦«╚▄ę║ųą▓Ņäe▓╗┤¾ĪŻęįŽ┬╩Ū─│£žČ╚Ž┬▀@╦─ĘN╦ßį┌▒∙┤ū╦ßųąĄ─ļŖļx│ŻöĄ:
| ╦ß | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6Ī┴10-5 | 6.3Ī┴10-9 | 1.6Ī┴10-9 | 4.2Ī┴10-10 |
 2H++S
2H++S ╠ņ╠ņŽ“╔Žę╗▒Š║├ŠĒŽĄ┴ą┤░Ė
╠ņ╠ņŽ“╔Žę╗▒Š║├ŠĒŽĄ┴ą┤░Ė ąĪīW╔·10ĘųńŖæ¬ė├Ņ}ŽĄ┴ą┤░Ė
ąĪīW╔·10ĘųńŖæ¬ė├Ņ}ŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ĻPė┌╩ę£žŽ┬Ž┬┴ą╚▄ę║Ą─šfĘ©▓╗š²┤_Ą─╩Ū
| AŻ«╦«Ą─ļŖļx│╠Č╚Ż║ó┘=ó┌=ó█=ó▄ |
| BŻ«Ęųäe╝ė╦«ŽĪßī10▒ČŻ¼╚▄ę║Ą─pHŻ║ó┘>ó┌>ó█>ó▄ |
CŻ«ó┘Īóó█ā╔╚▄ę║Ą╚¾wĘe╗ņ║ŽŻ║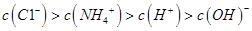 |
DŻ«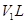 ╚▄ę║ó┌┼c ╚▄ę║ó┌┼c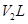 ╚▄ę║ó█╗ņ║ŽŻ¼╚¶ ╚▄ę║ó█╗ņ║ŽŻ¼╚¶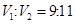 Ż¼ät╗ņ║Ž╚▄ę║pH=4(║÷┬į╚▄ę║¾wĘeūā╗») Ż¼ät╗ņ║Ž╚▄ę║pH=4(║÷┬į╚▄ę║¾wĘeūā╗») |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąöó╩÷š²┤_Ą─╩Ū( )
| AŻ«pH=3Ą─┤ū╦ß╚▄ę║┼cpH=11Ą─Üõč§╗»Ōc╚▄ę║Ą╚¾wĘe╗ņ║Ž║¾pH=7 |
| BŻ«╬’┘|Ą─┴┐ØŌČ╚ŽÓĄ╚Ą─CH3COOH║═CH3COONa╚▄ę║Ą╚¾wĘe╗ņ║ŽŻ║c(CH3COOŻŁ)+c(CH3COOH)=2c(Na+) |
| CŻ«│Ż£žŽ┬Ż¼Ž“NH4Cl╚▄ę║ųą╝ė╚ļ░▒╦«ų┴╚▄ę║Ą─pH=7Ż¼┤╦Ģr╚▄ę║ųącŻ©NH4+Ż®ŻŠcŻ©C1ŻŁŻ® |
| DŻ«0.1molĪżLŻŁ1NaHCO3╚▄ę║Ż║c(NaŻ½)ŻŠc(HCO3ŻŁ)ŻŠc(OHŻŁ)ŻŠc(HŻ½) |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ŽÓ═¼╬’┘|Ą─┴┐ØŌČ╚Ą─NaCN║═NaClOŽÓ▒╚,NaCN╚▄ę║Ą─pH▌^┤¾,ätŽ┬┴ąĻPė┌═¼£žĪó═¼¾wĘeĪó═¼ØŌČ╚Ą─HCN║═HClO╚▄ę║Ą─šfĘ©ųąš²┤_Ą─╩Ū(ĪĪĪĪ)
| AŻ«╦ߥ─ÅŖ╚§:HCN>HClO |
| BŻ«pH:HClO>HCN |
| CŻ«┼cNaOHŪĪ║├═Ļ╚½Ę┤æ¬Ģr,Ž¹║─NaOHĄ─╬’┘|Ą─┴┐:HClO>HCN |
| DŻ«╦ßĖ∙ļxūėØŌČ╚:c(CN-)<c(ClO-) |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
H2SO3╩ŪČ■į¬╚§╦߯¼NaHSO3╚▄ę║│╩╦ßąįĪŻį┌0.1 molĪżLŻŁ1 NaHSO3╚▄ę║ųąŻ¼Ž┬┴ąĻPŽĄš²┤_Ą─╩ŪŻ© Ż®
| AŻ«c(HSO3-)ŻŠc(SO32-)ŻŠc(H2SO3) |
| BŻ«c(NaŻ½)ŻĮc(HSO3-)Ż½2c(SO32-)Ż½c(H2SO3) |
| CŻ«c(NaŻ½)ŻĮc(HSO3-)ŻŠc(HŻ½)ŻŠc(OHŻŁ) |
| DŻ«c(NaŻ½)Ż½c(HŻ½)ŻĮc(HSO3-)Ż½c(OHŻŁ)Ż½c(SO32-) |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ęčų¬25 ĪµĢrKW=10-14,╚ń╣¹100 ĪµĢrKW=5.5Ī┴10-13,▀@šf├„(ĪĪĪĪ)
| AŻ«100 ĪµĢr╦«Ą─ļŖļx│╠Č╚▌^ąĪ |
| BŻ«Ū░š▀c(H+)▌^║¾š▀┤¾ |
| CŻ«╦«Ą─ļŖļx▀^│╠╩Ūę╗éĆ╬³¤ß▀^│╠ |
| DŻ«100 ĪµĢr0.1 molĪżL-1 DClĄ─ųž╦«╚▄ę║ųą╦«Ą─ļŖļx│╠Č╚ę╗Č©╩Ū╩ę£žĢrļŖļx│╠Č╚Ą─10▒Č |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąĻPė┌ļŖļx│ŻöĄĄ─šfĘ©š²┤_Ą─╩Ū(ĪĪĪĪ)
| AŻ«ļŖļx│ŻöĄļSų°╚§ļŖĮŌ┘|Ą─ØŌČ╚į÷┤¾Č°į÷┤¾ |
| BŻ«CH3COOHĄ─ļŖļx│ŻöĄ▒Ē▀_╩Į×ķKa= |
| CŻ«CH3COOH╚▄ę║ųą╝ė╚ļ╔┘┴┐CH3COONa╚▄ę║,ļŖļx│ŻöĄ£pąĪ |
| DŻ«ļŖļx│ŻöĄų╗┼c£žČ╚ėąĻP,┼cØŌČ╚¤oĻP |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ą╚▄ę║ųą╬ó┴ŻØŌČ╚ĻPŽĄę╗Č©š²┤_Ą─╩Ū(ĪĪĪĪ)
| AŻ«░▒╦«┼c┬╚╗»õ@Ą─pHŻĮ7Ą─╗ņ║Ž╚▄ę║ųąŻ║c(ClŻŁ)ŻŠc(NH4+) |
| BŻ«ą┬ųŲ┬╚╦«ųąŻ║c(ClŻŁ)ŻŠc(HŻ½)ŻŠc(OHŻŁ)ŻŠc(ClOŻŁ) |
| CŻ«╩ę£žŽ┬Ż¼Ž“0.01 molĪżLŻŁ1 NH4HSO4╚▄ę║ųąĄ╬╝ėĄ╚ØŌČ╚Ą╚¾wĘeĄ─NaOH╚▄ę║Ż║c(NaŻ½)=c(SO42-)ŻŠc(NH4+)ŻŠc(HŻ½)ŻŠc(OHŻŁ) |
| DŻ«pHŻĮ2Ą─ę╗į¬╦ß║═pHŻĮ12Ą─ę╗į¬ÅŖēAĄ╚¾wĘe╗ņ║ŽŻ║c(OHŻŁ)ŻĮc(HŻ½) |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ī”ė┌│Ż£žŽ┬pHŠ∙×ķ4Ą─╚²ĘN╚▄ę║Ż║ó┘¹}╦߯¼ó┌CH3COOH╚▄ę║Ż¼ó█NH4Cl╚▄ę║Ż¼Ž┬┴ąšfĘ©ųąš²┤_Ą─╩Ū(ĪĪĪĪ)
| AŻ«╚▄ę║ųąė╔╦«ļŖļx│÷Ą─c(HŻ½)Ż║ó┌>ó█ |
| BŻ«ŽĪßī100▒Č║¾╚▄ę║Ą─pHŻ║ó┘<ó█ |
| CŻ«ųą║═ŽÓ═¼¾wĘeĄ─╔Ž╩÷╚▄ę║Ž¹║─NaOH╚▄ę║Ą─¾wĘeŻ║ó┘<ó┌ |
| DŻ«ó┌║═ó█Ą╚¾wĘe╗ņ║Ž║¾Ą─╚▄ę║Ż║c(CH3COOŻŁ)Ż½c(ClŻŁ)ŻĮc(NH) |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com