
某化學興趣小組為探究SO2的性質,按下圖所示裝置進行實驗。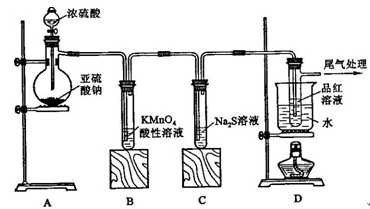
請到答F列問題:
(1)裝置A中盛放亞硫酸鈉的儀器名稱是 ,其中發生反應的化學方程式為 ;
(2)實驗過程中,裝置B、C中發生的現象分別是 、 ,這些現象分別說明SO2具有的性質是 和 ;裝置B中發生反應的離子方程式為 ;
(3)裝置D的目的是探究SO2與品紅作用的可逆性,請寫出實驗操作及現象 ;
(4)尾氣可采用 溶液吸收。
(1)蒸餾燒瓶 Na2SO3+H2SO4(濃)= Na2SO4+ H2O+SO 2↑
(2)溶液由紫紅色變為無色 無色溶液中出現黃色渾濁
還原性 氧化性 5SO2 + MnO4- + 2H2O = 2Mn2+ + 5SO42- + 4H+
(3)品紅溶液褪色后,關閉分液漏斗的旋塞,點燃酒精燈加熱,溶液恢復為紅色
(4)NaOH
解析試題分析:該實驗為制備SO2并檢驗其性質,則A為SO2的發生裝置,B、C、D為檢驗裝置;B中為酸性高錳酸鉀溶液。它具有強氧化性能把SO2氧化成H2SO4,它本身被還原為Mn2+,溶液的紫色變淺或褪去。故可用于檢驗SO2的還原性;C中為硫化鈉溶液,其具有強還原性二者發生反應產生難溶于水的S單質,看見溶液變渾濁,故可用于檢驗SO2的氧化性;D中為品紅溶液,可檢驗SO2的漂白性;SO2的漂白是結合漂白,產生的無色物質不穩定,受熱容易分解而恢復原來的紅色。SO2是大氣污染物,它是酸性氧化物,可用堿性溶液NaOH來消除其危害。
考點:考查SO2的實驗室制法及性質的檢驗。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:填空題
硫酸和硝酸是中學階段常見的兩種強酸,請就兩者與金屬銅的反應情況回答下列問題:
(1)在100 mL 18 mol·L-1的濃硫酸中加入過量的銅片,加熱使之充分反應,產生的氣體在標準狀況下的體積可能是 (填寫代號);
| A.7.32 L | B.6.72 L | C.20.16 L | D.30.24 L |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硅在地殼中的含量較高,硅及其化合物的開發由來已久,在現代生活中有廣泛應用。回答下列問題:
(1)陶瓷、水泥和玻璃是常用的傳統的無機非金屬材料,其中生產普通玻璃的主要原料有 。
(2)高純硅是現代信息、半導體和光伏發電等產業都需要的基礎材料。工業上提純硅有多種路線,其中一種工藝流程示意圖及主要反應如下: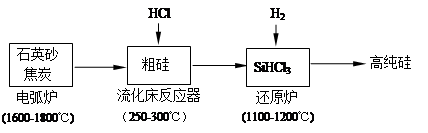
①工業上用石英砂和焦炭在電弧爐中高溫加熱到1600℃-1800℃除生成粗硅外,也可以生產碳化硅,則在電弧爐內可能發生的反應的化學方程式為 。
②在流化床反應的產物中,SiHCl3大約占85%,還有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化學反應方程式 。
(3)有關物質的沸點數據如下表,提純SiHCl3的主要工藝操作依次是沉降、冷凝和 ;SiHCl3極易水解,其完全水解的產物為 。
| 物質 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸點/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅。三氯甲硅烷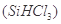 還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
還原法是當前制備高純硅的主要方法,生產過程示意圖如下: 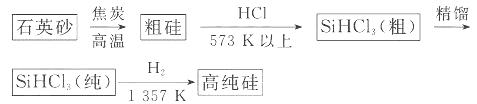
①寫出由純 制備高純硅的化學方程式: ____________________________________。
制備高純硅的化學方程式: ____________________________________。
②整個制備過程必須嚴格控制無水無氧。 遇水劇烈反應生成
遇水劇烈反應生成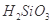 、HCl和另一種物質,配平后的化學反應方程式為___________________________;
、HCl和另一種物質,配平后的化學反應方程式為___________________________;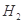 還原
還原 過程中若混入
過程中若混入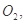 可能引起的后果是____________________________________。
可能引起的后果是____________________________________。
(2)下列有關硅材料的說法正確的是_________ (填字母)。
| A.碳化硅化學性質穩定,可用于生產耐高溫水泥 |
| B.氮化硅硬度大、熔點高,可用于制作高溫陶瓷和軸承 |
| C.高純度的二氧化硅可用于制造高性能通訊材料——光導纖維 |
| D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
濃硫酸在實驗室可用來干燥Cl2、HCl等氣體,這是利用了濃硫酸的__________性。 蔗糖遇濃硫酸變黑,是由于濃硫酸具有__________性。若將盛有濃硫酸的容器敞口放在空氣中一段時間后, 其質量會__________(填“增加”、“減少”或“沒有變化”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖表示在沒有通風櫥的條件下制備氯氣時設計的裝置,圖中a、b是可控制的彈簧鐵夾。(氯氣在飽和氯化鈉溶液中的溶解度較小。)
(1)儀器A的名稱是 ;水槽中應盛放的是 ;燒杯中盛放的是 ;燒瓶中反應的化學方程式 ;
在收集氯氣時,應打開 關閉 (填a, b)當氯氣收集完畢,尾氣處理時燒杯中發生反應的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如圖是現今常規生產發煙硫酸和硫酸的流程圖: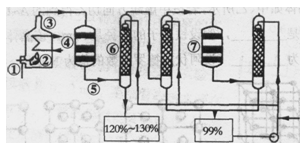
(1)在④處二氧化硫被氧化成三氧化硫,④的設備名稱是 .該處發生反應的方程式為 .為提高三氧化硫的產率,該處應采用 (填“等溫過程”或“絕熱過程”)為宜.
(2)在⑦處進行二次催化處理的原因是 .
(3)⑤處氣體混合物主要是氮氣和三氧化硫.此時氣體經過⑥后不立即進入⑦是因為: .
(4)20%的發煙硫酸(SO3的質量分數為20%)1噸需加水 噸(保留2位有效數字)才能配制成98%的成品硫酸.
(5)在②處發生1500℃的“不完全燃燒”,即先混入少量干燥空氣,然后在③處于700℃下再繼續燃燒.試簡述這種燃燒方式對環境保護是有利的原因 .
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
金剛石SiC具有優良的耐磨、耐腐蝕特性,應用廣泛.
(1)碳與同周期元素Q的單質化合僅能生成兩種常見氣態化合物,其中一種化合物H為非極性分子,碳元素在周期表中的位置是,Q是,R的電子式為.
(2)一定條件下,Na還原CCl4可制備金剛石,反應結束冷卻至室溫后,回收CCl4的實驗操作名稱為,除去粗產品中少量鈉的試劑為.
(3)碳還原制SiC,其粗產品中雜質為Si和SiO2.先將20.0g 粗產品加入到過量的NaOH溶液中充分反應,收集到0.1mol氫氣,過濾得SiC固體11.4g,濾液稀釋到1L,生成氫氣的離子方程式為,硅酸鈉的物質的量濃度為
粗產品加入到過量的NaOH溶液中充分反應,收集到0.1mol氫氣,過濾得SiC固體11.4g,濾液稀釋到1L,生成氫氣的離子方程式為,硅酸鈉的物質的量濃度為
(4)下列敘述正確的有(填序號),ks5u
①Na還原CCl4的反應、Cl2與H2O的反應均是置換反應②水晶、干冰熔化時克服粒子間作用力的類型相同③Na2SiO3溶液與SO3的反應可用于推斷Si與S的非金屬性強弱
④鈉、鋰分別在空氣中燃燒,生成的氧化物中陰陽離子數目比均為1:2
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
化學肥料在農業生產中有重要作用。農業生產中,大量施用的化肥主要是氮肥、磷肥、鉀肥。
(1)普鈣是磷肥,它的有效成分是__________________(寫化學式)。
(2)尿素是一種含氮量較高的氮肥,工業生產尿素是將氨氣與二氧化碳在加壓、加熱的條件下反應生成氨基甲酸銨(H2NCOONH4),再使氨基甲酸銨脫水得到尿素。反應的化學方程式為_________、___________。
(3)某化肥廠用NH3制備NH4NO3,已知由NH3制NO的產率是96%、NO制HNO3的產率是92%,則制HNO3所用去NH3的質量占耗用全部NH3質量的__________%。
(4)合成氨氣是生產氮肥的重要環節。合成氨生產簡易流程示意圖如下: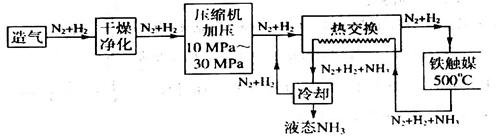
從示意圖可知其存在循環操作。簡要說明為什么在化工生產中經常采用循環操作___________。合成氨的反應需在500℃進行,其主要原因是_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com