
 2Cl2+2H2O
2Cl2+2H2O

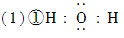
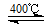 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)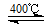 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)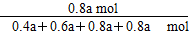 ×100%≈30.8%。
×100%≈30.8%。

科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中的化學鍵斷裂時需要吸收的能量/kJ | 436 | a | 369 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.該反應中舊鍵斷裂需吸收能量,新鍵形成需放出能量,所以總能量不變 |
| B.上述熱化學方程式中的ΔH的值與反應物的用量無關 |
| C.該反應的化學能可以轉化為電能 |
| D.反應物的總能量高于生成物的總能量 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
A.C(s)+ O2(g)=CO(g)ΔH=-393.5 kJ·mol-1 O2(g)=CO(g)ΔH=-393.5 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(g)ΔH=+571.6 kJ·mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
D. C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)ΔH=-1 400 kJ·mol-1 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)ΔH=-1 400 kJ·mol-1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 Si(s)+4HCl(g)ΔH=+Q kJ·mol-1(Q>0)某溫度、壓強下,將一定量反應物通入密閉容器進行以上反應(此條件下為可逆反應),下列敘述正確的是( )。
Si(s)+4HCl(g)ΔH=+Q kJ·mol-1(Q>0)某溫度、壓強下,將一定量反應物通入密閉容器進行以上反應(此條件下為可逆反應),下列敘述正確的是( )。| A.反應過程中,若增大壓強能提高SiCl4的轉化率 |
| B.若反應開始時SiCl4為1 mol,則達到平衡時,吸收熱量為Q kJ |
| C.反應至4 min時,若HCl濃度為0.12 mol·L-1,則H2的反應速率為0.03 mol·(L·min-1) |
| D.當反應吸收熱量為0.025Q kJ時,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液中恰好反應 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題


 2CO2(g)+N2(g),已知該反應在570K時的平衡常數為1×1059,但反應速率極慢。下列說法正確的是:________
2CO2(g)+N2(g),已知該反應在570K時的平衡常數為1×1059,但反應速率極慢。下列說法正確的是:________| A.裝有尾氣凈化裝置的汽車排出的氣體中不再含有NO或CO |
| B.提高尾氣凈化效率的常用方法是升高溫度 |
| C.增大壓強,上述平衡右移,故實際操作中可通過增壓的方式提高其凈化效率 |
| D.提高尾氣凈化效率的最佳途徑是使用高效催化劑 |

 Ni(CO)4(g),鎳與CO反應會造成鎳催化劑中毒。為防止鎳催化劑中毒,工業上常用SO2除去CO,生成物為S和CO2。已知相關反應過程的能量變化如圖所示
Ni(CO)4(g),鎳與CO反應會造成鎳催化劑中毒。為防止鎳催化劑中毒,工業上常用SO2除去CO,生成物為S和CO2。已知相關反應過程的能量變化如圖所示

 2N2(g)+3H2O(g)△H<0。為提高氮氧化物的轉化率可采取的措施是(任意填一種)____________________。
2N2(g)+3H2O(g)△H<0。為提高氮氧化物的轉化率可采取的措施是(任意填一種)____________________。
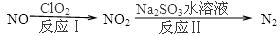
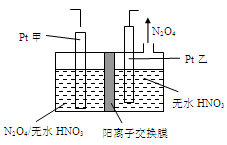
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題

| A.500mL 2.0mol·L-1 HCl和500mL 2.0mol·L-1 NaOH的反應符合圖1,且ΔE=57.3kJ |
| B.500mL 2.0mol·L-1 H2SO4和500mL 2.0mol·L-1 Ba(OH)2的反應符合圖2,且ΔE=114.6kJ |
| C.發生圖1能量變化的任何反應,一定不需加熱即可發生 |
| D.CaO、濃硫酸溶于水時的能量變化符合圖1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.“低碳經濟”是指減少對化石燃料的依賴,達到低污染、低排放的模式 |
| B.“低碳生活”倡導生活中耗用能量盡量減少,從而減少CO2的排放 |
| C.所有垃圾都可以采用露天焚燒或深埋的方法處理 |
| D.“靜電除塵”、“燃煤固硫”、“汽車尾氣催化凈化”都能提高空氣質量 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com