
【題目】實驗室利用反應![]() 合成洋茉莉醛的流程如下。下列說法錯誤的是
合成洋茉莉醛的流程如下。下列說法錯誤的是
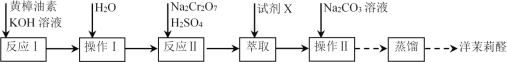
A.水洗的目的是除去KOHB.試劑X應選用有機溶劑
C.加入Na2CO3溶液的目的是除去酸D.進行蒸餾操作時可選用球形冷凝管
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】已知X+、Y2+、Z-、W2-四種離子均具有相同的電子層結構,下列關于X、Y、Z、W四種元素的描述,不正確的是( )
A. 原子半徑:X>Y>Z>WB. 原子序數:Y>X>Z>W
C. 原子最外層電子數:Z>W>Y>XD. 金屬性:X>Y,還原性:W2->Z-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)蘇打屬于________晶體,與鹽酸反應時需要破壞的化學鍵有_________。
(2)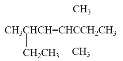 可與H2反應,請用系統命名法對其產物命名_________。
可與H2反應,請用系統命名法對其產物命名_________。
(3)在蔗糖與濃硫酸的黑面包實驗中,蔗糖會變黑并膨脹,請用化學方程式解釋膨脹的主要原因:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】欲用98%的濃硫酸(g=1.84g·cm-3)配制成濃度為0.5mol·L-1的稀硫酸500ml。
(1)選用的主要儀器有:
①__________,②__________,③__________,④____________,⑤____________。
(2)請將下列各操作,按正確的序號填在橫線上。
A.用量筒量取濃H2SO4 |
B.反復顛倒搖勻 |
C.用膠頭滴管加蒸餾水至刻度線 |
D.洗凈所用儀器 |
E.稀釋濃H2SO4
F.將溶液轉入容量瓶
其操作正確的順序依次為______________________。
(3)簡要回答下列問題:
①所需濃硫酸的體積為____________mL。
②如果實驗室有15mL、20mL、50mL的量筒應選用____________mL的量筒最好,量取時發現量筒不干凈用水洗凈后直接量取將使濃度__________(“偏高”、“偏低”、“無影響”)
③將濃硫酸沿燒杯內壁慢慢注入盛水的燒杯中,并用玻璃棒不斷攪拌的目的是____________,若攪拌過程中有液體濺出結果會使濃度偏____________。
④在轉入容量瓶前燒杯中液體應____________,否則會使濃度偏____________;并洗滌燒杯和玻璃棒2~3次,洗滌液也要轉入容量瓶,否則會使濃度____________。
⑤定容時必須使溶液凹液面與刻度線相切,若俯視會使濃度____________;仰視則使濃度___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義。
(1)2CO(g)=2C(s)+O2(g),該反應不能自發進行的原因是_____________________
(2)臭氧是一種殺菌消毒劑,還是理想的煙氣脫硝劑。一種脫硝反應中,各物質的物質的量隨時間的變化如圖所示,寫出該反應的化學方程式__________________________。
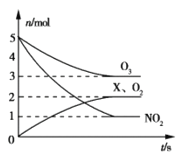
(3)利用脫氮菌可凈化低濃度NO廢氣。當廢氣在塔內停留時間均為90s的情況下,測得不同條件下NO的脫氮率如圖I、Ⅱ所示。
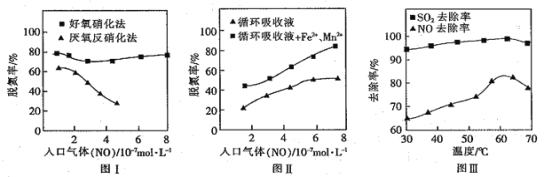
① 由圖I知,當廢氣中的NO含量增加時,宜選用________法提高脫氮的效率。
② 圖Ⅱ中,循環吸收液加入Fe2+、Mn2+,提高了脫氮的效率,其可能原因為________。
③研究表明:NaClO2/H2O2酸性復合吸收劑可同時有效脫硫、脫硝。圖Ⅲ所示為復合吸收劑組成一定時,溫度對脫硫脫硝的影響。溫度高于60℃后,NO去除率下降的原因為________。
(4)氨氮是造成水體富營養化的重要因素之一,用次氯酸鈉水解生成的次氯酸將水中的氨氮(用NH3表示)轉化為氮氣除去,涉及的相關反應如下:
反應①:NH3+HClO=NH2Cl+H2O
反應②:NH2Cl+HClO=NHCl2+H2O
反應③:2NHCl2+H2O=N2+HClO+3HCl
已知在水溶液中NH2Cl較穩定,NHCl2不穩定易轉化為氮氣。在其他條件一定的情況下,改變![]() (即NaClO溶液的投入量),溶液中次氯酸鈉對氨氮去除率及余氯量 (溶液中+1價氯元素的含量) 的影響如圖4所示。
(即NaClO溶液的投入量),溶液中次氯酸鈉對氨氮去除率及余氯量 (溶液中+1價氯元素的含量) 的影響如圖4所示。
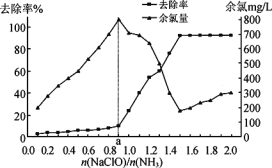
①反應中氨氮去除效果最佳的![]() 值約為_______。
值約為_______。
②a點之前氨氮去除率較低的原因為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 是重要的工業原料,鈾濃縮一直為國際社會關注。下列說法正確的是
是重要的工業原料,鈾濃縮一直為國際社會關注。下列說法正確的是
A. ![]() 原子核中含有92個中子 B.
原子核中含有92個中子 B. ![]() 原子核外有143個電子
原子核外有143個電子
C. ![]() 與
與![]() 互為同位素 D.
互為同位素 D. ![]() 與
與![]() 為同一核素
為同一核素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下圖表示的一些物質或概念間的從屬關系中正確的是
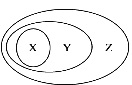
X | Y | Z | |
A | 水 | 單質 | 純凈物 |
B | 非金屬氧化物 | 酸性氧化物 | 氧化物 |
C | 電解質 | 化合物 | 純凈物 |
D | 化合反應 | 氧化還原反應 | 化學反應 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA是阿伏加德羅常數的值。下列說法正確的是
A.密閉容器中,2 mol NO 和 1 mol O2 反應后分子總數為 2NA
B.標準狀況下,7.8 g 乙炔和苯的混合物中含 C—H 鍵數目為 0.6NA
C.將 1 mol NH3 通入足量水中,NH3·H2O、NH4+粒子數目之和為 NA
D.1 L 0.1 mol·L1 FeCl3 溶液中含 Fe3+數目為 0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳酸亞鐵可用于制備補血劑。某研究小組制備了 FeCO3,并對 FeCO3 的性質和應用進行了探究。
已知:①FeCO3 是白色固體,難溶于水②Fe2++6SCN-Fe(SCN)64-(無色)
Ⅰ.FeCO3 的制取(夾持裝置略)
實驗i
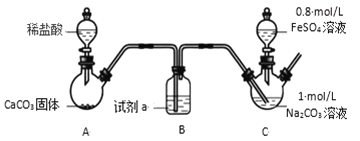
裝置 C 中,向 Na2CO3 溶液(pH=11.9)通入一段時間 CO2 至其 pH 為 7,滴加一定量 FeSO4溶液,產生白色沉淀,過濾、洗滌、干燥,得到 FeCO3 固體。
(1)試劑 a 是________。
(2)向 Na2CO3 溶液通入 CO2 的目的是________。
(3)C 裝置中制取 FeCO3 的離子方程式為________。
Ⅱ.FeCO3 的性質探究
實驗ii
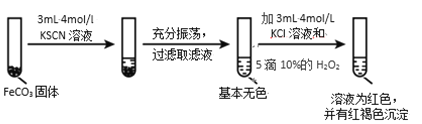
實驗iii
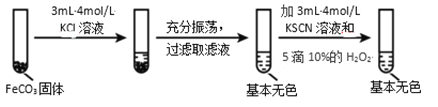
(4)對比實驗ⅱ和ⅲ,得出的實驗結論是________。
(5)依據實驗ⅱ的現象,寫出加入 10%H2O2 溶液的離子方程式________。
Ⅲ.FeCO3的應用
(6)FeCO3 溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亞鐵補血劑,此反應的離子方程式為____。
(7)該實驗小組用 KMnO4 測定補血劑中亞鐵含量進而計算乳酸亞鐵的質量分數,發現乳酸亞鐵的質量分數總是大于 100%,其原因是____(不考慮操作不當引起的誤差)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com