
【題目】危化倉庫中往往存有鈉、鉀、硫、白磷(P4)、硝酸銨和氰化鈉(NaCN)等危險品。請回答下列問題:
(1)NH4NO3為爆炸物,在某溫度下按下式進行分解:5NH4NO3=4N2↑+2HNO3+9H2O
則被氧化和被還原的氮元素質量之比為_____________;
(2)硫酸銅溶液是白磷引起中毒的一種解毒劑:1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
若6molH3PO4生成,則被CuSO4氧化的P4的物質的量為______________mol;
(3)NaCN屬于劇毒物質,有一種處理方法其原理為:CN-與S2O32-反應生成兩種離子,一種與Fe3+可生成紅色弱電解質,另一種與H+作用產生能使品紅溶液腿色的刺激性氣體,寫出離子反應方程式:__________________。
處理CN一還常用的一種方法是:用ClO一氧化處理生成CNO一,反應的離子方程式如下;
aCN-+bClO-+ 2cOH一=dCNO-+eN2↑+fCO32-+bCl-+cH2O
上述化學方程式可能的配平化學計量數有多組,回答下列問題:
①方程式中e:f的值為_________(填字母);
A.1 B.1/2 C.2 D.不能確定
②若d=e=l,則b=_________。
【答案】 5:3 0.75 CN-+S2O32-=SCN-+SO32- B 6
【解析】(1)5NH4NO3═2HNO3+4N2↑+9H2O的反應中,氮元素由銨根中-3價升高為0價,被氧化,氮元素由硝酸根中+5價降低為0價,被還原,根據電子轉移守恒,可知被氧化的氮原子與被還原的氮原子物質的量之比為(5-0):[0-(-3)]=5:3,則被氧化和被還原的氮元素質量之比為5:3,故答案為:5:3;
(2)Cu元素的化合價由+2價降低到+1價,CuSO4是氧化劑,P4中部分磷元素由0價降低到-3價,部分磷元素由0價升高到+5價,磷元素的化合價既升高又降低,所以P4既是氧化劑又是還原劑,若6molH3PO4生成,則參加反應CuSO4為6mol×![]() =15mol,根據電子轉移守恒,被CuSO4氧化的P4的物質的量為
=15mol,根據電子轉移守恒,被CuSO4氧化的P4的物質的量為![]() =0.75mol,故答案為:0.75;
=0.75mol,故答案為:0.75;
(3)CN-與S2O32-反應生成兩種離子,一種與Fe3+可生成紅色弱電解質,另一種與H+作用產生能使品紅溶液腿色的刺激性氣體,反應生成SCN-與SO32-,反應離子方程式為:CN-+S2O32-=SCN-+SO32-,故答案為:CN-+S2O32-=SCN-+SO32-;
①由CN-離子中碳與氮原子之比為1:1,而碳氮轉化為CNO-和N2以及CO32-,以因為CNO-離子碳氮之比為1:1,所以N2和CO32-兩微粒之比為1:2,所以e:f=1:2,故答案為:B;
②反應aCN-+bClO-+2cOH-=dCNO-+eN2↑+fCO32-+bCl-+cH2O,若d=e=1,根據碳與氮原子之比為1:1,則f=2,由碳元素化合價升高1×2+2×2=6,氮元素化合價升高2×3=6,氯元素化合價降低為6,根據得失電子守恒得到b×2=12,b=6,故答案為:6。


 浙大優學小學年級銜接捷徑浙江大學出版社系列答案
浙大優學小學年級銜接捷徑浙江大學出版社系列答案科目:高中化學 來源: 題型:
【題目】高聚物…—CH2—CH2—CH2—…是用下列何種物質聚合成的( )
A. CH3—CH3 B. CH3—CH2—CH3
C. CH2=CH2 D. CH2=CH—CH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于各圖的敘述正確的是
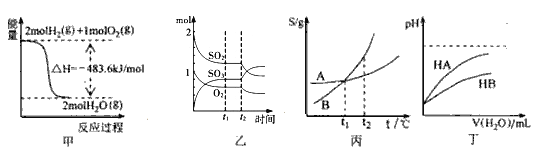
A. 圖甲表示H2與O2發生反應過程中的能量變化,則H2的燃燒熱為241.8 kJmol-1
B. 圖乙表示一定條件下進行的反應2SO2+O2![]() 2SO3各成分的物質的量變化,t2時刻改變的條件一定是縮小容器體積
2SO3各成分的物質的量變化,t2時刻改變的條件一定是縮小容器體積
C. 圖丙表示A、B兩物質的溶解度隨溫度變化情況,將t1℃時A、B的飽和溶液分別升溫至t2℃時,溶質的質量分數ω(B)>ω(A)
D. 圖丁表示常溫下,稀釋HA、HB兩種酸的稀溶液時,溶液pH隨加水量的變化,則NaA溶液的pH小于同濃度的NaB溶液的pH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在空氣中直接蒸發下列鹽的溶液:①Fe2(SO4)3 ②Na2CO3 ③KC1 ④CuCl2 ⑤NaHCO3可以得到相應鹽的晶體(可以含有結晶水)的是( )
A.①③⑤ B.①②③ C.②④ D.①③④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A2On2-可將B2-氧化為B單質,A2On2-則被還原為A3+,又知100mL的0.3mol/L的A2On2-與150mL的0.6mol/L B2-恰好完全反應,則A2On2-中的n值為
A.4 B.5 C.6 D.7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】固體X是由兩種常見元素組成的化合物,其中金屬元素與另一元素的質量比為14:1。在一定條件下X可發生如圖的轉化關系,有的反應標出全部產物,有的反應標出部分產物。已知P為氣體混合物,R是一種無色無味能使澄清石灰水變渾濁的氣體,C為紅褐色沉淀,M為一種常見金屬單質。

試回答下列問題:
(1)X的化學式為__________。
(2)實現G→H,欲不引進新的雜質,N可以選擇下列物質中的_________(填序號)。
①KMnO4 ②HNO3 ③H2O2 ④Cl2
(3)寫出下列轉化的化學方程式:
B→D:____________________;H→C:____________________。
(4)已知P中有一種氣體與氫氧化鈉溶液反應可生成兩種正鹽,該反應的離子方程式為:___________。
(5)X與濃硝酸在一定條件下反應時,若有1 mol X被氧化時,轉移的電子數目為__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com