
【題目】NA表示阿伏加德羅常數的數值,下列說法正確的是
A. 在標準狀況下,11.2L HF含有的分子數目為0.5NA
B. 高溫下,16.8 g Fe與足量水蒸氣完全反應失去0.8NA個電子
C. 常溫下,0.2 L 0.5 mol·L-1 NH4NO3溶液中含有的氮原子數小于0.2NA
D. 18g葡萄糖(C6H12O6)分子含有的羥基數目為0.6NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】(1) 與氫氣反應的化學方程式是__________;
與氫氣反應的化學方程式是__________;
(2)寫出正戊烷CH3(CH2)3CH3的兩種同分異構體的結構簡式和名稱(系統命名法):
①結構簡式:_____________、名稱:_____________
②結構簡式:_____________、名稱:_____________。
(3)某一氯代烷烴分子中有2個“-CH3”、2個“-CH2-”、1個“ ”和1個“-Cl”,符合上述條件的有機物共四種,寫出它們的結構簡式:
”和1個“-Cl”,符合上述條件的有機物共四種,寫出它們的結構簡式:![]() 、
、 、_________、_________。
、_________、_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度恒定的條件下,在2 L容積不變的密閉容器中,發生反應:2SO2(g)+O2(g) ![]() 2SO3(g)。開始充入4 mol的SO2和2 mol的O2,10 s后達到平衡狀態,此時c(SO3)=0.5 mol·L-1,下列說法不正確的是 ( )
2SO3(g)。開始充入4 mol的SO2和2 mol的O2,10 s后達到平衡狀態,此時c(SO3)=0.5 mol·L-1,下列說法不正確的是 ( )
A.v(SO2)∶v(O2)=2∶1B.10 s內,v(SO3)=0.05 mol·L-1·s-1
C.SO2的平衡轉化率為25%D.平衡時容器內的壓強是反應前的5/6倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A可由葡萄糖發酵得到,也可從酸牛奶中提取。純凈的A為無色粘稠液體,易溶于水。為研究A的組成與結構,進行了如下實驗:
(1)稱取A9.0g,升溫使其汽化,測其密度是相同條件下H2的45倍。則A的相對分子質量為:______。
(2)將此9.0gA在足量純O2充分燃燒,并使其產物依次緩緩通過濃硫酸、堿石灰,發現兩者分別增重5.4g和13.2g。則A的分子式為:________。
(3)另取A9.0g,跟足量的NaHCO3粉末反應,生成2.24LCO2(標準狀況),若與足量金屬鈉反應則生成2.24LH2(標準狀況)。用結構簡式表示A中含有的官能團:______________________。
(4)A的核磁共振氫譜如下圖:則A中含有__________種氫原子。
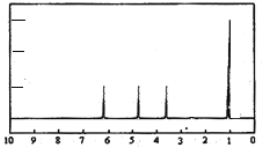
(5)綜上所述,A的結構簡式_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】沉淀的生成、溶解和轉化在無機物制備和提純以及科研等領域有廣泛應用。已知25℃時,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
(1)將濃度均為0.1 mol·L-1的BaCl2溶液與Na2SO4溶液等體積混合,充分攪拌后過濾,濾液中c(Ba2+)=_____mol·L-1。
(2)醫學上進行消化系統的X射線透視時,常使用BaSO4作內服造影劑。胃酸酸性很強( pH約為1), 但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是_______________________。(用沉淀溶解平衡原理解釋)。萬一誤服了少量BaCO3,應盡快用大量0.5mol·L-1Na2SO4溶液給患者洗胃,如果忽略洗胃過程中Na2SO4溶液濃度的變化,殘留在胃液中的Ba2+濃度僅為________mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A.1 mol S和O2的摩爾質量都是32 g
B.23g NO2和N2O4的混合氣體中所含的O原子數為NA
C.1 mol任何氣體中都含有相同的原子數
D.22.4 L CO2氣體中含有3NA個原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硝酸鋁[Al(NO3)3]是一種常用媒染劑。工業上用鋁灰(主要含Al、Al2O3、Fe2O3等)制取硝酸鋁晶體[Al(NO3)3·9H2O]的流程如下:
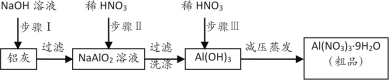
完成下列填空:
(1)常溫下,鋁遇濃硫酸、濃硝酸時在表面生成致密的氧化膜,這種現象稱為__________,鋁粉常用來還原一些金屬氧化物以冶煉某些難熔的金屬,這類氧化還原反應叫__________反應;
(2)步驟Ⅰ的離子方程式是_________________,_________________;
(3)若在實驗室中完成步驟Ⅱ,為提高鋁元素的利用率,可用__替換稀硝酸;
a.稀硫酸 b.稀鹽酸 c.醋酸 d.二氧化碳
(4)在步驟Ⅲ的實際操作過程中,待沉淀完全溶解后還會加入稍過量稀硝酸,用平衡移動原理解釋此時加入稀硝酸的目的:_______________________;
(5)溫度高于200℃時,硝酸鋁完全分解成氧化鋁、二氧化氮和氧氣,寫出該反應的化學方程式:_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積為2 L的密閉容器中發生反應xA(g)+yB(g)![]() zC(g)。圖甲表示200 ℃時容器中A、B、C物質的量隨時間的變化,圖乙表示不同溫度下平衡時C的體積分數隨起始n(A)∶n(B)的變化關系。則下列結論正確的是( )
zC(g)。圖甲表示200 ℃時容器中A、B、C物質的量隨時間的變化,圖乙表示不同溫度下平衡時C的體積分數隨起始n(A)∶n(B)的變化關系。則下列結論正確的是( )
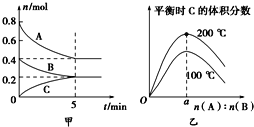
A. 200℃時,反應從開始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B. 200℃時,該反應的平衡常數為25
C. 當外界條件由200℃降溫到100℃,原平衡一定被破壞,且正逆反應速率均增大
D. 由圖乙可知,反應xA(g)+yB(g)![]() zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 0.1 mol H2中含有的分子數為6.02×1022
B. 24 g Mg變成Mg2+時失去的電子數為6.02×1023
C. 1 L 1 mol·L-1 CaCl2溶液中含有的Cl-數為6.02×1023
D. 常溫常壓下,11.2 L O2中含有的原子數為6.02×1023
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com