
ĪŠŅ}─┐Ī┐ĪŠ╗»īW-▀xą▐3Ż║╬’┘|ĮYśŗ║═ąį┘|Ī┐ ╔ķĄ─ę╗ą®╗»║Ž╬’│Żė├ū„░ļī¦¾wĪó│²▓▌ä®ĪóÜó╩¾╦ÄĄ╚Ż¼╗ž┤Ž┬┴ąå¢Ņ}Ż║
Ż©1Ż®īæ│÷╗∙æB╔ķįŁūėĄ─ļŖūė┼┼▓╝╩Į_________________Ż╗ėą_________________éĆ╬┤│╔ī”ļŖūėĪŻ
Ż©2Ż®╝┌Ą¬╔ķ║ŽĮ▓─┴ŽĄ─╠½Ļ¢─▄ļŖ│žą¦┬╩▀_40%ĪŻGaĪóNĪóAsļŖžōąįė╔┤¾ĄĮąĪĄ─Ēśą“╩Ū____________Ż╗
Ż©3Ż®As4O6Ą─ĘųūėĮYśŗ╚ńłD╦∙╩ŠŻ¼ŲõųąAsįŁūėĄ─ļs╗»ĘĮ╩Į×ķ______________Ż¼1mol As4O6║¼ėą![]() µIĄ─╬’┘|Ą─┴┐×ķ____________molĪŻ
µIĄ─╬’┘|Ą─┴┐×ķ____________molĪŻ

Ż©4Ż®As┼cN╩Ū═¼ūÕį¬╦žŻ¼AsH3Ą─Ęą³c▒╚NH3Ą─Ęą³c Ż¼įŁę“╩Ū ĪŻ
Ż©5Ż®H3AsO4║═H3AsO3╩Ū╔ķĄ─ā╔ĘN║¼č§╦߯¼Ė∙ō■ĮYśŗ┼cąį┘|Ą─ĻPŽĄŻ¼H3AsO4Ą─╦ßąį▒╚H3AsO3ÅŖĄ─įŁę“╩ŪŻ║ ĪŻ
Ż©6Ż®Š¦░¹ėąā╔éĆ╗∙▒Šę¬╦ž
ó┘įŁūėū°ś╦ģóöĄŻ¼▒Ē╩ŠŠ¦░¹ā╚▓┐Ė„įŁūėĄ─ŽÓī”╬╗ų├Ż¼LiZnAs╗∙ŽĪ┤┼░ļī¦¾wĄ─Š¦░¹╚ńłD╦∙╩ŠŻ¼ŲõųąįŁūėū°ś╦ģóöĄA╠ÄLi×ķ(0Ż¼0Ż¼1/2)Ż╗B╠ÄAs×ķ(1/4Ż¼1/4Ż¼1/4)Ż╗C╠ÄLiĄ─ū°ś╦ģóöĄ×ķ ĪŻ
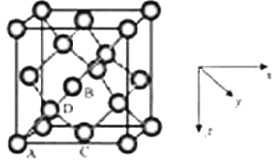
ó┌Š¦░¹ģóöĄŻ¼├Ķ╩÷Š¦░¹Ą─┤¾ąĪ║═ą╬ĀŅŻ¼ęčų¬LiZnAså╬Š¦Ą─Š¦░¹ģóöĄŻ¼a=594pmŻ¼NA▒Ē╩Š░óĘ³┘żĄ┬┴_│ŻöĄĄ─öĄųĄŻ¼Ųõ├▄Č╚×ķ gcm-3(┴ą│÷ėŗ╦Ń╩Į╝┤┐╔)ĪŻ
ĪŠ┤░ĖĪ┐
Ż©1Ż®[Ar]3d104s24p3Ż╗3Ż╗
Ż©2Ż®N>As>GaŻ╗Ż©3Ż®sp3Ż╗12Ż╗
Ż©4Ż®Ą═Ż╗AsH3Ęųūėķg▓╗─▄ą╬│╔ÜõµIŻ¼Č°NH3Ęųūėķg─▄ą╬│╔ÜõµIŻ╗
Ż©5Ż®H3AsO4║═H3AsO3┐╔Ęųäe▒Ē╩Š×ķ(HO)3AsO║═(HO)3AsŻ¼H3AsO3ųąĄ─As×ķ+3ārŻ¼Č°H3AsO4ųąĄ─As×ķ+5ārŻ¼š²ļŖąįĖ³Ė▀Ż¼ī¦ų┬As-O-HųąOĄ─ļŖūėŽ“AsŲ½ęŲŻ¼Ė³ęūļŖļx│÷H+ļxūėŻ╗
Ż©6Ż®ó┘![]() Ż╗ó┌
Ż╗ó┌![]() Ż╗
Ż╗
ĪŠĮŌ╬÷Ī┐
įćŅ}Ęų╬÷Ż║Ż©1Ż®AsĄ─įŁūėą“öĄ×ķ33Ż¼ė╔śŗįņįŁ└Ē┐╔ų¬ļŖūė┼┼▓╝×ķ1s22s22p63s23p63d104s24p3Ż¼ėą3éĆ╬┤│╔ī”ļŖūėŻ¼╣╩┤░Ė×ķ1s22s22p63s23p63d104s24p3Ż╗3Ż╗
Ż©2Ż®═¼ų▄Ų┌ļSįŁūėą“öĄ▀fį÷ļŖžōąįį÷┤¾Ż¼Ga║═As═¼ų▄Ų┌Ż¼AsĄ─įŁūėą“öĄ▌^┤¾Ż¼╣╩ļŖžōąį▌^┤¾Ą─╩ŪAsŻ╗As╠Äė┌ó§AūÕŻ¼═¼ų„ūÕį¬╦žŻ¼ļSįŁūėą“öĄ▀fį÷ļŖžōąį£pąĪŻ¼GaĪóNĪóAsļŖžōąįė╔┤¾ĄĮąĪĄ─Ēśą“N>As>GaŻ¼╣╩┤░Ė×ķŻ║N>As>GaŻ╗
Ż©3Ż®Ė∙ō■ĮYśŗ╩ŠęŌłDŻ¼AsĄ─ārīėļŖūėī”öĄ=3+1=4Ż¼▓╔ė├sp3ļs╗»Ż¼1mol As4O6║¼ėą![]() µIĄ─╬’┘|Ą─┴┐×ķ3Ī┴4mol=12molŻ¼╣╩┤░Ė×ķŻ║sp3Ż╗12Ż╗
µIĄ─╬’┘|Ą─┴┐×ķ3Ī┴4mol=12molŻ¼╣╩┤░Ė×ķŻ║sp3Ż╗12Ż╗
Ż©4Ż®AsH3║═NH3ą╬│╔Ą─Š¦¾wŠ∙╩ŪĘųūėŠ¦¾wŻ¼ŲõĘą³c╩▄Ęųūėķgū„ė├┴”┤¾ąĪĄ─ė░ĒæŻ¼ī”ė┌ĮM│╔║═ĮYśŗŽÓ╦ŲĄ─╬’┘|Ęųūėķgū„ė├┴”║═ŲõŽÓī”įŁūė┘|┴┐│╔š²▒╚Ż¼─▄ē“ą╬│╔ÜõµIĄ─Ęą³c╔²Ė▀Ż¼NH3Ęųūėķg─▄ą╬│╔ÜõµIŻ¼AsH3Ęųūėķg▓╗─▄ą╬│╔ÜõµIŻ¼ę“┤╦AsH3Ą─Ęą³c▒╚NH3Ą─Ęą³cĄ═Ż¼╣╩┤░Ė×ķŻ║Ą═Ż╗AsH3Ęųūėķg▓╗─▄ą╬│╔ÜõµIŻ¼Č°NH3Ęųūėķg─▄ą╬│╔ÜõµIŻ╗
Ż©5Ż®H3AsO4║═H3AsO3┐╔▒Ē╩Š×ķ(HO)3AsO║═(HO)3 AsŻ¼H3AsO3ųąĄ─As×ķ+3ārŻ¼Č°H3AsO4ųąĘŪ┴u╗∙č§▌^ČÓĪóAs×ķ+5ārŻ¼š²ļŖąįĖ³Ė▀Ż¼ī¦ų┬As-O-HųąĄ─OĄ─ļŖūėĖ³Ž“AsŲ½ęŲŻ¼įĮęūļŖļx│÷H+Ż¼╣╩┤░Ė×ķŻ║H3AsO4║═H3AsO3┐╔▒Ē╩Š×ķ(HO)3AsO║═(HO)3 AsŻ¼H3AsO3ųąĄ─As×ķ+3ārŻ¼Č°H3AsO4ųąĘŪ┴u╗∙č§▌^ČÓĪóAs×ķ+5ārŻ¼š²ļŖąįĖ³Ė▀Ż¼ī¦ų┬As-O-HųąĄ─OĄ─ļŖūėĖ³Ž“AsŲ½ęŲŻ¼įĮęūļŖļx│÷H+Ż╗
Ż©6Ż®ó┘D┼cų▄ć·4éĆįŁūėą╬│╔š²╦─├µ¾wĮYśŗŻ¼D┼cĒö³cAĄ─▀BŠĆ╠Äė┌Š¦░¹¾wī”ĮŪŠĆ╔ŽŻ¼▀^├µą─BĪóC╝░╔ŽĄū├µ├µą─įŁūėĄ─ŲĮ├µŪęŲĮąąé╚├µīóŠ¦░¹2Ą╚ĘųŻ¼═¼└Ē▀^DįŁūėĄ─ŪęŲĮŲĮąąé╚├µĄ─ŲĮ├µīó░ļéĆŠ¦░¹į┘2Ą╚Ę▌Ż¼┐╔ų¬D╠Äė┌ĄĮĖ„éĆ├µĄ─![]() ╠ÄŻ¼ätCįŁūėĄ─ū°ś╦ģóöĄ×ķ(
╠ÄŻ¼ätCįŁūėĄ─ū°ś╦ģóöĄ×ķ(![]() Ż¼
Ż¼![]() Ż¼
Ż¼![]() )Ż¼╣╩┤░Ė×ķŻ║(
)Ż¼╣╩┤░Ė×ķŻ║(![]() Ż¼
Ż¼![]() Ż¼
Ż¼![]() )Ż╗
)Ż╗
ó┌1éĆŠ¦░¹ųąĘųäe║¼ėą4éĆLiĪóZnĪóAsįŁūėŻ¼1molŠ¦░¹Ą─┘|┴┐×ķ4Ī┴147gŻ¼1molŠ¦░¹Ą─¾wĘe×ķ (594Ī┴10-10)3NAcm3Ż¼ät├▄Č╚×ķ![]() gcm-3Ż¼╣╩┤░Ė×ķŻ║
gcm-3Ż¼╣╩┤░Ė×ķŻ║![]() ĪŻ
ĪŻ


 ABC┐╝═§╚½ā׊ĒŽĄ┴ą┤░Ė
ABC┐╝═§╚½ā׊ĒŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąšfĘ©š²┤_Ą─╩Ū
AŻ«─”Ā¢╩Ūć°ļHå╬╬╗ųŲųąĄ─Ų▀éĆ╗∙▒Š╬’└Ē┴┐ų«ę╗
BŻ«1molO2ųą╝s║¼ėą6.02Ī┴1023éĆO2
CŻ«1mol╚╬║╬╬’┘|Č╝║¼ėą6.02Ī┴1023éĆįŁūė
DŻ«─”Ā¢▒Ē╩Š╬’┘|Ą─┴┐
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąĻPė┌╝Ü░¹ā╚į¬╦ž║═╗»║Ž╬’Ą─öó╩÷Ż¼Õeš`Ą─╩Ū
A. ĮM│╔╝Ü░¹Ė╔ųžųą║¼┴┐ūŅČÓĄ─╗»īWį¬╦ž╩Ū╠╝
B. ┴ū╩Ū┴ūų¼ĪóATPĪóDNAĄ╚╗»║Ž╬’Ą─ĮM│╔į¬╦žŻ¼╩ŪĮM│╔╔·╬’¾wĄ─┤¾┴┐į¬╦ž
C. ŠĆ┴Ż¾wĪó╚~ŠG¾w║═║╦╠Ū¾wųąČ╝─▄«a╔·╦«
D. į┌╝Ü░¹Ą─ę╗╔·ųąŻ¼╝Ü░¹ųąĄ─ūįė╔╦«/ĮY║Ž╦«Ą─ųĄųØu╔Ž╔²
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ą╬’┘|ųąŻ¼╝╚║¼ėąļxūėµIŻ¼ėų║¼ėąĘŪśOąį╣▓ārµIĄ─╩Ū
A. Na2O2 B. CaCl2 C. NH4Cl D. H2O
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐─│ÅUę║ųą║¼ėą┤¾┴┐Ą─KŻ½ĪóClŻŁĪóBrŻŁŻ¼▀Ćėą╔┘┴┐Ą─Ca2Ż½ĪóMg2Ż½ĪóSO42ĪźĪŻ─│蹊┐ąįīW┴ĢąĪĮM└¹ė├▀@ĘNÅUę║üĒųŲ╚Ī▌^╝āā¶Ą─┬╚╗»ŌøŠ¦¾w╝░ę║õÕ(Br2)Ż¼įOėŗ┴╦╚ńłD╦∙╩ŠĄ─┴„│╠łDŻ║
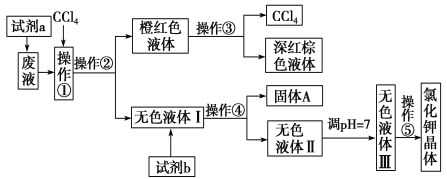
┐╔╣®įćä®aĪóįćä®b(įćä®b┤·▒Ēę╗ĮMįćä®)▀xō±Ą─įć䮯║’¢║═Na2CO3╚▄ę║Īó’¢║═K2CO3╚▄ę║ĪóKOH╚▄ę║ĪóBaCl2╚▄ę║ĪóBa(NO3)2╚▄ę║ĪóH2O2╚▄ę║Īó╦ßąįKMnO4╚▄ę║ĪóŽĪ¹}╦ßĪŻ
šłĖ∙ō■┴„│╠łDŻ¼╗ž┤ŽÓĻPå¢Ņ}Ż║
Ż©1Ż® ▓┘ū„ó┘ó┌ó█ó▄ó▌Ą─├¹ĘQ╩Ū_____________
ó┘_______ó┌________ó█________ó▄________ó▌________
Ż©2Ż® │²╚ź¤o╔½ę║¾wó±ųąĄ─Ca2Ż½ĪóMg2Ż½ĪóSO42ĪźŻ¼▀x│÷įćä®b╦∙┤·▒ĒĄ─įć䮯¼░┤Ą╬╝ėĒśą“ę└┤╬╩Ū________________(╠Ņ╗»īW╩Į)ĪŻ
Ż©3Ż®š{╣ØpHĄ──┐Ą─╩Ū____________________Ż¼▓┘ū„ĘĮĘ©╩Ū_______________________ĪŻ
Ż©4Ż®▓┘ū„ó▌ųąė├ĄĮĄ─┤╔┘|āxŲ„├¹ĘQ╩Ū ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąīŹ“×āxŲ„▓╗ę╦ų▒Įėė├üĒ╝ė¤ßĄ─╩Ū
A. įć╣▄ B. █ßłÕ C. ¤²▒Ł D. ▓Ż┴¦░¶
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąĻPė┌╝Ü░¹ųą╠╝į¬╦žĄ─šfĘ©Ż¼š²┤_Ą─╩Ū
A. ╠╝╩Ūš╝╚╦¾w╝Ü░¹§rųžūŅČÓĄ─į¬╦ž
B. ║╦╦ßĪó┴ūų¼ĪóĄ░░ū┘|Š∙║¼╠╝į¬╦ž
C. śŗ│╔╝Ü░¹Ą─╗»║Ž╬’Š∙ęį╠╝µ£×ķ╣Ū╝▄
D. ╠╝ī┘ė┌╝Ü░¹ųąĄ─╬ó┴┐į¬╦ž
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąĻPė┌╦«į┌╚╦¾wųąĄ─ū„ė├Õeš`Ą─╩ŪŻ© Ż®
AŻ«╠ß╣®─▄┴┐ BŻ«ū÷ĀIB╬’┘|╦«ĮŌĄ─Ę┤æ¬╬’ CŻ«ū÷╚▄ä® DŻ«š{╣ؾw£ž
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ż©1Ż®õX¤ßĘ┤æ¬╩ŪõXĄ─ę╗éĆųžę¬ąį┘|Ż¼įōąį┘|ė├═Š╩«ĘųÅVĘ║Ż¼▓╗āH▒╗ė├ė┌║ĖĮėõō▄ēŻ¼Č°Ūę▀Ć│Ż▒╗ė├ė┌ę▒¤ÆĖ▀╚█³cĄ─Įī┘╚ńŌCĪóŃtĪóÕiĄ╚ĪŻ

ó┘─│ąŻ╗»īW┼d╚żąĪĮM═¼īWŻ¼╚Ī┤┼ąįč§╗»ĶF░┤Į╠▓─ųąĄ─īŹ“×čbų├Ż©╚ńłD╝ūŻ®▀MąąõX¤ßĘ┤æ¬Ż¼¼FŽ¾║▄ēčė^ĪŻ╚ĪĘ┤æ¬║¾Ą─Ī░ĶFēKĪ▒╚▄ė┌¹}╦߯¼Ž“ŲõųąĄ╬╝ėKSCN╚▄ę║Ż¼░l¼F╚▄ę║ūāč¬╝t╔½ĪŻ│÷¼F▀@ĘN¼FŽ¾Ą─įŁę“Ż¼│²┴╦┐╔─▄╗ņėąø]Ę┤æ¬═ĻĄ─┤┼ąįč§╗»ĶF═ŌŻ¼▀Ćėąę╗éĆįŁę“╩Ū Ż╗
ó┌╚¶ūC├„╔Ž╩÷╦∙Ą├Ī░ĶFēKĪ▒ųą║¼ėąĮī┘õXŻ¼┐╔▀xō± Ż©╠Ņįćä®├¹ĘQŻ®Ż¼╦∙░l╔·Ę┤æ¬Ą─ļxūėĘĮ│╠╩Į×ķ Ż╗
Ż©2Ż®¼FėąFeCl3ĪóAlCl3Ą─╗ņ║Ž╚▄ę║100mL,ųĄ╬╝ė╚ļNaOH╚▄ę║Ż¼╔·│╔│┴ĄĒĄ─╬’┘|Ą─┴┐ļS╝ė╚ļĄ─NaOHĄ─╬’┘|Ą─┴┐Ą─ĻPŽĄ╚ńłDŻ¼
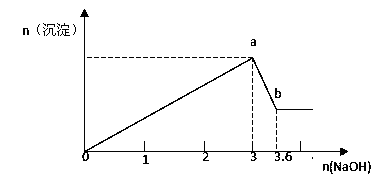
šłėŗ╦Ń│÷ó┘a╠Ä│┴ĄĒĄ─┐é╬’┘|Ą─┴┐ mol;
ó┌cŻ©FeCl3Ż®= mol/LŻ╗ó█cŻ©AlCl3Ż®= mol/L
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com