
(15分)資料顯示:鎂與飽和碳酸氫鈉溶液反應產生大量氣體和白色不溶物。某同學通過如下實驗探究反應原理并驗證產物。
實驗I:用砂紙擦去鎂條表面氧化膜,將其放入盛適量滴有酚酞的飽和碳酸氫鈉溶液的燒杯中,迅速反應,產生大量氣泡和白色不溶物,溶液的淺紅色加深。
(1)該同學對反應中產生的白色不溶物做出如下猜測:
猜測1:白色不溶物可能為
猜測2:白色不溶物可能為MgCO3
猜測3:白色不溶物可能為堿式碳酸鎂[xMg(OH)2?yMgCO3]
(2)為了確定產物成份(包括產生的氣體、白色不溶物及溶液中溶質),進行以下定性實驗。請填寫表中空白:
| 實驗序號 | 實 驗 | 實驗現象 | 結 論 |
| 實驗Ⅱ | 將實驗I中收集到的氣體點燃 | 安靜燃燒,火焰呈淡藍色 | 氣體成分為 ① |
| 實驗Ⅲ | 將實驗I中的白色不溶物濾出、洗滌,取少量加入足量 ② | ③ | 白色不溶物中含有MgCO3 |
| 實驗Ⅳ | 取實驗Ⅲ中的濾液,向其中加入適 量 ④ 稀溶液 | 產生白色沉淀,溶液紅色變淺 | 溶液中存在CO32-離子 |

(1)猜測1: Mg(OH)2(2分)
(2)①氫氣(或H2)(1分)
②稀鹽酸(合理均可)(2分)
③產生氣泡,沉淀全部溶解 (2分)
④CaCl2或BaCl2(2分)
(3)①防止空氣中的水蒸氣和CO2進入裝置B中,影響實驗結果(2分)
②Mg(OH)2?2MgCO3 或 Mg3(OH)2(CO3)2 (2分)
(4)3Mg+4NaHCO3+2H2O= Mg(OH)2? 2MgCO3↓+2Na2CO3+3H2↑(2分)
解析試題分析:⑴根據猜測2、3的內容可確定猜測1為“白色不溶物可能為Mg(OH)2”;
⑵實驗Ⅱ:根據氣體的火焰呈淡藍色,可確定氣體的成分為氫氣;
實驗Ⅲ:結合Mg(OH)2、MgCO3的性質,可用稀鹽酸等與其反應,若產生氣泡,且沉淀全部溶解,說明白色不溶物中含有MgCO3;
實驗Ⅳ:要證明溶液中存在CO32-離子,可向實驗Ⅲ的濾液中加入CaCl2或BaCl2,觀察是否產生白色沉淀來證明;
⑶①裝置末端用堿石灰吸收空氣中水蒸氣和CO2,防止其進入裝置B中,影響實驗結果;
②根據xMg(OH)2?yMgCO3的灼燒反應:xMg(OH)2?yMgCO3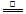 (x+y)MgO+xH2O+yCO2
(x+y)MgO+xH2O+yCO2
有n(H2O)=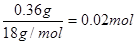 ;n(CO2)=
;n(CO2)=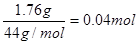 ,則x:y=1:2,即得白色不溶物的化學式為Mg(OH)2?2MgCO3或Mg3(OH)2(CO3)2。
,則x:y=1:2,即得白色不溶物的化學式為Mg(OH)2?2MgCO3或Mg3(OH)2(CO3)2。
⑷綜上可得該反應的反應物有Mg、NaHCO3,生成物有Mg(OH)2? 2MgCO3、Na2CO3、H2,最后根據觀察法將其配平。
考點:本題以“鎂與飽和碳酸氫鈉溶液反應”為素材考查實驗探究。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:實驗題
(20分)某研究性學習小組在實驗室中配制0.20mol·L-1的鹽酸標準溶液,然后用其滴定某未知濃度的氫氧化鈉溶液。
⑴配制待測液:將1.7 g含有少量雜質(不與鹽酸反應)的固體燒堿樣品配制成200 mL溶液,所需的主要玻璃儀器除燒杯,200 mL容量瓶,量筒,還有 ﹑ 。
⑵滴定:
①盛裝0.20mol·L-1鹽酸標準液應該用 式滴定管,
②滴定時,先向錐型瓶中加酚酞作為指示劑;再逐滴滴定,觀察到 時為滴定終點。
③有關數據記錄如下:
| 滴定序號 | 待測液體體積(mL) | 所耗鹽酸標準液的體積(mL) | |
| 起始讀數 滴定前 | 終點讀數 | ||
| 1 | 20.00 | 0.50 | 20.40 |
| 2 | 20.00 | 6.00 | 26.10 |
| 3 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某同學旅游時發現,苗族人的銀飾美麗而富有民族文化,制作銀飾時可以選用Fe(NO3)3溶液做蝕刻劑。受此啟發,該同學所在的化學興趣小組在實驗室選用Fe(NO3)3溶液清洗做過銀鏡反應的試管,發現不但銀鏡溶解,而且較少產生刺激性氣體。
化學興趣小組對Fe(NO3)3溶液溶解銀的原理進行探究:
【提出假設】假設1: Fe(NO3)3溶液顯酸性,在此酸性條件下NO3-能氧化Ag;
假設2:Fe3+具有氧化性,能氧化Ag
【驗證假設】
(1)甲同學驗證假設1。
①他用淡紫色的Fe(N03)3·9H20晶體(分析純,Mr=404)配制1.5mol/L的Fe(N03)3落液100mL。需要稱取_____g Fe(N03)3·9H20晶體,配制過程中所用到的儀器除燒杯、玻璃棒外還必需:__________
②測得1.5 mol/L的Fe(NO3)3溶液pH約為1,其原因用化學用語表示為____。
③將pH=1的HN03溶液加入到鍍有銀鏡的試管中,振蕩,觀察到銀鏡慢慢溶解,產生無色氣體并在液面上方變為紅棕色,溶液中發生反應的離子方程式應是_____
④將1.5mol/L的Fe(NO3)3溶液加入到鍍有銀鏡的試管中,振蕩,觀察到銀鏡很快溶解,并且溶液顏色加深。
(2)乙同學驗證假設2。分別用溶質的質量分數為2%、10%的足量FeCl3溶液加入到鍍有銀鏡的試管中,振蕩,都看不出銀鏡溶解。乙同學由此得出結論,假設2不成立。
你是否同意乙的結論?_______,簡述理由:_______
【思考與交流】I甲同學的實驗④中,溶液顏色為什么會加深?查閱資料得知,Fe2+能與NO形成配離子: (棕色)。已知,同濃度的硝酸氧化性比Fe3+略強。
(棕色)。已知,同濃度的硝酸氧化性比Fe3+略強。
根據以上信息綜合分析,濃、稀Fe(N03)3溶液溶解銀鏡時,發生的反應有何不同?
__________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有A、B、C、D、E五種易溶于水的強電解質,它們由如下離子組成(各種離子不重復)。
| 陽離子 | H+、NH4+、Mg2+、Ba2+、Al3+ |
| 陰離子 | OH-、Cl-、HCO3-、NO3-、SO42- |
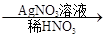 白色沉淀。請回答下列問題:
白色沉淀。請回答下列問題: 白色沉淀”有關反應的離子方程式____________________________。
白色沉淀”有關反應的離子方程式____________________________。| 實驗步驟 | 預期現象和結論 |
| 取適量C的溶液于試管中, ① 。 | 預期現象和結論1: ② ; 預期現象和結論2: ③ ; |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
鐵礦石是工業煉鐵的主要原料之一,其主要成分為鐵的氧化物(設雜質中不含鐵元素和氧元素,且雜質不與硫酸反應)。某研究性學習小組對某鐵礦石中鐵的氧化物的化學式進行探究。
Ⅰ.鐵礦石中含氧量的測定,以下實驗過程不完整,請補充完整。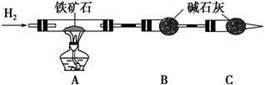
(1)按上圖組裝儀器,并______________________________________________;
(2)將8.0 g鐵礦石放入硬質玻璃管中,裝置B、C中的藥品如圖所示(夾持儀器均省略);
(3)從左端導氣管口處不斷地緩緩通入H2,____________________________,
點燃A處酒精燈;
(4)充分反應后,撤掉酒精燈,________________________________________;
(5)測得反應后裝置B增重2.25 g,則鐵礦石中氧的百分含量為________。
Ⅱ.鐵礦石中含鐵量的測定,流程如下。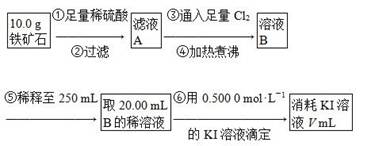
(1)步驟④中煮沸的作用是___________________________________________。
(2)步驟⑤中用到的玻璃儀器有燒杯、膠頭滴管、250 mL容量瓶、________。
(3)下列有關步驟⑥的操作中說法正確的是________。
a.因為碘水為黃色,所以滴定過程中不需加指示劑
b.錐形瓶不需要用待測液潤洗
c.滴定過程中可利用淀粉溶液作指示劑
d.滴定過程中,眼睛注視滴定管中液面變化
e.滴定結束后,30 s內溶液不恢復原來的顏色,再讀數
f.滴定結束后,滴定管尖嘴部分有氣泡,則測定結果偏大
(4)若滴定過程中消耗0.500 0 mol·L-1 KI溶液20.00 mL,則鐵礦石中鐵的百分含量為________。
Ⅲ.由Ⅰ、Ⅱ可以推算出該鐵礦石中鐵的氧化物的化學式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
Fridel—Crafts反應是向苯環上引入烷基最重要的方法,在合成上有很大的實用價值,該反應可以簡單表示如下:Ar+RX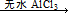 ArR+HX △H<0(Ar表示苯基)。某化學興趣小組在實驗室先利用叔丁醇(沸點90.70C)與鹽酸反應制得叔丁基氯(沸點500C),再利用Fridel—Crafts反應原理制備對叔丁基苯酚(熔點990C)。反應流程及實驗裝置如下圖所示:
ArR+HX △H<0(Ar表示苯基)。某化學興趣小組在實驗室先利用叔丁醇(沸點90.70C)與鹽酸反應制得叔丁基氯(沸點500C),再利用Fridel—Crafts反應原理制備對叔丁基苯酚(熔點990C)。反應流程及實驗裝置如下圖所示:
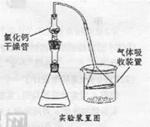
試回答下列問題:
(1)實驗裝置燒杯中漏斗的作用是________。
(2)巳知Fridel—Cxafts反應是放熱反應,為防止叔丁基氣的蒸氣被大量的HCl氣體帶走而影響產率,應將錐形瓶置于_______(填“冷水浴”或“熱水浴”)中。
(3)有機層中加入飽和氣化鈉溶液及飽和碳酸氫鈉溶液的作用可能是_______。通過 操作可將叔丁基氯粗產物轉化為較為純凈的叔丁基氯。
(4)某同學因去掉該制備裝置中的氣化鈣干燥管,發現產率很低(觀察不到對叔丁基苯酚白色固體)且錐形瓶中有大量的白霧,他推測是作催化劑的AlCl3發生強烈水解所致,該同學設計如下實驗方案進行驗證,請完成下表內容。
| 實驗方案 | 實驗現象 | 能否說明水解 |
| ①將錐形瓶中白霧通入HNO3酸化的AgNO3溶液 | | |
| ②將充分冒白霧后的液體抽濾,得不溶性固體,將固體分成兩份, 。 | 兩份固體均溶解 | |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某實驗小組用下列裝置進行乙醇催化氧化的實驗。
(1)實驗過程中銅網出現黑色和紅色交替的現象,請寫出相應的化學方程式 、 。在不斷鼓入空氣的情況下,熄滅酒精燈,反應仍能繼續進行,說明該乙醇催化反應是 反應。(填吸熱或放熱)
(2)甲和乙兩個水浴作用不相同.甲的作用是 ;乙的作用是 。
(3)反應進行一段時間后,試管a中收集到的主要有機生成物是 。(寫名稱)若要檢驗試管a中能收集的該物質,進行的操作為 。
(4)若試管a中收集到的液體用紫色石蕊試紙檢驗,試紙顯紅色,說明液體中還含有 。(寫結構簡式)
要除去該物質,可向混合液中加入 (填寫序號)。再通過 (填試驗操作名稱)即可除去。
| A.水 | B.苯 | C.碳酸氫鈉溶液 | D.四氯化碳 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
化學無處不在,下面說法正確的是
| A.“地溝油”禁止食用,但可用于制造生物柴油 |
B.“PM2.5”是指大氣中直徑小于或等于2.5 m(1 m(1 m=1×10-6m)的顆粒,“PM2.5”與空氣形成的分散系屬于膠體 m=1×10-6m)的顆粒,“PM2.5”與空氣形成的分散系屬于膠體 |
| C.紅寶石、水晶、玻璃、陶瓷等都是硅酸鹽制品 |
| D.分餾、裂化、裂解是利用化學變化來煉制加工石油的三種重要方法 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com