
【題目】關于阿佛加德羅常數(NA)的說法中錯誤的是( )
A. 等物質的量的CH4和H2O,核外電子總數均為10NA
B. 12克NaHSO4和MgSO4的固體混合物中含陽離子數為0.1NA
C. 反應2NH4ClO4![]() N2↑+Cl2↑+2O2↑+4H2O,每產生1molO2轉移電子數為7NA
N2↑+Cl2↑+2O2↑+4H2O,每產生1molO2轉移電子數為7NA
D. 100g質量分數為46%C2H5OH溶液中,含氫原子數為12NA
【答案】A
【解析】
A、甲烷和水的物質的量不明確,故等物質的量的兩者中含有的電子數相同,但不一定是10NA個,故A錯誤;
B、NaHSO4和MgSO4的摩爾質量均為120g/mol,12g混合物的物質的量為0.1mol,且兩者均由1個陽離子和1個陰離子構成,故0.1mol混合物中含有的陽離子為0.1NA個,故B正確;
C、反應2NH4ClO4![]() N2↑+Cl2↑+2O2↑+4H2O中,氯元素由+7價降為0價,故此反應轉移14mol電子,生成2mol氧氣,故當生成1mol氧氣時,反應轉移7NA個電子,故C正確;
N2↑+Cl2↑+2O2↑+4H2O中,氯元素由+7價降為0價,故此反應轉移14mol電子,生成2mol氧氣,故當生成1mol氧氣時,反應轉移7NA個電子,故C正確;
D、在乙醇溶液中,除了乙醇外,水也含氫原子,100g質量分數為46%的乙醇溶液中,乙醇的質量為46g,物質的量為1mol,含6NA個H原子;水的質量為54g,物質的量為3mol,含H原子為6NA個,故共含12NA個,故D正確。
故選:A。


科目:高中化學 來源: 題型:
【題目】已知草酸為二元弱酸:H2C2O4![]() HC2O4﹣+ H+ Ka1 ; HC2O4﹣
HC2O4﹣+ H+ Ka1 ; HC2O4﹣![]() C2O42﹣+H+ Ka2,T℃常溫下,向某濃度的草酸溶液中逐滴加入一定量濃度的KOH溶液,所得溶液中H2C2O4、HC2O4﹣、C2O42﹣三種,微粒的物質的量分數(δ)與溶液pH的關系如圖所示,則下列說法中不正確的是
C2O42﹣+H+ Ka2,T℃常溫下,向某濃度的草酸溶液中逐滴加入一定量濃度的KOH溶液,所得溶液中H2C2O4、HC2O4﹣、C2O42﹣三種,微粒的物質的量分數(δ)與溶液pH的關系如圖所示,則下列說法中不正確的是

A. T℃時,lgKa2=-4.2
B. pH=1.2溶液中:c(K+)+c(H+)=c(OH﹣)+c(H2C2O4)
C. pH=2.7溶液中:![]()
D. 向pH=1.2的溶液中再加KOH溶液,將pH增大至4.2的過程中水的電離度一直增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某酯W是一種療效明顯的血管擴張劑,一種合成流程如下:
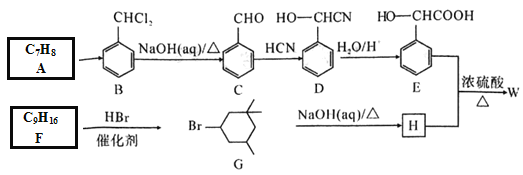
回答下列問題
(1)E中含碳官能團的名稱是_______;C的名稱是_____。
(2)A→B反應條件和試劑是___________;C→D的反應類型是___________。
(3)寫出W的結構簡式:___________。能測定H分子中所含化學鍵和官能團種類的儀器名稱是____________。
(4)寫出F→G的化學方程式:__________。
(5)R是E的同分異構體R同時具備下列條件的結構有______種
①遇氯化鐵溶液發生顯色反應; ②能發生水解反應和銀鏡反應,其中,在核磁共振氫譜上有5組峰且峰的面積比為1:1:2:2:2的結構簡式為___________。
(6)以乙醛為原料合成環酯 ,設計合成路線(其他試劑自選):______________。
,設計合成路線(其他試劑自選):______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,在容積為 10L 的密閉容器中,1molX 和 1molY 進行如下反應:2X(g)+Y(g)![]() Z(g) 經 60s 達到平衡,生成 0.3molZ,下列說法正確的是
Z(g) 經 60s 達到平衡,生成 0.3molZ,下列說法正確的是
A. 以 X 濃度變化表示的反應速率為 0.001mol/(L·s)
B. 將容器容積變為 20L,Z 的平衡濃度為原來的 1/2
C. 若增大壓強,則正反應速率增大,逆反應速率減小
D. 若升高溫度,X 的體積分數增大,則該反應的ΔH >0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關物質的轉化關系如下圖所示(部分物質與條件已略去)。已知A、B均為由相同的兩種元素組成的無色液體,C、E、G、I均為無色氣體,其中C為單質,E為最簡單的烴,G能使澄清石灰水變渾濁,I能使品紅褪色;D、E均由兩種元素組成,D的摩爾質量為144g·mol-1,H中兩種元素質量比為7∶8,F是白色膠狀沉淀,J是紅棕色固體。

(1)G的電子式為_____。
(2)H的化學式為_____。
(3)寫出反應①的化學方程式:______。
(4)寫出反應②的離子方程式:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯堿工業的原理改進方法如圖分兩個階段進行,下列說法中錯誤的是( )

A. 在階段I中,電源a為正極、b為負極
B. 階段Ⅱ陰極反應:Na0.44-xMnO2+xe-+xNa+=Na0.44MnO2
C. 比傳統氯堿工業減少了陽離子交換膜,避免氫氣和氯氣混合,便于NaOH提純
D. 階段Ⅰ,Ⅱ的反應不能都在飽和食鹽水的條件下進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在呼吸面具和潛水艇中可用過氧化鈉作為供氧劑,請選擇適當的化學試劑和實驗用品,用下圖中的實驗裝置進行實驗,證明過氧化鈉可作供氧劑。

(1)A是制取CO2的裝置.寫出A中發生反應的化學方程式___________________。
(2)填寫表中空格:
儀器 | 加入試劑 | 加入該試劑的目的 |
B | 飽和NaHCO3溶液 | 除去二氧化碳中的氯化氫 |
C | ____________ | ____________ |
D | NaOH溶液 | ____________ |
(3)寫出C中發生反應的化學方程式:___________________。
(4)試管F中收集滿氣體后,下一步實驗操作是把E中的導管移出水面,關閉分液漏斗活塞,用拇指堵住試管口,取出試管,立即把_____________________,則證明試管中收集的氣體是氧氣。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用惰性電極電解足量下列溶液一段時間后,再加入一定量括號內的純凈物,能使溶液恢復到原來的成分和濃度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨電極為惰性電極,溶液中陽離子在陰極放電,陰離子在陽極放電。A、電解AgNO3溶液,Ag+在陰極放電生成Ag,OH-在陽極放電生成O2,且n(Ag)∶n(O2)=2∶1,則應加入Ag2O恢復濃度,故A錯誤;B、電解NaOH溶液,H+在陰極放電生成H2,OH-在陽極放電生成O2,且n(H2)∶n(O2)=2∶1,則應加入一定量的H2O恢復原樣,故B錯誤;C、電解KCl溶液,H+在陰極放電生成H2,Cl-在陽極放電生成Cl2,且n(H2)∶n(Cl2)=1∶1,則應加入一定量HCl恢復原樣,故C錯誤;D、電解CuSO4溶液,Cu2+在陰極放電生成Cu,OH-在陽極放電生成O2,且n(Cu)∶n(O2)=2∶1,則應加入一定量CuO恢復原樣,故D正確。故選D。
點睛:分析電解反應的原理,在兩極析出什么物質(固體或氣體),相當于什么物質脫離反應體系,根據元素守恒和原子比例,加入對應的物質,即可使溶液完全復原。
【題型】單選題
【結束】
28
【題目】工業上用電解法處理含鎳酸性廢水并得到單質Ni的原理如圖所示。下列說法不正確的是

已知:①Ni2+在弱酸性溶液中發生水解
②氧化性:Ni2+(高濃度)>H+>Ni2+(低濃度)
A. 碳棒上發生的電極反應:4OH--4e-=O2↑+2H2O
B. 電解過程中,B中NaCl溶液的物質的量濃度將不斷減少
C. 為了提高Ni的產率,電解過程中需要控制廢水pH
D. 若將圖中陽離子膜去掉,將A、B兩室合并,則電解反應總方程式發生改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等離子的溶液中,逐滴加入5molL-1的氫氧化鈉溶液,所加氫氧化鈉溶液的體積(mL)與產生沉淀的物質的量(mol)關系如圖所示。下列敘述正確的是( )

A.x與y的差值為0.02mol
B.原溶液中c(Cl-)=0.75mol·L-1
C.原溶液的pH=1
D.原溶液中n(Mg2+)∶n(Al3+)=5∶2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com