
【題目】下列關于同分異構體數目的敘述不正確的是( )
A.甲苯苯環上的1個氫原子被含3個碳原子的烷基取代,所得產物有6種
B.已知丙烷的二氯代物有4種異構體,則其六氯代物的異構體數目也為4種
C.含有5個碳原子的某飽和鏈烴,其一氯代物有3種
D.菲的結構為 ,它與硝酸反應,可生成5種一硝基取代物
,它與硝酸反應,可生成5種一硝基取代物
 芝麻開花課程新體驗系列答案
芝麻開花課程新體驗系列答案科目:高中化學 來源: 題型:
【題目】環己烯是一種重要的化工原料。
(1)實驗室可由環己醇制備環己烯,反應的化學方程式是______________________________________________________。
(2)實驗裝置如下圖所示,將10 mL環己醇加入試管A中,再加入1 mL濃硫酸,搖勻后放入碎瓷片,緩慢加熱至反應完全,在試管C內得到環己烯粗品。

環己醇和環己烯的部分物理性質如下:
密度 | 熔點 | 沸點 | 溶解性 | |
環己醇 | 0.96 | 25 | 161 | 能溶于水 |
環己烯 | 0.81 | -103 | 83 | 難溶于水 |
① A中碎瓷片的作用是_____________;導管B除了導氣外還具有的作用是___________________。
② 試管A置于水浴中的目的是_________________________________;
試管C置于冰水浴中的目的是_______________________________。
(3)環己烯粗品中含有少量環己醇和酸性雜質。精制環己烯的方法是:
① 向環己烯粗品中加入_________(填入編號),充分振蕩后,___________________(填操作名稱)。
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
② 再對初步除雜后的環己烯進行蒸餾,得到環己烯精品。蒸餾時,蒸餾燒瓶中要加入少量生石灰,目的是__________________________。
③ 實驗制得的環己烯精品質量低于理論產量,可能的原因是_______________。
A.蒸餾時從70℃開始收集產品
B.環己醇實際用量多了
C.制備粗品時環己醇隨產品一起蒸出
(4)以下區分環己烯精品和粗品的方法,合理的是________________。
A.加入水觀察實驗現象
B.加入金屬鈉觀察實驗現象
C.加入酸性高錳酸鉀溶液,振蕩后觀察實驗現象
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗中,所選取的分離裝置與對應原理都正確的是 ( )

選項 | 目 的 | 裝置 | 原 理 |
A | 氫氧化鐵膠體的純化 | ① | 膠體粒子不能通過濾紙,離子及小分子可以通過濾紙 |
B | 分離苯中的溴苯 | ③ | 苯(0.88 g/mL)和溴苯(1.5 g/mL)的密度不同 |
C | 粗鹽提純 | ①② | NaCl在水中的溶解度很大 |
D | 除去環己醇中的環烯 | ④ | 環己醇的沸點(161 ℃)與環己烯的沸點(83 ℃)相差較大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生欲探究FeSO4溶液與濃HNO3的反應。
該同學向盛有FeSO4溶液的試管中滴入數滴濃硝酸,并振蕩試管,預期現象為試管中會立即產生紅棕色氣體,溶液焰色逐漸變黃。但實際操作時觀察到液面上方氣體變化紅棕色,且試管中溶液顏色變為深棕色。
為了進一步探究溶液變為深棕色的原因,該同學進行如下實驗。
回答下列問題
(1)向FeSO4溶液和反應后溶液中加入KSCN溶液,前者不變紅色,后者變紅,該現象的結論是________。
(2)該同學通過查閱資料,認為溶液的深棕色可能是NO2或NO與溶液中Fe2+或Fe3+發生反應而得到的。為此他利用如圖裝置(氣密性已檢驗,尾氣處理裝備略)進行探究。
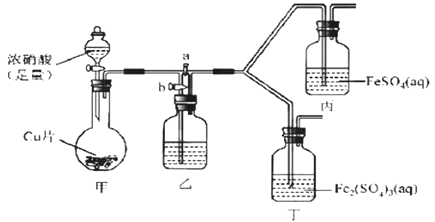
Ⅰ.打開活塞a、關閉b,并使甲裝置中反應開始后,觀察到丙中溶液逐漸變為深棕色,而丁中溶液無明顯變化。
Ⅱ.打開活塞b、關閉a,一段時間后再停止甲中反應。
Ⅲ.為與Ⅰ中實驗進行對照重新更換丙、丁后,使甲中反應重復進行步驟Ⅰ實驗,觀察到的現象與步驟Ⅰ中相同。
①銅與足量濃硝酸反應的離子方程式是_______________。
②裝置乙的試劑為____________________。
③步驟Ⅱ的目的是_______________________。
④該實驗可得出的結論是______________________。
(3)該同學重新進行FeSO4溶液與濃HNO3的反應的實驗,觀察到了預期現象,其實驗操作是_________,反應的離子方程式為___________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】蔗糖與濃硫酸的炭化實驗會產生大量的有刺激性氣味的氣體對環境產生污染。為此,某化學興趣小組設計了如下裝置進行實驗。玻璃管中①②③分別為CO檢測試紙 (浸有氯化鈀洛液的濾紙,遇CO變黑色)、滴有品紅溶液的濾紙、滴有酸性KMn04 溶液的濾紙,a和b分別為兩個小氣球。

實驗步驟如下:按圖示連接好儀器,然后檢查裝置的氣密性;裝好試劑,夾緊止水夾K,向A瓶中的蔗糖上小心滴加濃硫酸,片刻后可觀察到A瓶內蔗糖變黑,體積膨脹,有白霧產生,氣球a鼓起,玻璃管中①號濾紙白色變黑色,②號和③號濾紙均褪色。請回答以下問題:
(1)上圖中盛有濃硫酸的儀器名稱為________。待上述反應結束后,點燃酒精燈并在②號和③號濾紙的玻璃管近均勻加熱,觀察到的現象是_______。
(2)B瓶中酸性KMnO4溶液的作用是______________,發生反應的離子方程式為_____。
(3)打開止水夾K,使氣球a內氣體緩慢通過B瓶和C瓶,一段時間之后,發現澄清石灰水變渾濁,但此現象并不能證明該反應生成了CO2。為了證明有CO2生成并簡化實驗裝置,可在④號位置放上滴有______的濾紙(從以下試劑中選擇)。
A.品紅濃液 B.酸性高錳酸鉀溶液 C.溴水 D.澄清石灰水
(4)若反應生成的兩種碳的氧化物在相同條件下的體積比為2:1,則濾紙炭化后體積膨脹發生反應的化學方程式可能為_________。(若是氧化還原反應,請用單線橋法在化學反應方程式上標明電子轉移的方向和數目。)
(5)若在尾端沒有氣球b,會有什么不良結果?_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.高純度氫氧化鎂廣泛應用于醫藥、電力等領域。鎂硅酸鹽礦石可用于生產氫氧化鎂,簡要工藝流程如圖所示:

已知:
①溶液Ⅰ中除含Mg2+、SO42外,還含有少量Fe3+、Al3+、Fe2+等離子;
②常溫下,幾種金屬離子開始沉淀和沉淀完全時的pH如下表所示:
金屬離子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
開始沉淀時的pH | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全時的pH | 3.7 | 5.2 | 9.7 | 12.4 |
請回答下列問題:
(1)鎂在元素周期表中的位置_______________;
(2)向溶液Ⅱ中加入試劑X是_____________,作用是_________________________;
(3)流程中不加H2O2引起的后果是___________________________________;
(4)說出母液的一種用途___________________;
(5)加入H2O2溶液發生反應的離子方程式是___________________;
Ⅱ.海水中含有豐富的鎂資源。某同學設計了從模擬海水中制備MgO的實驗方案:

模擬海水中的離子濃度/ (mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某種離子的濃度小于1.0×10-5 mol/L,可認為該離子不存在;實驗過程中,假設溶液體積不變。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp [Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12。請回答下列問題:
(6)沉淀物X為_____________;
(7)濾液N中Ca2+濃度為_______________;
(8)加NaOH固體調整pH=12.5是否可行______(填“是”“否”);原因是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com