
【題目】與12.8g SO2所含有原子數相等的NO的質量為
A. 3.0g B. 6.0g C.9.0g D.18.0g
 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:高中化學 來源: 題型:
【題目】某研究性學習小組設計了一組實驗來探究元素周期律。甲同學根據元素非金屬性與對應最高價含氧酸之間的關系,設計了如圖裝置來一次性完成碳族元素中C與Si的非金屬性強弱比較的實驗研究;乙同學設計了如圖裝置來驗證鹵族元素性質的遞變規律。

據如圖回答:
(1)甲同學設計實驗的依據是____________________________________。
(2)寫出選用的化學試劑:B____________,其作用為___________。
(3)C中反應的離子方程式為____________________________________________。
據如圖回答:
乙同學的實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ.當B中溶液由黃色變為棕紅色時,關閉活塞a。
Ⅳ.打開活塞b,將少量C中溶液滴入D中,關閉活塞b,取下D振蕩,靜置后CCl4層溶液變為紫紅色。
(4)寫出B處反應的離子方程式 ___________________________________________。
(5)A中驗證氯氣的氧化性強于碘的實驗現象是_____________________。
(6)過程Ⅲ實驗的目的是_________________________。
(7)綜合甲、乙兩同學的實驗得出的結論是:同主族元素從上到下元素的非金屬逐漸減弱,其原因是___________________________________________(試從原子結構角度解釋)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制下列溶液時常需加入少量括號內的物質,其中不是為了抑制離子水解的是
A.NaAlO2(NaOH) B.SnCl2(HCl)
C.FeCl3(HCl) D.FeSO4(Fe)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分析下列表格中烴的排列規律,判斷排列在第15位烴的分子式是
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | … |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | … |
A. C6H12 B. C6H14 C. C7H12 D. C7H14
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】尿黑酸是由酪氨酸在人體內非正常代謝而產生的一種物質。其轉化過程如下:
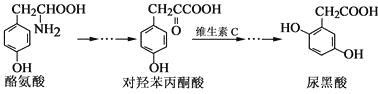
下列說法錯誤的是( )
A. 酪氨酸既能與鹽酸反應,又能與氫氧化鈉反應
B. 1 mol尿黑酸與足量濃溴水反應,最多消耗3 mol Br2
C. 對羥基苯丙酮酸分子中在同一平面上的碳原子至少有7個
D. 1 mol尿黑酸與足量NaHCO3反應,最多消耗3 mol NaHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列鹵代烴在KOH醇溶液中加熱不反應的是( )
① ![]() ② (CH3)2CHCH2Cl ③ (CH3)3CCH2Cl ④ CHCl2-CHBr2 ⑤
② (CH3)2CHCH2Cl ③ (CH3)3CCH2Cl ④ CHCl2-CHBr2 ⑤ ![]() ⑥ CH2Cl2
⑥ CH2Cl2
A.①③⑥ B.②③⑤ C.全部 D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A. 稀鹽酸可除去燒瓶內殘留的MnO2 B. 可用磨口玻璃瓶保存NaOH溶液
C. 稀硝酸可除去試管內壁的銀鏡 D. 煮沸自來水可除去其中的CaCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用太陽能熱化學硫碘循環分解水制氫反應過程如下圖所示:
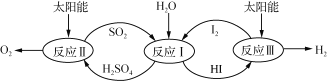
(1) 反應Ⅱ中涉及的熱化學方程式為:
①H2SO4(l)=SO3(g)+H2O(g) ΔH=+177.3 kJ·mol-1
②2SO3(g) = 2SO2(g)+O2(g) ΔH=a kJ·mol-1
③2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) ΔH=+550.2 kJ·mol-1則 a= ;
(2)反應Ⅰ得到的產物可用I2進行分離。該產物的溶液在過量I2的存在下會分成兩層 :含低濃度I2的H2SO4溶液層和高濃度的I2的HI溶液層。
①區分兩層溶液可加入的試劑為 (填化學式)。
②下列說法正確的是 (填序號)。
A. SO2在反應Ⅰ中作氧化劑
B. 加過量I2前,H2SO4溶液和HI不互溶
C. 兩層溶液的密度存在差異
D. I2在HI溶液中比在H2SO4溶液中易溶
(3)用氧缺位鐵酸銅(CuFe2O4-x)作催化劑,利用太陽能熱化學循環分解H2O也可制H2,其物質轉化如右圖所示。
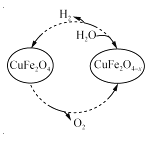
①氧缺位鐵酸銅(CuFe2O4-x)與水反應的化學方程式為 。
②若x=0.15,則1 mol CuFe2O4參與該循環過程理論上一次能制得標準狀況下的H2體積為 L。
③CuFe2O4可用電化學方法得到,其原理如圖所示,則陽極的電極反應式為 。
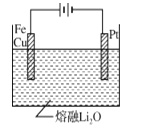
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】安徽古代科學家方以智在其《物理小識》卷七《金石類》中指出:有硇水者,剪銀塊投之,則旋而為水。其中的“硇水”指 ( )
A. 硝酸 B. 硫酸 C. 鹽酸 D. 醋酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com