
【題目】下列對化學反應的認識正確的是
A. 化學反應過程中,分子的種類和數目一定發生改變
B. 吸熱反應有的不加熱也能發生,放熱反應都不需要加熱就能發生
C. 熵值增大的反應都是混亂度增大的反應,焓變和熵變都小于0的反應肯定是自發的
D. 反應物的總焓小于生成物的總焓時,ΔH>0
【答案】D
【解析】
A.化學反應前后分子種類發生變化,但數目不一定變化;
B. 有的吸熱反應不加熱也會發生,有的放熱的化學反應需要加熱才能發生;
C. 反應自發進行的判斷根據是:ΔH-T![]() S<0;
S<0;
D. 反應焓變△H=H(生成物)-H(反應物),當反應物的總焓小于生成物的總焓時,△H>0。
A.化學反應前后分子種類發生變化,但數目不一定變化,如前后分子數不變的化學反應,故A錯誤;
B. 有的吸熱反應不加熱也會發生,如氯化銨和氫氧化鋇晶體的反應,有的放熱的化學反應需要加熱才能發生,如鋁熱反應,故B錯誤;
C. 反應自發進行的判斷根據是:ΔH-T![]() S<0,ΔH和
S<0,ΔH和![]() S均小于0,ΔH-T
S均小于0,ΔH-T![]() S的正負取決于溫度,高溫下可能不能自發進行,故C錯誤;
S的正負取決于溫度,高溫下可能不能自發進行,故C錯誤;
D. 根據公式△H=H(生成物)-H(反應物),生成物的總焓小于反應物總焓,故D正確。
所以D選項是正確的。


科目:高中化學 來源: 題型:
【題目】某烷烴相對分子質量為86,若該分子中僅含有3個甲基(—CH3),則其一氯取代物最多有( )種(不考慮立體異構)
A. 7 B. 8 C. 9 D. 10
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化鐵和高鐵酸鉀都是常見的水處理劑。某興趣小組以鐵屑為原料模擬工業上制備氯化鐵及進一步氧化制備高鐵酸鉀的流程如下:

請回答下列問題:
(1)“氧化”階段通入過量空氣比用氯氣作氧化劑具有的優點是__________________________________。
(2)“合成”階段生成Na2FeO4的離子方程式為__________________________________。
(3)為了檢驗“氧化”過程中所得FeCl3溶液中是否含有Fe2+,某同學取少量溶液于試管中,選用下列試劑可以達到目的的是_______(填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若選用酸性K MnO4溶液進行檢驗,請分析方案是否合理,并說明理由:_____________________________。
(4)過程①制取FeCl3固體的具體操作步驟是_____________________________________________________。若使6.4mol/LFeCl3飽和溶液不析出Fe(OH)3,需控制溶液的pH小于_______{已知該實驗條件下,Ksp[(Fe(OH)3]=8.5×10-36,Kw=1.1×10-13,1.13≈1.33}
(5)在不同溫度和不同pH下,FeO42-的穩定性如下圖所示:

從上圖分析,為了提高“合成”階段Na2FeO4的產率,可采取的實驗條件范圍為______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨基甲酸銨(H2 NCOONH4)是一種白色晶體,是常見的實驗藥品,可由干燥的NH3和干燥的CO2在任何比例下反應得到每生成1.0g氨基甲酸銨放出2.05kJ的熱量。回答下列問題:
(1)實驗室可選用下列裝置(I~V)制備干燥的NH3和CO2。
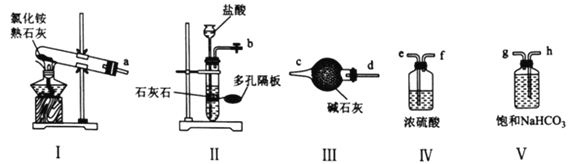
①用裝置I、Ⅲ制備并純化NH3時,接口a與________________(填接口字母)相連,裝置I中發生反應的化學方程式為________________________。
②制備并純化CO2時,按氣流從左至右的方向,各接口連接順序為________________(填接口字母)
(2)一種制備氨基甲酸銨的改進實驗裝置如下圖所示:
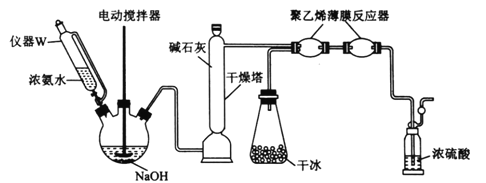
①用儀器W代替分液漏斗的優點是________________________;用干冰裝置代替(1)中制備并純化CO2裝置的優點是________________________。
②“薄膜反應器”中發生反應的熱化學方程式為________________________;盛濃硫酸的裝置的作用是________________________________(列舉2點)。
③體系中若有水蒸氣,還可能生成的銨鹽是________________________(填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用系統命法寫出下列物質名稱或結構簡式
(1) __________
__________
(2) ____________
____________
(3)![]() ___________
___________
(4)![]() ____________
____________
(5)2,6-二甲基-4-乙基辛烷_______
(6)2-甲基-1-戊烯____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電動自行車由于靈活、快捷、方便,已成為上班族的主要代步工具,其電源常采用鉛蓄電池。反應原理:Pb(s)+PbO2(s)+2H2SO4(aq) ![]() 2PbSO4(s)+2H2O(l)。根據此反應判斷下列敘述錯誤的是( )
2PbSO4(s)+2H2O(l)。根據此反應判斷下列敘述錯誤的是( )
A. 放電時負極反應:Pb(s)+SO42-(aq)-2e- = PbSO4(s)B. 放電時化學能轉化為電能
C. 放電時,電解液的密度增大D. 放電時,正負極質量都增加
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向濃度均為0.1mol·L-1、體積均為100mL的兩種一元酸HX、HY溶液中,分別加入NaOH的稀溶液,lg[c(H+)/c(OH-)]隨加入NaOH的物質的量的變化如圖所示。下列說法正確的是( )

A. a點溶液的pH=2
B. c點溶液中:c(Yˉ)>c(Na+)>c(HY)>c(H+)>c(OHˉ)
C. b點溶液中:c(Yˉ)+c(HY)=c(Na+)
D. 水的電離程度:a<b<c
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列熱化學方程式:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= —24.8 kJ·mol-1;3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ·mol-1 ;Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +19.4kJ·mol-1則14g CO氣體與足量FeO充分反應得到Fe單質和CO2氣體時的釋放或吸收的熱量為
A. 放出11 kJ B. 放出5.5kJ C. 吸收11 kJ D. 吸收5.5 kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.CO2溶于水得到的溶液能導電,則CO2屬于電解質
B.電離需要通電才能進行
C.氯化氫的水溶液能導電,液態氯化氫不能導電
D.NaCl晶體不能導電,所以NaCl是非電解質
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com