
【題目】按要求完成下面每一小題:
(1)下列各物質中,互為同位素的是________,互為同素異形體的是________,互為同系物的是________,互為同分異構體的是________。
①金剛石與石墨 ②12C與14C ③乙酸和甲酸甲酯
④  與
與  ⑤
⑤  與
與 ![]()
⑥  與
與 ![]() ⑦CH3﹣CH3和
⑦CH3﹣CH3和 ![]()
(2)已知TiCl4在通常情況下是無色液體,熔點為﹣37℃,沸點為136℃,可知TiCl4為________晶體。
(3)相對分子質量為72的烷烴,它的一氯代物只有一種,此烷烴的結構簡式為____________________。
(4)寫出在光照條件下,甲烷與氯氣發生反應生成氣態有機物的化學方程式:_________________。
【答案】 ② ① ⑦ ③⑥ 分子 C(CH3)4 CH4+Cl2 ![]() CH3Cl+HCl
CH3Cl+HCl
【解析】(1)①金剛石和石墨為碳元素的不同單質,為同素異形體;
②12C與14C的質子數相同,而中子數不同,二原子互為同位素;
③乙酸和甲酸甲酯的分子式相同,結構不同,互為同分異構體;
④ 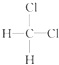 與
與 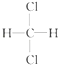 為同種物質;
為同種物質;
⑤ 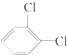 與
與 ![]() 為同種物質;
為同種物質;
⑥ 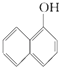 與
與 ![]() 的分子式相同,結構不同,互為同分異構體;
的分子式相同,結構不同,互為同分異構體;
⑦CH3﹣CH3和 ![]() 結構相似,組成相差n個CH2原子團的有機物,互為同系物;
結構相似,組成相差n個CH2原子團的有機物,互為同系物;
故互為同位素的是②,互為同素異形體的是①,互為同系物的是⑦,互為同分異構體的是③⑥;
(2)TiCl4是共價型化合物,熔沸點較低,應為分子晶體;
(3)相對分子質量為72的烷烴分子式為C5H12,它的一氯代物只有一種,此烷烴的結構簡式為C(CH3)4;
(4)CH3Cl常溫下是氣體,則在光照條件下,甲烷與氯氣發生反應生成氣態有機物的化學方程式為CH4+Cl2 ![]() CH3Cl+HCl。
CH3Cl+HCl。


 優等生題庫系列答案
優等生題庫系列答案科目:高中化學 來源: 題型:
【題目】寫出下列反應的熱化學方程式:
(1)46克NO2(g)與H2O (1)充分反應生成HNO3(aq)和NO(g),放熱46kJ。__________;
(2)用 CO 還原1molFe2O3,放熱24.8kJ。___________;
(3)1molHgO(s)分解為液態汞和氧氣,吸熱90.7kJ。___________;
(4)根據最新“人工固氮”的研究報道,在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生下列反應,
已知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ·mol-l,
2NH3(g) △H=-92.4kJ·mol-l,
2H2(g)+O2(g)=2H2O (1) △H=-571.6kJ·mol-l,
則 2N2(g)+6H2O(1)![]() 4NH3(g)+3O2(g)△H= ___________。
4NH3(g)+3O2(g)△H= ___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面關于硅的敘述中,正確的是
A. 硅是親氧元素,在自然界中以化合態存在
B. 硅是構成礦物和巖石的主要元素,硅在地殼中的含量在所有元素中居第一位
C. 硅的活潑性比碳強,只有在高溫下才能跟氫氣起化合反應
D. 二氧化硅在電子工業中,是重要的半導體材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關含硅物質的說法正確的是
A. 二氧化碳通入水玻璃可以制得硅酸 B. 二氧化硅可以用作太陽能光電池板
C. 高純度的硅單質廣泛用于制作光導纖維 D. 二氧化硅是酸性氧化物,它不溶于任何酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬晶體的堆積密度大,原子配位數高,能充分利用空間的原因是( )
A. 金屬原子的價電子數少
B. 金屬晶體中有自由電子
C. 金屬原子的原子半徑大
D. 金屬鍵沒有飽和性和方向性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】全世界每年鋼鐵因銹蝕造成大量的損失。某城市擬用如圖方法保護埋在酸性土壤中的鋼質管道,使其免受腐蝕。關于此方法,下列說法不正確的是( )

A.土壤中的鋼鐵易被腐蝕是因為在潮濕的土壤中形成了原電池
B.金屬棒M的材料應該是比鎂活潑的金屬
C.金屬棒M上發生反應:M-ne-=Mn+
D.這種方法稱為犧牲陽極的陰極保護法
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com