
【題目】下列氣體可以用排水集氣法收集的是
A. HCl B. SO2 C. NO D. NO2
 紅果子三級測試卷系列答案
紅果子三級測試卷系列答案 課堂練加測系列答案
課堂練加測系列答案 輕松課堂單元測試AB卷系列答案
輕松課堂單元測試AB卷系列答案科目:高中化學 來源: 題型:
【題目】2A(g) ![]() 2B(g) + C(g) △H < 0 ,現欲使正反應速率減小,C的濃度增大,可行的措施是(其它條件不變)( )
2B(g) + C(g) △H < 0 ,現欲使正反應速率減小,C的濃度增大,可行的措施是(其它條件不變)( )
A.加壓 B.減壓 C.減少C的濃度 D.降溫
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中,給一氧化碳和水蒸氣的氣體混合物加熱,在催化劑存在下發生反應:CO(g)+H2O(g)![]() H2(g)+CO2(g)。在500 ℃時,平衡常數K=9。若反應開始時,一氧化碳和水蒸氣的濃度都是0.02 mol/L,則在此條件下CO的轉化率為( )
H2(g)+CO2(g)。在500 ℃時,平衡常數K=9。若反應開始時,一氧化碳和水蒸氣的濃度都是0.02 mol/L,則在此條件下CO的轉化率為( )
A. 25% B. 50% C. 75% D. 80%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. SO2的漂白原理與次氯酸相同
B. 煤的干餾可得到石油氣、汽油、煤油、柴油等
C. 從海水中提取所有物質都必須通過化學反應才能實現
D. 純堿可用于生產普通玻璃,日常生活中也可用純堿溶液來除去物品表面的油污
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家用氮化鎵材料與銅組裝成如圖所示的人工光合系統,利用該裝置成功地實現了以CO2和H2O合成CH4。下列關于該電池敘述錯誤的是( )
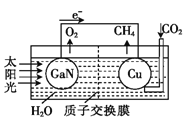
A.電池工作時,是將太陽能轉化為電能
B. 銅電極為正極,電極反應式為:CO2+8e-+8H+=CH4+2H2O
C.電池內部H+透過質子交換膜從左向右移動
D.為提高該人工光合系統的工作效率,可向裝置中加入少量硝酸溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ、氮肥的使用在提高糧食產量的同時,也導致了土壤、水體污染等環境問題。
(1)長期過量使用銨態化肥NH4Cl,易導致土壤酸化,請用化學用語解釋原因
(2)工業上處理氨氮廢水的方法是采用電解法將NO3-轉化為N2,如圖所示


B極的電極反應方程式是_________________________
(3)除去60L廢水中的62 mg NO3-后, 廢水的pH= 。
Ⅱ、如下圖所示C、D、E、F、X、Y都是惰性電極。將電源接通后,向(乙)中滴入酚酞溶液,在 F極附近顯紅色。
(1)若用甲醇、空氣燃料電池作電源,電解質為KOH溶液,則A極的電極反應式為 。
(2)欲用(丙)裝置給銅鍍銀,銀應該是 電極(填G或H)。
(3)(丁)裝置中Y極附近紅褐色變 (填深或淺)。
(4)通電一段時間后,C、D、E、F電極均有單質生成,其物質的量之比為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】黑火藥是由硫黃粉、硝酸鉀和木炭按一定比例混合而成的,爆炸時的反應是:S+2KNO3+3C=K2S+N2↑+3CO2↑,該反應的還原劑是( )
A.C
B.C和S
C.KNO3
D.S和KNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某廢催化劑含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同學用15.0 g該廢催化劑為原料,回收鋅和銅。采用的實驗方案如下:
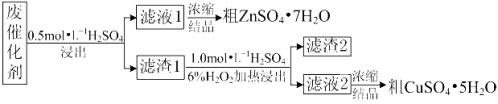
已知:① ZnS與稀硫酸反應時,化合價不變;
② CuS既不溶解于稀硫酸,也不與稀硫酸反應。
回答下列問題:
(1)在下列裝置中,第一次浸出必須用________________,第二次浸出應選用______________。(填標號)。第二次浸出時,加熱溫度不宜過高的原因是 。

(2)濾液1中含有Fe2+,請根據提供的試劑進行檢驗,則檢驗方法為: 。
(提供的試劑:稀鹽酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水)
(3)將濾液1、濾液2蒸發濃縮至 時,停止加熱,然后冷卻結晶得到相應的粗產品。
(4)若濾渣2中含有淡黃色固體,寫出第二次浸出的化學反應方程式: 。
(5)某同學在實驗完成之后,得到1.50 g CuSO4·5H2O,則銅的回收率為___________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com