
【題目】某同學設計如下實驗方案以分離KCl和BaCl2兩種固體混合物,供選試劑:Na2SO4溶液、K2CO3溶液、K2SO4溶液、硫酸、鹽酸

(1)操作①的名稱是 ,操作②的名稱是 。
(2)試劑a是 ,試劑b是 (填化學式)。
(3)加入試劑b所發生反應的離子方程式為 。
(4)該方案能否達到實驗目的(填能或不能) .若不能,應如何改進(若能,此問不用回答) 。
(5)若要測定原混合物中BaCl2的質量分數,除了要準確稱量混合物的質量外,至少還要獲得的數據是 。
A.固體C的質量 | B.沉淀A的質量 |
C.沉淀A1的質量(未干燥) | D.固體B的質量 |
【答案】(1)溶解(1分)過濾(1分)
(2)K2CO3(1分)HCl(1分)
(3)BaCO3+2H+=Ba2++CO2↑+H2O
(4)不能應在操作②的濾液中加入過量鹽酸后再蒸發結晶(2分)(5)D(2分)
【解析】試題分析:混合物溶于水制成溶液,要實現氯化鉀和氯化鋇的分離,需要把氯化鋇轉化為碳酸鋇,然后碳酸鋇與鹽酸反應轉化為氯化鋇,所以試劑a是碳酸鉀,產生的碳酸鋇沉淀通過過濾除去,濾液加入鹽酸后,蒸發、結晶即得到氯化鉀。沉淀與鹽酸反應生成氯化鋇,蒸發結晶得到氯化鋇。
(1)根據以上分析可知操作①的名稱是溶解,操作②的名稱是過濾,(2)試劑a是K2CO3。試劑b是鹽酸,(3)加入試劑b所發生反應的化學方程式為BaCO3+2HCl=BaCl2+CO2↑+H2O。(4)操作②的濾液中含有剩余的氯化鉀及K2CO3溶液、若要直接蒸發結晶得到的氯化鉀不純,必須除去碳酸鉀,需要加入足量的鹽酸;答案不能, 應在操作②的濾液中加入過量鹽酸后再蒸發結晶;(5)準確稱量KCl和BaCl2兩種固體混合物的質量,還應當直到硫酸鋇沉淀的質量,就能求出BaCl2質量,進而求出其質量分數;


科目:高中化學 來源: 題型:
【題目】可逆反應:2NO2 ![]() 2NO+O2在定容密閉容器中反應,達到平衡狀態的標志是( )
2NO+O2在定容密閉容器中反應,達到平衡狀態的標志是( )
①單位時間內生成n mol O2的同時生成2 nmolNO2
②單位時間內生成n mol O2的同時生成2 nmolNO
③用NO2、NO 、O2的物質的量濃度變化表示的反應速率之比為2:2:1的狀態
④混合氣體的顏色不再改變的狀態
⑤混合氣體的密度不再改變的狀態
⑥混合氣體的壓強不再改變的狀態
⑦混合氣體的平均相對分子質量不再改變的狀態
⑧NO2 、NO、O2的分子數之比為2:2:1的狀態
A.①③④⑦ B. ②③⑤⑦ C. ①④⑥⑦ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從根本上說,生物體都是由非生物界中的化學元素構成的,生物界和非生物界是統一的。生物界和非生物界的差異性表現在
A. 構成生物體的化學元素具有特異功能
B. 生物體中有個別的化學元素在非生物界中沒有
C. 組成生物體的化學元素在生物體內和在無機自然界中的元素種類相差很大
D. 組成生物體的化學元素在生物體內和在無機自然界中的元素含量相差很大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上以黃銅礦(主要成分CuFeS2)為原料制備CuS04.5H2O的主要流程如下:

(1)下列裝置不能用于吸收氣體X的是 。(填代號)。
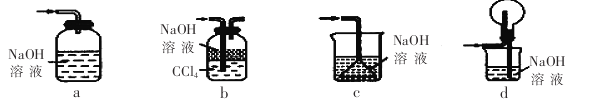
(2)熔渣Y的成分為Fe203和Fe0,選用提供的試劑,設計實驗驗證熔渣中含有FeO。
提供的試劑:稀鹽酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。
①從上述提供的試劑中選擇實驗驗證所需藥品 。
②寫出驗證過程中所發生的氧化還原反應的離子方程式 。
(3)向粗銅中加入硫酸和硝酸的混酸溶液制取硫酸銅時(雜質不參加反應),混酸中HNO3與H2S04的最佳物質的量之比為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數,下列敘述正確的是
A.標準狀況下,22.4LH2O含有的分子數為NA
B.常溫常壓下,1.06gNa2CO3含有的Na+離子數為0.02NA
C.通常狀況下,NA個CO2分子占有的體積為22.4L
D.物質的量濃度為0.5mol/L的MgCl2溶液中,含有Cl-個數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】C、H、N三種化學元素在組成人體的化學成分中,質量分數共占74%左右,而這三種元素在巖石圈中,其質量分數不到1%。這個事實說明
A. 生物界與非生物界的統一性 B. 生物界與非生物界的差異性
C. 元素在無機自然界中都可找到 D. 生物界的特殊性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羰基硫(COS)可作為一種糧食熏蒸劑,能防止某些昆蟲、線蟲和真菌的危害。在恒容密閉容器中,將CO和H2S混合加熱并達到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反應前CO物質的量為10mol,平衡后CO物質的量為8mol。下列說法正確的是
A.升高溫度,H2S濃度增加,表明該反應是吸熱反應
B.通入CO后,正反應速率逐漸增大
C.反應前H2S物質的量為7mol
D.CO的平衡轉化率為80%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
A. 磷脂和核苷酸的組成元素不同,磷脂中含有P,而核苷酸中含有N
B. 糖類俗稱“碳水化合物”,組成糖類的化學元素都是C、H、O
C. 下列物質中,葡萄糖、麥芽糖、核酸都屬于以碳鏈為骨架的生物大分子
D. 碳元素是組成生物體的最基本元素,這是因為碳元素在生物體中含量最多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖表示反應A(g)+B(g)![]() n C(g);(正反應為放熱反應),在不同條件下反應混合物中C的百分含量和反應過程所需時間的關系曲線。下列有關敘述正確的是( )
n C(g);(正反應為放熱反應),在不同條件下反應混合物中C的百分含量和反應過程所需時間的關系曲線。下列有關敘述正確的是( )

A. 反應由逆反應開始
B. a表示有催化劑,b表示無催化劑
C. 若n=2,其它條件相同,a比b的壓強大
D. 若其它條件相同,a比b的溫度高
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com