
【題目】下列物質中,屬于電解質的是( )
A.氯化鈉溶液
B.二氧化碳
C.氫氧化鈉固體
D.鐵
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下圖所示與對應敘述相符的是

A. 圖甲表示一定溫度下FeS和CuS的沉淀溶解平衡曲線,則Ksp(FeS)>Ksp(CuS)
B. 圖乙表示pH=2的甲酸與乙酸溶液稀釋時的pH變化曲線,則酸性:甲酸<乙酸
C. 圖丙表示用0.1000 mol·L-lNaOH溶液滴定25.00 mL鹽酸的滴定曲線,則 c(HCl)=0.0800 mol ·L-1
D. 圖丁表示反應N2(g)+3H2(g) ![]() 2NH3(g)平衡時NH3體積分數隨起始n(N2)/n(H2)變化的曲線,則轉化率:αA(H2)=αB(H2)
2NH3(g)平衡時NH3體積分數隨起始n(N2)/n(H2)變化的曲線,則轉化率:αA(H2)=αB(H2)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 將一小塊銅片放入盛有濃硫酸的試管中加熱反應后的溶液呈藍色
B. 將一小塊鈉放入盛有水的燒杯中,鈉在水面上游動,同時看到燒杯內的溶液變為紅色
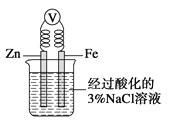
C. 如圖,一段時間后給燒杯內的溶液中加入氫氧化鈉溶液,可看到Fe電極附近有紅褐色沉淀生成
D. 向盛有少量Mg(OH)2沉淀懸濁液的試管中滴加氯化銨溶液,可看到沉淀溶解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列物質中,只存在離子鍵的是______,屬于共價化合物的是____,不存在化學鍵的是____。
①Ar ②CO2 ③Na2O2 ④H2SO4 ⑤NaCl ⑥NH4Cl ⑦CaO
(2)陰離子Xn﹣含N個中子,X的質量數為A,則ag X的氫化物中含質子的物質的量為_________mol。
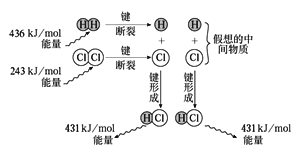
(3)觀察如圖,計算1molH2與1molCl2反應釋放的能量為______。若氫氣在氯氣中燃燒,反應過程中產生蒼白色的火焰,該反應中形成2 mol HCl時釋放的能量與上述計算的數值相比_______(填“大”或“小”或“相等”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F六種元素均位于周期表的前四周期,且原子序數依次增大。元素A是原子半徑最小的元素;B元素基態原子的核外電子分占四個原子軌道(能級);D元素原子的已成對電子總數是未成對電子總數的3倍;E與D處于同一主族;F位于ds區,且原子的最外層只有1個電子。
(1)E+離子的電子排布式是 。
(2)B、C、D元素的第一電離能由大到小的順序是 。
(3)B、C元素的某些氫化物的分子中均含有18個電子,則B的這種氫化物的化學式是 ;B、C的這些氫化物的沸點相差較大的主要原因是 。
(4)A、B、D可形成分子式為A2BD的某化合物,則該化合物分子中B原子的軌道雜化類型是 ;1 mol該分子中含有π鍵的數目是 。

(5)C、F兩元素形成的某化合物的晶胞結構如圖所示,則該化合物的化學式是 ,C原子的配位數是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應4A(s)+3B(g)===2C(g)+D(g),經2 min,B的濃度減少0.6 mol·L-1。下列說法正確的是( )
A.用A表示的反應速率是0.4 mol·L-1·min-1
B.分別用B、C、D表示反應的速率,其比值是3∶2∶1
C.在2 min末的反應速率,用B表示是0.3 mol·L-1·min-1
D.在這2 min內B和C兩物質濃度都是逐漸減小的
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通過以下途徑可以合成具有導電性的高分子材料F:

已知:

(1)物質C所含官能團的名稱為____________,試劑X的結構簡式是___________。
(2)條件Y是________________
(3)請寫出反應②的化學方程式:__________________
(4)C與H2以1:2反應所得產物的系統命名是________________
(5)反應⑥的化學反應類型為________,反應⑤的化學方程式_____________。
(6)反應①常用飽和食鹽水代替H2O,其目的是_________________
(7)寫出符合下列條件在B的所有同分異構體_______________。
①能與銀氨溶液反應 ②核磁共振氫譜有3個吸收峰
(8)參照上述合成信息,以丙炔、甲醛和乙酸為原料(無機試劑任選)設計路線合成乙酸—2-炔-1-丁酯
 _________________。
_________________。
合成路線示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com