
【題目】下列離子方程式中正確的是( )
A.Cu溶于稀HNO3:Cu+2 H++NO![]() ===Cu2++NO2↑+H2O
===Cu2++NO2↑+H2O
B.用石墨電極電解飽和食鹽水:2 Cl-+2 H2O ![]() 2 OH-+H2↑+Cl2↑
2 OH-+H2↑+Cl2↑
C.(NH4)2Fe(SO4)2溶液與過量NaOH溶液反應制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
D.向Fe(NO3)3溶液中加入過量的HI溶液:2 Fe3++2 I-===2 Fe2++I2
【答案】B
【解析】
試題分析:A、違反事實,或者漏了NO2與水的反應,正確的是3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O,A錯誤;B、用石墨電極電解飽和食鹽水的實質是溶質和溶劑同時反應生成堿放出氫氣和氯氣的過程,將易溶且完全電離的化合物拆寫、刪去未反應的鈉離子可得:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑,B正確;C、漏寫銨根與氫氧根的反應,正確的是2NH4+ + Fe2+ + 4OH- = Fe(OH)2↓ + 2NH3↑ + H2O,C錯誤;D、漏寫了Fe2+被硝酸氧化的反應,正確的是12H++3NO3-+Fe3++10I-═Fe2++3NO↑+6H2O+5I2,D錯誤;答案選B。
2OH-+H2↑+Cl2↑,B正確;C、漏寫銨根與氫氧根的反應,正確的是2NH4+ + Fe2+ + 4OH- = Fe(OH)2↓ + 2NH3↑ + H2O,C錯誤;D、漏寫了Fe2+被硝酸氧化的反應,正確的是12H++3NO3-+Fe3++10I-═Fe2++3NO↑+6H2O+5I2,D錯誤;答案選B。


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:
【題目】50g物質的量濃度為C1的濃H2SO4,質量分數為W1,與體積為V的水混合后得到物質的量濃度為C2的稀H2SO4,質量分數為W2(以下填“>”“<”或“=”)
(1)若W1=2W2,則C1_________2C2,V_________50mL.
(2)若C1=2C2,則W1_________2W2,V_________50mL.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國“蛟龍”號載人潛水器進行第五次下潛試驗,最大深度達到7062米,并安全返回。其動力電源是Al-AgO電池,原理如圖所示。下列說法中正確的是

A.Al電極是該電池的正極
B.Ag在AgO/Ag電極上發生氧化反應
C.該電池負極反應是2Al-6e-+8OH-=2AlO2-+4H2O
D.AgO/Ag電極附近溶液中的pH減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生活中的某些問題常常涉及化學知識,下列敘述錯誤的是
A. 純堿可用于制造玻璃,也可用于除去物品表面的油污
B. 用聚氯乙烯代替木材生產包裝盒、快餐盒等,以減少木材的使用
C. 黃河人海口沙洲的形成和鹵水點豆腐,都體現了膠體聚沉的性質
D. “煤改氣”、“煤改電”等燃料改造工程有利于減少環境污染
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作.不正確的是
A. 給試管、燒杯、蒸發皿和燒瓶加熱時都要墊上石棉網
B. 酒精燈內盛酒精不得超過容積的![]()
C. 往試管里裝粉末狀藥品.可以用紙槽
D. 酒精燈不慎碰翻著火,應立即用濕布蓋滅
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,將aLHCl(氣)溶于1L水中(水的密度為1gcm﹣3),得到的鹽酸的密度為bgmL﹣1,質量分數為w,物質的量濃度為cmolL﹣1則下列關系式中不正確的是
A.w=![]()
B.w=![]()
C.C=![]()
D.b=![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一個不傳熱的固定容積的密閉容器中,發生可逆反應mA(g)+nB(g)![]() pC(g)+qD(g),當m、n、p、q為任意整數(不為零)時,反應達到平衡的標志是
pC(g)+qD(g),當m、n、p、q為任意整數(不為零)時,反應達到平衡的標志是
①體系的壓強不再改變 ②體系的溫度不再改變 ③各組分的濃度不在改變
④各組分質量分數不再改變 ⑤反應速率v(A):v(B):v(C):v(D)=m:n:p:q
⑥單位時間內m molA斷鍵反應,同時p molC也斷鍵反應
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學課外活動小組設計實驗探究氮的化合物的性質,裝置如圖所示,其中A(裝置未畫出)為氣體發生裝置。檢查裝置氣密性后,先將C處鉑絲網加熱至紅熱,再將A處產生的氣體通過B裝置片刻后,撤去C處酒精燈。部分實驗現象如下:C處鉑絲繼續保持紅熱,F處銅片逐漸溶解。
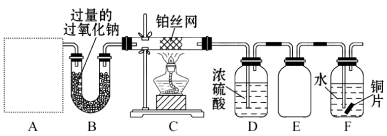
(1)實驗室制取A中氣體時若只用一種試劑,該試劑是 (填備選試劑的字母);
A.NH4HCO3 B.NH4Cl C.Ca(OH)2 D.NaOH
此時A中主要的玻璃儀器有 (填名稱);
(2)對于C中發生的可逆反應,其方程式為: ;
有關該反應的下列說法中正確的是 。
A.增大一種反應物的濃度可以提高另一種反應物的轉化率
B.工業上進行該反應時,可采取高壓的條件提高反應物轉化率
C.在一定條件下達到平衡時,反應物的平衡濃度之比一定是4∶5
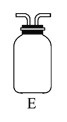
(3)E裝置可防止F中溶液倒吸進入D中,請在上圖中畫出裝置E中的導氣管。
(4)寫出F中發生反應的離子方程式: ;若進入F裝置的物質成分和質量一定,可向F中加入下列物質(填字母)中的 使銅片溶解的質量增多。
A.Na2CO3 B.NaCl C.CuSO4 D.H2SO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | Q | |
原子半徑 | 0.186 | 0.074 | 0.099 | 0.143 | ||
主要化合價 | -4,+4 | -2 | -1,+7 | +3 | ||
其他 | 陽離子無核外電子 | 無機非金屬材料的主角 | 焰色反應呈黃色 |
(1)X和M的原子可構成 18 電子的分子,該分子的結構式為 。
(2)R元素的單質與水反應的離子方程式是 。
(3)Z與Q相比,金屬性較強的是 (用元素符號表示),下列事實能證明這一結論的是 (填字母序號)。
a.Q的熔點比Z的熔點高,Q的硬度比Z的硬度大
b.Z與冷水反應迅速,而Q與冷水幾乎不反應
c.Z的最高價氧化物對應水化物是強堿,而Q的最高價氧化物對應水化物具有兩性
(4)與Y元素同主族的短周期元素E在自然界中存在多種核素,它們之間的關系互為 ,其中用于測定一些文物年代的核素的符號為 。
(5)寫出Z2M2與X2M反應的化學方程式并標出電子轉移關系。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com