
【題目】用烴A合成高分子化合物N的過程如下: 
已知:Ⅰ: 
Ⅱ: ![]()
Ⅲ:R1COOR2+R3OH ![]() R1COOR3+R2OH R1、R2、R3代表烴基或氫原子
R1COOR3+R2OH R1、R2、R3代表烴基或氫原子
回答下列問題:
(1)烴A的相對分子質量為26,A的結構簡式是 .
(2)B中所含官能團的名稱是 .
(3)C和D反應生成E的化學方程式是 .
(4)B和F反應生成G的化學方程式是 .
(5)H中含有一個甲基,H的結構簡式是 .
(6)E和K反應生成M的化學方程式是 .
(7)N和NaOH溶液反應的化學方程式是 .
(8)有機物Q是M的同分異構體,與M具有相同官能團,水解可以生成D,存在順反異構,Q的順式結構簡式是 .
【答案】
(1)CH≡CH
(2)醛基
(3)![]()
(4)![]()
(5)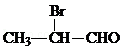
(6)![]()
(7)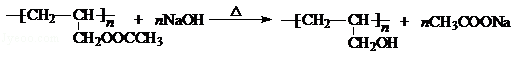
(8)
【解析】解:烴A的相對分子質量為26,則A為CH≡CH,B能發生銀鏡反應,則A與水發生加成反應生成B為CH3CHO,B被氧化成C為CH3COOH,根據E的分子式可知,C與甲醇在濃硫酸的作用下發生酯化反應生成E為CH3COOCH3 , 所以D為CH3OH,根據K的分子式結合轉化關系,B與F發生信息Ⅱ中的反應,生成G為CH2=CHCHO,所以F為HCHO,H中含有一個甲基,G與溴化氫發生加成反應生成H為 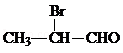 ,H與氫氣加成生成I為CH3CHBrCH2OH,I發生消去反應生成K為CH2=CHCH2OH,K和E發生信息Ⅲ中的酯交換反應生成M為CH3COOCH2CH=CH2 , M發生加聚反應得N為
,H與氫氣加成生成I為CH3CHBrCH2OH,I發生消去反應生成K為CH2=CHCH2OH,K和E發生信息Ⅲ中的酯交換反應生成M為CH3COOCH2CH=CH2 , M發生加聚反應得N為 ![]() .
.
(1.)根據上面的分析可知,A的結構簡式是CH≡CH,所以答案是:CH≡CH;
(2.)B為CH3CHO,B中所含官能團的名稱是醛基,所以答案是:醛基;
(3.)C與甲醇在濃硫酸的作用下發生酯化反應生成E為CH3COOCH3 , 反應生成E的化學方程式是 ![]() ,
,
所以答案是: ![]() ;
;
(4.)B和F反應生成G的化學方程式是 ![]() ,
,
所以答案是: ![]() ;
;
(5.)根據上面的分析可知,H的結構簡式是  ,
,
所以答案是:  ;
;
(6.)K和E發生信息Ⅲ中的酯交換反應生成M為CH3COOCH2CH=CH2 , 反應的化學方程式是 ![]() ,
,
所以答案是: ![]() ;
;
(7.)N和NaOH溶液發酯的水解反應,反應的化學方程式是  ,
,
所以答案是:  ;
;
(8.)M為CH3COOCH2CH=CH2 , 有機物Q是M的同分異構體,與M具有相同官能團,即有酯基和碳碳雙鍵,水解可以生成CH3OH,存在順反異構,說明碳碳雙鍵上連有不同的原子或原子團,則Q的順式結構簡式是  ,
,
所以答案是:  .
.


科目:高中化學 來源: 題型:
【題目】關于熱化學方程式:2H2(g)+O2 (g)![]() 2H2O(l), △H=﹣571.6kJmol﹣1,下列有關敘述不正確的是( )
2H2O(l), △H=﹣571.6kJmol﹣1,下列有關敘述不正確的是( )
A.2mol H2完全燃燒生成液態水時放出571.6 kJ的熱
B.1mol H2完全燃燒生成液態水時放出285.8kJ的熱
C.2個氫分子完全燃燒生成液態水時放出571.6 kJ的熱
D.上述熱化學方程式可表示為H2(g)+![]() O2(g) = H2O(l), △H=﹣285.8 kJmol﹣1
O2(g) = H2O(l), △H=﹣285.8 kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子能在無色澄清溶液大量共存的是
A. MnO4-、NO3-、K+、Cl- B. NH4+、Mg2+、SO42-、Cl-
C. Na+、H+、SO42-、CO32- D. K+、Na+、NO3-、Cu2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅冶金技術以火法冶煉為主.
(1)火法煉銅的工藝流程如下: 
反應Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=﹣768.2kJmol﹣1
反應Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJmol﹣1
①在反應Ⅱ中,每生成1mol SO2轉移電子mol.
②反應Cu2S(s)+O2(g)═2Cu(s)+SO2(g)的△H=kJmol﹣1 .
③理論上m1:m2= .
(2)煉銅的副產品SO2多用于制硫酸和石膏等化學產品.
①制硫酸中重要的一步反應是
2SO2(g)+O2(g)2SO3(g)△H=﹣196kJmol﹣1 .
圖表示將2.0mol SO 2 和1.0mol O 2 置于1L密閉容器中,當其他條件一定時,SO2(g)的平衡轉化率α隨X的變化關系,X(X1、X2)代表壓強或溫度.
X代表的物理量是 . A對應條件下平衡常數K= .
②下圖表示的是生產石膏的簡單流程,請用平衡移動原理解釋向CaCO3懸濁液中通入SO 2發生反應的原因 . 
(3)工業硫酸中往往含有一定量SO2 , 測定過程如下:取m g工業硫酸配成100mL溶液,取出20.00mL溶液,加入1mL指示劑,用c molL﹣1 I2標準溶液滴定,消耗的I2標準溶液V mL,工業硫酸中含有SO2的質量分數的計算式是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學在實驗室利用氫氧化鈉、鹽酸分離鐵粉和鋁粉混合物,物質轉化關系如圖所示: 
下列說法不正確的是( )
A.x為NaOH溶液,y為鹽酸
B.a→b發生的反應為:AlO2﹣+H++H2O═Al(OH)3↓
C.b→c→Al的反應條件分別為:加熱、電解
D.a、b、c既能與酸又能與堿反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】依據敘述,寫出下列反應的熱化學方程式:
(1)若適量的N2和O2完全反應,每生成23 g NO2需要吸收16.95 kJ熱量。其熱化學方程式為______________________________________________。
(2)用NA表示阿伏加德羅常數,在C2H2(氣態)完全燃燒生成CO2和液態水的反應中,每有5NA個電子轉移時,放出650 kJ的熱量。其熱化學方程式為
__________________________________________________________________。
(3)已知拆開1 mol H—H鍵、1 mol N—H鍵、1 mol N≡N鍵分別需要的能量是436 kJ、391 kJ、946 kJ,則N2與H2反應生成NH3的熱化學方程式為
___________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知拆開1 mol氫氣中的化學鍵需要消耗436 kJ能量,拆開1 mol氧氣中的化學鍵需要消耗498 kJ能量,根據如圖中的能量圖,回答下列問題:

(1)分別寫出①②的數值:
①__________;②__________。
(2)生成H2(Xg)中的1 mol H—O鍵放出__________kJ的能量。
(3)已知:H2O(l)![]() H2O(g)△H=+44 kJ mol1,試寫出氫氣在氧氣中完全燃燒生成液態水的熱化學方程式:___________________________________。
H2O(g)△H=+44 kJ mol1,試寫出氫氣在氧氣中完全燃燒生成液態水的熱化學方程式:___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫時,CaCO3在水中的溶解平衡曲線如圖所示,已知:25℃其溶度積為2.8×10﹣9 mol2/L2 , 下列說法不正確的是( ) 
A.x數值為2×10﹣5
B.c點時有碳酸鈣沉淀生成
C.加入蒸餾水可使溶液由d點變到a點
D.b點與d點對應的溶度積相等
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com