
【題目】Ni和Fe在工業生產和新型材料領域有廣泛的應用,黃鐵礦被稱“愚人金”,化學成分是FeS2,晶體屬正方體晶系的硫化物礦物。室溫為非活性物質。溫度升高后變得活潑。在空氣中氧化成三氧化二鐵和二氧化硫,主要用于接觸法制硫酸;回答下列問題:
(1)將FeS2與稀鹽酸所對應得到H2S2,H2S2分子中,共價鍵的類型是___________________;FeS2氧化得到SO2,在SO2分子中的S原子的雜化軌道類型是______________________;
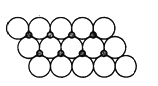
(2)FeS2的晶體中的Fe2+離子的排列方式如下圖所示:

①每個Fe2+周圍最近的等距離的S22-離子有________個;
②已知FeS2的晶胞參數是a0=54nm,它的密度為_____________gcm-3;(列式并計算,阿伏加德羅常數為6.02×1023)。
(3)NiO晶體結構與NaCl晶體類似,其晶胞的棱長為acm,則該晶體中距離最近的兩個陽離子核間的距離為___________(用含有a的代數式表示)。在一定溫度下,NiO晶體可以自發地分散并形成“單分子層”(如右圖),可以認為氧離子作密致單層排列,鎳離子填充其中,列式并計算每平方米面積上分散的該晶體的質量為________g(氧離子的半徑為1.40×10-10m,![]() =1.732)。
=1.732)。
【答案】(1)極性鍵和非極性鍵形成δ鍵 sp2
(2)①6 ②ρ=![]() =
=![]() =5.06
=5.06
(3)![]() ;
;![]() 1.83×10-3(g)
1.83×10-3(g)
【解析】
試題分析:(1)H2S2分子中,存在H-S鍵為極性共價鍵和S-S鍵為非極性共價鍵,在SO2分子中的S原子的價層電子對數為![]() =3,所以S原子的雜化軌道類型為sp2雜化;
=3,所以S原子的雜化軌道類型為sp2雜化;
(2)①每個Fe2+周圍最近的等距離的S22-離子存在于面心,共有6個;
②一個晶胞內含有Fe2+數目為8×![]() +6×
+6×![]() =4,含有S2-數目為12×
=4,含有S2-數目為12×![]() +1=4,一個晶胞的質量m=
+1=4,一個晶胞的質量m=![]() ,一個晶胞體積V=a03,則晶胞密度ρ=
,一個晶胞體積V=a03,則晶胞密度ρ=![]() =
=![]() =5.06gcm-3;
=5.06gcm-3;
(3)根據氯化鈉的結構知,氧離子和相鄰的鎳離子之間的距離為![]() ,距離最近的兩個陽離子核間的距離是距離最近的氧離子和鎳離子距離的
,距離最近的兩個陽離子核間的距離是距離最近的氧離子和鎳離子距離的![]() 倍,所以其距離是
倍,所以其距離是![]() acm;根據圖片知,每個氧化鎳所占的面積=2×1.40×10-10m×2×1.40×10-10m×sin60°,則每平方米含有的氧化鎳個數=
acm;根據圖片知,每個氧化鎳所占的面積=2×1.40×10-10m×2×1.40×10-10m×sin60°,則每平方米含有的氧化鎳個數=![]() ,每個氧化鎳的質量=
,每個氧化鎳的質量=![]() g,所以每平方米含有的氧化鎳質量═
g,所以每平方米含有的氧化鎳質量═![]() =1.83×10-3。
=1.83×10-3。


 提分百分百檢測卷系列答案
提分百分百檢測卷系列答案 寶貝計劃期末沖刺奪100分系列答案
寶貝計劃期末沖刺奪100分系列答案 能考試全能100分系列答案
能考試全能100分系列答案科目:高中化學 來源: 題型:
【題目】Ⅰ、按要求書寫下列化學方程式和名稱:
(1)1,3-丁二烯與等物質的量的單質溴在60℃時發生1,4-加成
(2)甲苯制備TNT ,用系統命名給TNT命名
(3)乙醛發生銀鏡反應
Ⅱ、(1)某烴A的質譜圖表明其相對分子質量為84,紅外光譜表明分子中含有碳碳雙鍵,與氫氣加成反應可得到結構簡式為(CH3)2CHCH(CH3)2的烷烴,則此烯烴可能的結構簡式是: (任寫一種)。
(2)核磁共振譜表明A分子中只有一種類型的氫。
①用系統命名法給A命名: 。
②A中的碳原子是否都處于同一平面? (填“是”或者“不是”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組同學進行如下實驗,以檢驗化學反應中的能量變化。請回答下列問題:

(1)實驗中發現,反應后①中的溫度升高;②中的溫度降低.由此判斷鋁條與鹽酸的反應是 熱反應, Ba(OH)28H2O與NH4Cl的反應是 熱反應.反應過程 (填“①”或“②”)的能量變化可用圖2表示。
(2)現有如下兩個反應:
(A)NaOH+HCl=NaCl+H2O (B)2FeCl3+Cu=2FeCl2+CuCl2
以上兩個反應能設計成原電池的是 , 負極材料為:____ ___,電解質溶液為:_______ ___,負極的電極反應式為:_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學技術名詞審定委員會已確定第116號元素Lv的名稱為鉝。關于![]() Lv的敘述錯誤的是
Lv的敘述錯誤的是
A. 原子序數116 B. 中子數177 C. 核外電子數116 D. 相對原子質量293
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有金屬單質A、B、C、I和氣體甲、乙、丙及物質D、E、F、G、H。其中B是地殼中含量最多的金屬。它們之間能發生如下反應(圖中有些反應的產物和反應的條件沒有全部標出)。
請根據以上信息回答下列問題:
(1)寫出下列物質的化學式 甲: 乙: C: H: 。
(2)寫出反應⑦的離子方程式: ________。
(3)要除去物質F中的物質G,可行的方法是( )
A.滴入KSCN溶液 B.通入足量的氯氣 C.滴入NAOH溶液 D.加入過量鐵粉
(4)若將D溶液滴入F溶液中,將其長時間露置于空氣中觀察到的現象為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由N、B等元素組成的新型材料有著廣泛用途。
(1)B2H6是一種高能燃料,它與Cl2反應生成的BCl3可用于半導體摻雜工藝及高純硅制造,由第二周期元素組成的與BCl3互為等電子體的陰離子為_________(填離子符號,填一個)。
(2)氮硼烷化合物(H2N→BH2)和Ti(BH4)3均為廣受關注的新型化學氮化物儲氫材料。
①H2N→BH2中N原子的雜化類型為_________;
②Ti(BH4)3由TiCl3和LiBH4反應制得。基態Ti3+的未成對電子數有____個,BH4-的立體構型是_________;寫出該制備反應的化學方程式_________;
③氮硼烷可由六元環狀化合物(HB=NH)3通過如下所對應制得:
3CH4+2(HB=NH)3+6H2O═3CO2+6H3BNH3與上述化學方程式有關的敘述不正確的是_________;.(填標號)
A.氮硼烷中存在配位鍵
B.第一電離能:N>O>C>B
C.反應前后碳原子的軌道雜化類型不變
D.CH4、H2O、CO2分子空間構型分別是:正四面體形、V形、直線形
(3)磷化硼(BP)是受到高度關注的耐麿材料;如圖1為磷化硼晶胞。
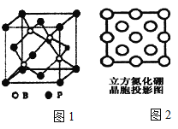
①磷化硼晶體屬于________晶體(填晶體類型),________(填是或否)含有配位鍵。
②晶體中B原子的配位數為_______。
(4)立方氮化硼是一種新型的超硬、耐麿、耐高溫的結構材料,其結構和硬度都與金剛石相似,但熔點比金剛石低,原因是________。圖2是立方氮化硼晶胞沿z軸的投影圖,請在圖中圓球上涂“●”和畫“×”分別標明B與N的相對位置。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國著名的化學家侯德榜先生(下圖)改革國外的純堿生產工藝,生產流程表示如下:

![]()
(1)沉淀池中發生的化學反應方程式是
________________________________________________________________________
________________________________________________________________________。
(2)寫出上述流程中X物質的分子式________。
(3)使原料氯化鈉的利用率從70%提高到90%以上,主要是設計了________(填上述流程中的編號)的循環。從沉淀池中取出沉淀的操作是________。
(4)為檢驗產品碳酸鈉中是否含有氯化鈉,可取少量試樣溶于水后,再滴加_______________________。
(5)向母液中通氨氣,加入細小食鹽顆粒,冷卻析出副產品,通氨氣的作用有________(填編號字母)。
(a)增大NH的濃度,使NH4Cl更多地析出
(b)使NaHCO3更多地析出
(c)使NaHCO3轉化為Na2CO3,提高析出的NH4Cl純度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米TiO2在涂料、光催化、化妝品等領域有著極其廣泛的應用。制備納米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,經過濾、水洗,再烘干、焙燒除去水分得到粉體TiO2 。用現代分析儀器測定TiO2粒子的大小。用氧化還原滴定法測定TiO2的質量分數:一定條件下,將TiO2溶解并還原為Ti3+ ,再以KSCN溶液作指示劑,用NH4Fe(SO4)2標準溶液滴定Ti3+至全部生成Ti4+。
請回答下列問題:
(1)TiCl4水解生成TiO2·x H2O的化學方程式為
(2)玻璃棒有多種用途,下列實驗操作中玻璃棒的作用完全相同的是 (填字母)
①測定醋酸鈉溶液的pH ②加熱食鹽溶液制備NaCl晶體
③配制0.1mol/L的硫酸溶液 ④用淀粉—KI試紙檢驗溶液中氧化性離子
⑤配制10%的硫酸鈉溶液
A.①⑤ B.②⑤ C.①④ D.③④
(3)水洗時檢驗TiO2·x H2O已洗凈的方法是
(4)下列可用于測定TiO2粒子大小的方法是 (填字母代號)
a.核磁共振氫譜 b.紅外光譜法 c.質譜法 d.透射電子顯微鏡法
(5)滴定終點的現象是
(6)滴定分析時,稱取TiO2(摩爾質量為Mg·mol-1)試樣w g,消耗c mol·L-1 NH4Fe(SO4)2標準溶液V mL,則TiO2質量分數表達式為 %
(7)下列操作會導致TiO2質量分數測定結果偏高的是
A. 滴定終點讀取滴定管刻度時,俯視標準液液面
B. 配制標準溶液時,燒杯中的NH4Fe(SO4)2溶液有少量濺出
C. 容量瓶清洗之后,未干燥
D.配制標準溶液定容時,俯視刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由丙烯經下列反應可制得F、G兩種高分子化合物,它們都是常用的塑料。化合物有E最早發現于酸牛奶中,它是人體內糖代謝的中間體,可由馬鈴薯.玉米淀粉等發酵制得,E的鈣鹽是人們喜愛的補鈣劑之一。
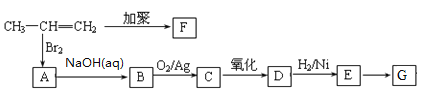
已知:![]()
(1)D中所含官能團名稱。E→G的反應類型為_________。
(2)聚合物F的結構簡式。聚合物G的結構簡式_________
(3)在一定條件下,兩分子E在濃硫酸作用下形成一種六元環狀化合物,該化合物的結構簡式是_________。
(4)B轉化為C的化學反應方程式是_________。
(5)下列四種化合物與E互為同分異構體的是_________。
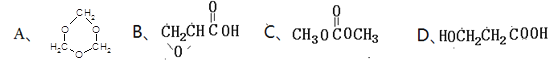
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com