
亞氯酸鈉(NaClO2)是一種強氧化性漂白劑,廣泛用于紡織、印染和食品工業。它在堿性環境中穩定存在。某同學查閱資料后設計生產NaClO2的主要流程如下。
(1)Ⅰ、Ⅲ中發生反應的還原劑分別是 、 (填化學式)。
(2)Ⅱ中反應的離子方程式是 。
(3)A的化學式是 ,裝置Ⅲ中A在 極區產生。
(4)ClO2是一種高效水處理劑,可用亞氯酸鈉和稀鹽酸為原料制備:
5NaClO2 + 4HCl =" 5NaCl" + 4ClO2↑ + 2H2O。
① 該反應中氧化劑和還原劑的物質的量之比是 。
② 研究表明:若反應開始時鹽酸濃度越大,則氣體產物中Cl2的含量越大,運用氧化還原反應規律分析其原因是 。
(5)NaClO2變質可分解為NaClO3和NaCl。取等質量變質前后的NaClO2試樣配成溶液,分別與足量FeSO4溶液反應時,消耗Fe2+的物質的量相同,從電子守恒的角度解釋其原因是 。
(1)Na2SO3 H2O(2分)
(2)2ClO2 + H2O2 + 2OH- = 2ClO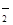 + O2↑+ 2H2O(2分)
+ O2↑+ 2H2O(2分)
(3)H2SO4(2分) 陽 (2分)
(4)1∶4 (2分) ClO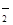 的氧化性或Cl-的還原性隨溶液的酸性和濃度的增大而增強,因此Cl-被氧化得到Cl2 (2分)
的氧化性或Cl-的還原性隨溶液的酸性和濃度的增大而增強,因此Cl-被氧化得到Cl2 (2分)
(5)NaClO2變質前后分別與Fe2+反應時,最終均得到等量NaCl,Cl元素均由+3價變為-1價,根據電子守恒,兩個過程中得到的電子的物質的量相同(2分)
解析試題分析:(1)Ⅰ中發生的反應是亞硫酸鈉被氯酸鈉氧化,、Ⅲ中發生的反應是電解水,因此在這兩個反應中還原劑分別是:Na2SO3 H2O(2分)
(2)2ClO2 + H2O2 + 2OH- = 2ClO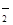 + O2↑+ 2H2O(2分)
+ O2↑+ 2H2O(2分)
(3)Ⅲ裝置中左邊氫氧根離子放電,剩余的氫離子跟硫酸根離子結合成硫酸,所以A是:H2SO4; 因為是氫氧根離子放電,所以這邊是電解池的陽極。
(4)在這個反應中發生的是亞氯酸鈉中氯元素的自身氧化還原反應,既作氧化劑,也作還原劑,作氧化劑的亞氯酸鈉是化合價降低的,也就是由正三價變成正一價,為一摩爾,作還原劑的亞氯酸鈉是化合價升高的,也就是由正三價變成正四價,為四摩爾,所以該反應中氧化劑和還原劑的物質的量之比是1∶4 ;ClO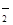 的氧化性或Cl-的還原性隨溶液的酸性和濃度的增大而增強,因此Cl-被氧化得到Cl2 。
的氧化性或Cl-的還原性隨溶液的酸性和濃度的增大而增強,因此Cl-被氧化得到Cl2 。
(5)NaClO2變質前后分別與Fe2+反應時,最終均得到等量NaCl,Cl元素均由+3價變為-1價,根據電子守恒,兩個過程中得到的電子的物質的量相同(2分)
考點:氧化還原反應的有關知識。


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:填空題
(1)某化學興趣小組為了探究Cl2的相關性質,設計了如下的實驗。
①寫出Cl2與水反應的離子方程式 。
②通入Cl2后,從集氣瓶A、B的現象可得出的結論是 ;從化學實驗的安全環保角度考慮,你認為還應增加的裝置是 。
(2)①如圖所示,上述實驗過程中,不會產生氣體的是 ;
②寫出反應D的化學方程式 。
(3)碘是人體中不可缺少的微量元素,食鹽中加入碘元素能有效防止缺碘引起的疾病。以前在食鹽中加入碘化鉀(KI),放置一年后,碘流失約92%。現在食鹽中加入碘酸鉀(KIO3),在相同條件下碘僅損失約7%。
①食鹽中加入碘化鉀的碘損失率高的原因是 ;
②萃取碘水中的碘時,一般選用的試劑是(填字母) ;
A.酒精 B.四氯化碳 C.醋酸 D.硝酸銀溶液
③可用鹽酸酸化的碘化鉀和淀粉溶液檢驗食鹽中的碘酸鉀。反應的化學方程式為:
5KI+KIO3 + 6HCl =" 6KCl" + 3I2 + 3H2O,反應的現象是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
光纖預制棒是光纜生產的最“源頭”項目,目前國內光纜生產廠家約200家,大部分靠買進口光纖預制棒來生產光纜。
(1)光纖預制棒跟光導纖維的成分相同,那么光纖預制棒的化學成分是 。
(2)如果把光纜裸露在堿性土壤中,結果會短路,用離子方程式說明原因 。
(3)下列說法正確的是 。
| A.石英與普通玻璃都是硅酸鹽制品 |
| B.二氧化硅是良好的半導體材料 |
| C.工藝師用鹽酸刻蝕石英制作藝術品 |
| D.石英與二氧化碳中的化學鍵相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E代表單質或化合物,它們之間的相互轉化關系如下圖所示。A為地殼中含量僅次于氧的非金屬元素的單質。
請填空:
(1)形成單質A的元素,在化合物中的最高化合價為 。
(2)B和碳反應生成A和E的化學方程式是 。
(3)C的化學式為 ,D 的化學式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鹽酸、硫酸和硝酸都是重要的化工原料,也是化學實驗室里必備的重要試劑。請回答下列問題:
(1) 常溫下,可用鐵、鋁制的容器盛放濃硫酸,說明濃硫酸具有 性,用玻璃棒蘸取濃硫酸滴在紙上,紙逐漸變黑,說明濃硫酸具有 性,實驗室不能用濃硫酸干燥氨氣,說明硫酸具有 性。
(2) 硝酸銅是制備Cu-Zn-Al系催化劑的重要原料,工業上用洗凈的廢銅屑作原料來制備硝酸銅。右圖所示制備方法符合“綠色化學”思想的
是 (填序號)。
(3) ①在100ml 18 mol/L濃硫酸中加入過量銅片,加熱使之充分反應,產生的氣體在標準狀況下的體積可能是 。
| A.40.32 L | B.30.24 L | C.20.16 L | D.13.44 L |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氫溴酸(HBr)是一種與鹽酸化學性質相似的物質,陽離子相同的溴鹽與氯鹽溶解性也比較相似,現有以下六種物質:Fe、Fe2O3、CO2、Cu(OH)2、CaCO3、Na2SO4,請從中選取物質,寫出能與氫溴酸反應的化學方程式(可不填滿,不反應的寫出倒扣1分,本題扣到0分為止):
(1)
(2)
(3)
(4)
(5)
(6)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
“探險隊員”——鹽酸,不小心走進了化學迷宮,迷宮有許多“吃人的野獸”(即能與鹽酸反應的物質或者是水溶液),鹽酸必須避開它們,否則就無法通過。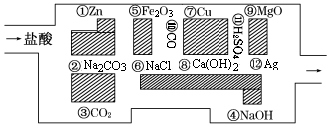
(1)請你幫助它走出迷宮(請用圖中物質前的序號表示):____________。
(2)在能“吃掉”鹽酸的化學反應中,屬于酸和堿中和反應的有 個。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
甲、乙兩組同學分別對銅、鐵與硝酸的反應進行探究,請你參與并完成對有關問題的解答。
(1)甲組同學采用如圖所示裝置驗證銅與硝酸的反應。已知儀器a中盛有足量一定濃度的硝酸溶液,試管b中盛有3.2 g銅。
①請寫出銅與稀硝酸反應的離子反應方程式 。
②在銅與硝酸的反應中,硝酸所表現出的化學性質主要有 。
③儀器c中收集的氣體主要是 。(填分子式)
④待試管b中反應進行完全,如果向b中液體里加入足量氫氧化鈉溶液,可生成沉淀的質量是 g。
(2)乙組同學對鐵與稀硝酸的反應進行探究。他們用a mol Fe和含有b mol HNO3的稀硝酸進行實驗,若兩種物質恰好反應都無剩余,且HNO3只被還原成NO,反應結束后溶液中含有Fe3+和Fe2+。則
①反應結束后的溶液中NO3-的物質的量的取值范圍是 。(用含a的代數式等表示)
②若反應結束后的溶液中Fe3+、Fe2+的物質的量之比n(Fe3+)∶n(Fe2+) 為3∶1,則b/a的值為 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
在500mL 0.2 mol·L-1的稀硝酸中加入1.92g銅片,讓其充分反應。試求:
(1)產生的氣體在標準狀況下所占的體積為多少?
(2)反應后溶液中H+的物質的量濃度是多少?(溶液體積變化忽略不計)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com