
常溫下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有關微粒的物質的量變化如下圖, 根據圖示判斷,下列說法正確的是
A.H2A在水中的電離方程式是:H2A  H+ + HA-;HA—
H+ + HA-;HA—  H+ + A2-
H+ + A2-
B.當V(NaOH)=20mL時,則有:c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)
C.等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水小
D.當V(NaOH)=30mL時,則有:2c(H+) + c(HA-) + 2c(H2A) = c(A2-) + 2 c(OH-)
BC
解析試題分析:由圖像可知溶液中存在H2A 、HA—、A2-三種微粒。所以H2A為二元弱酸。Ⅰ為H2A的變化曲線;Ⅱ為HA-的變化曲線;Ⅲ為A2-的變化曲線。H2A在水中的電離方程式是:H2A  H+ + HA-;HA—
H+ + HA-;HA— H+ + A2-。錯誤。B.當V(NaOH)=20mL時,恰好發生反應NaOH+ H2A=NaHA+H2O.根據物料守恒可得c(Na+) =c(H2A)+c(HA-)+c(A2-).因此c(Na+) > c(HA-)。在加入NaOH溶液20ml前HA-已經大量存在而且隨NaOH體積的增大而增多,說明HA-的電離作用大于水解作用。所以c(H+) > c(OH-) 。因為在溶液中除了HA-電離產生H+,水也電離產生H+。所以c(H+) > c(A2-)。強電解質的電離作用遠大于弱電解質的電離,所以c(HA-) > c(H+)。因此c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)。正確。C. 等體積等濃度的NaOH溶液與H2A溶液混合后得到NaHA.由于HA-的電離作用大于水解作用,所以溶液顯酸性。HA-電離產生的H+對水的電離平衡H2O
H+ + A2-。錯誤。B.當V(NaOH)=20mL時,恰好發生反應NaOH+ H2A=NaHA+H2O.根據物料守恒可得c(Na+) =c(H2A)+c(HA-)+c(A2-).因此c(Na+) > c(HA-)。在加入NaOH溶液20ml前HA-已經大量存在而且隨NaOH體積的增大而增多,說明HA-的電離作用大于水解作用。所以c(H+) > c(OH-) 。因為在溶液中除了HA-電離產生H+,水也電離產生H+。所以c(H+) > c(A2-)。強電解質的電離作用遠大于弱電解質的電離,所以c(HA-) > c(H+)。因此c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)。正確。C. 等體積等濃度的NaOH溶液與H2A溶液混合后得到NaHA.由于HA-的電離作用大于水解作用,所以溶液顯酸性。HA-電離產生的H+對水的電離平衡H2O H++OH-起到了抑制作用。所以其溶液中水的電離程度比純水小。正確。D. 當V(NaOH)=30mL時,溶液為NaHA與Na2A等物質的量的混合物。根據電荷守恒可得①c(Na+)+ c(H+)= 2c(A2-) + c(OH-)+ c(HA-).根據物料守恒可得②2c(Na+)=3c(H2A)+3 c(HA-)+3c(A2-)。將①整理代入②,可得2c(H+) + c(HA-) + 3c(H2A) = c(A2-) + 2 c(OH-)。錯誤。
H++OH-起到了抑制作用。所以其溶液中水的電離程度比純水小。正確。D. 當V(NaOH)=30mL時,溶液為NaHA與Na2A等物質的量的混合物。根據電荷守恒可得①c(Na+)+ c(H+)= 2c(A2-) + c(OH-)+ c(HA-).根據物料守恒可得②2c(Na+)=3c(H2A)+3 c(HA-)+3c(A2-)。將①整理代入②,可得2c(H+) + c(HA-) + 3c(H2A) = c(A2-) + 2 c(OH-)。錯誤。
考點:考查微粒濃度的大小比較、電離平衡、水解平衡的知識。


科目:高中化學 來源: 題型:單選題
下列各溶液中,有關成分的物質的量濃度關系正確的是 ( )
A.10mL 0.5mol/L CH3COONa溶液與6mL 1mol/L鹽酸混合:c(Cl-)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.0.1mol/L pH為4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.硫酸氫銨溶液中滴加氫氧化鈉至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D.pH相等的(NH4)2SO4、 (NH4)2Fe (SO4)2、NH4Cl溶液:c(NH4Cl)<c[(NH4)2Fe (SO4)2]< c[(NH4)2SO4]
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下向四份0.1 mol·L-1的醋酸鈉溶液中分別加入少量冰醋酸、硫酸氫鈉固體、醋酸鈉固體、氫氧化鈉固體(忽略溶液體積及溫度變化),則溶液中c(Ac-)/c(Na+)變化正確的是
| A.增大、增大、不變、減小 |
| B.增大、減小、增大、減小 |
| C.減小、增大、增大、減小 |
| D.增大、減小、不變、減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列敘述正確的是( )
| A.將稀氨水逐滴加入稀硫酸中,當溶液pH=7時,c(SO42-)>c(NH4+) |
| B.兩種醋酸溶液的物質的量濃度分別為c1和c2,pH分別為a和a+1,則c1=10c2 |
| C.pH=11的NaOH的溶液與pH=3的醋酸溶液等體積混合,滴入石蕊試液呈紅色 |
D.向0.1 mol/L的氨水中加入少量硫酸銨固體,則溶液中 增大 增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在0.1 mol·L-1的HCN溶液中存在如下電離平衡HCN H++CN-,對該平衡,下列敘述正確的是( )
H++CN-,對該平衡,下列敘述正確的是( )
| A.加入少量NaOH固體,平衡向正反應方向移動 |
| B.加水,平衡向逆反應方向移動 |
| C.滴加少量0.1 mol·L-1 HCl溶液,溶液中c(H+)減少 |
| D.加入少量NaCN固體,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一定溫度下,當Mg(OH)2固體在水溶液中達到下列平衡時:Mg(OH)2 Mg2++2OH-,要使Mg(OH)2固體減少而c(Mg2+)不變,可采取的措施是 ( )
Mg2++2OH-,要使Mg(OH)2固體減少而c(Mg2+)不變,可采取的措施是 ( )
| A.加MgSO4 | B.加HCl溶液 | C.加NaOH | D.加少量水 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法不正確的是 ( )
| A.Ksp只與難溶電解質的性質和溫度有關 |
| B.由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定條件下可轉化為CuS沉淀 |
| C.其他條件不變,離子濃度改變時,Ksp不變 |
| D.兩種難溶電解質作比較時,Ksp小的,溶解度一定小 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
水的電離平衡曲線如圖所示,下列說法不正確的是 ( )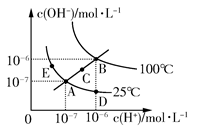
| A.圖中五點KW間的關系:B>C>A=D=E |
| B.若從A點到D點,可采用在水中加入少量酸的方法 |
| C.若從A點到C點,可采用溫度不變時在水中加入適量NH4Cl固體的方法 |
| D.若處在B點時,將pH=2的硫酸與pH=10的KOH等體積混合后,溶液顯中性 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列溶液一定呈中性的是 ( )。
| A.c(H+)=c(OH-)=10-6 mol·L-1的溶液 |
| B.pH=7的溶液 |
| C.使石蕊試液呈紫色的溶液 |
| D.酸與堿恰好完全反應生成正鹽的溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com