
【題目】如圖是四種常見有機物的比例模型,請回答下列問題:

(1)向丙中加入溴水,振蕩靜置后,觀察到溶液分層,上層為_______色。
(2)甲的同系物的通式為CnH2n+2,當n=5時,寫出含有3個甲基的有機物的結構簡式_____。
下圖是用乙制備D的基本反應過程

(3)A中官能團為__________。
(4)反應①的反應類型是__________。
(5)寫出反應④的化學方程式_______。
(6)現有138gA和90gC發生反應得到80gD。試計算該反應的產率為______(用百分數表示,保留一位小數)。
【答案】橙紅(或橙) ![]() —OH (或羥基) 加成反應 CH3COOH+CH3CH2OH
—OH (或羥基) 加成反應 CH3COOH+CH3CH2OH ![]() CH3 COOCH2CH3+H2O 60.6%
CH3 COOCH2CH3+H2O 60.6%
【解析】
由四種常見有機物的比例模型可知,甲為CH4,乙為乙烯,丙為苯,丁為CH3CH3OH。乙烯與水反應生成乙醇,乙醇氧化生成乙醛,乙醛氧化生成乙酸,乙醇和乙酸發生酯化反應生成乙酸乙酯,乙醇D為乙酸乙酯,結合四種物質的結構和性質分析解答。
(1)苯的密度比水小,溴易溶于苯,上層溶液顏色為橙紅色(或橙色),下層為水層,幾乎無色,故答案為:橙紅(或橙);
(2)當n=5時,分子中含有3個甲基,則主鏈有4個C原子,應為2-甲基丁烷,結構簡式為![]() ,故答案為:
,故答案為:![]() ;
;
(3)乙烯與水反應生成乙醇,乙醇氧化生成乙醛,乙醛氧化生成乙酸,乙醇和乙酸發生酯化反應生成乙酸乙酯,乙醇D為乙酸乙酯,因此A為乙醇,含有的官能團為-OH (或羥基),故答案為:-OH(或羥基);
(4)反應①為乙烯與水的加成反應,故答案為:加成反應;
(5)反應④為乙醇和乙酸的酯化反應,反應的化學方程式為CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,故答案為:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,故答案為:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(6)138g乙醇的物質的量為![]() =3mol,90g乙酸的物質的量為
=3mol,90g乙酸的物質的量為![]() =1.5mol,則乙酸完全反應,可得1.5mol乙酸乙酯,質量為132g,而反應得到80g乙酸乙酯,則反應的產率為
=1.5mol,則乙酸完全反應,可得1.5mol乙酸乙酯,質量為132g,而反應得到80g乙酸乙酯,則反應的產率為![]() ×100%=60.6%,故答案為:60.6%。
×100%=60.6%,故答案為:60.6%。


 心算口算巧算一課一練系列答案
心算口算巧算一課一練系列答案科目:高中化學 來源: 題型:
【題目】碘化亞銅(CuⅠ)是陽極射線管覆蓋物,不溶于水和乙醇。下圖是工業上由冰銅制取無水碘化亞銅的流程。
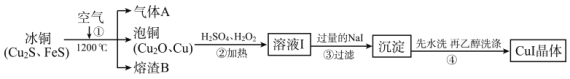
(1)FeS中S的化合價為_____________。
(2)步驟①中Cu2S被轉化為Cu,同時有大氣污染物A生成,相關化學反應方程式為_____________,熔渣B的主要成分為黑色磁性物質,其化學式為_____________。
(3)步驟②中H2O2的作用是_____________;步驟③中加入過量NaI涉及的主要離子反應方程式為_____________。
(4)步驟④用乙醇洗滌的優點是_____________;檢驗沉淀是否洗滌干凈的方法是_____________。
(5)溶液I中通常含少量Fe(Ⅲ)。已知該工業條件下,Fe(OH)3的Ksp=1.0×10-38,據此分析除去Fe(Ⅲ)(即c(Fe3+)≤1.0×10-5mol/L)應調節pH不小于_____________(水的離子積以常溫計)。
(6)準確稱取 m g CuI樣品,加入足量的Fe2(SO4)3溶液,發生反應為2CuⅠ+4Fe3+===2Cu2++4Fe2++I2,待樣品完全反應后,用amol/L酸性KMnO4溶液滴定Fe(Ⅱ),消耗標準液的體積平均值為ⅴmL。樣品中CuI的質量分數的計算表達式為_____________;如果滴定前,酸式滴定管沒有用標準液潤洗,CuI的質量分數_____________(填“偏低”、“偏高”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將等物質的量的X、Y氣體充入一個密閉容器中,在一定條件下發生如下反應并達到平衡:X(g)+Y(g) ![]() 2Z(g) ΔH<0。當改變某個條件并達到新平衡后,下列敘述正確的是( )
2Z(g) ΔH<0。當改變某個條件并達到新平衡后,下列敘述正確的是( )
A. 升高溫度,X的體積分數減小
B. 增大壓強(縮小容器體積),Z的濃度不變
C. 保持容器體積不變,充入一定量的惰性氣體,Y的濃度不變
D. 保持容器體積不變,充入一定量的Z,X的體積分數增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物“利尿酸”是一種常見的興奮劑,其分子結構如下圖,下列說法正確的是

A. 利尿酸是芳香烴
B. 利尿酸與AgNO3溶液反應有白色沉淀生成
C. 一定條件下,利尿酸能發生取代反應、加成反應和酯化反應
D. 1mol利尿酸與飽和碳酸鈉溶液反應能放出1 mol CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究性學習小組用高錳酸鉀粉末與濃鹽酸制取氯氣,并驗證其性質。

(資料在線)高錳酸鉀粉末與濃鹽酸混合即產生氯氣。
請回答下列問題:
(1)該實驗中A部分的裝置應選用下圖中的______(填序號)

(2)實驗中A發生反應的離子方程式是_________。
(3)一段時間后D中的現象為_________。
(4)請你設計一個實驗,證明洗氣瓶C中的亞硫酸鈉已被氧化(簡述實驗步驟) _________。
(5)圖(1)整套實驗裝置存在的明顯缺陷是_________。
(6)圖(2)裝置a處通入氯氣,證明氯氣是否具有漂白性,該設計能否達到實驗目的? _________ (填“能”或“不能”)。若能請說明理由,若不能則提出改進的措施_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1,2-二氯丙烷(CH2ClCHClCH3)是重要的化工原料,工業上可用丙烯加成法生產,主要副產物為3-氯丙烯(CH2=CHCH2C1) ,反應原理為
i.CH2=CHCH,3(g)+Cl2(g)![]() CH2ClCHClCH3(g) ΔH1= -134 kJ mol-1
CH2ClCHClCH3(g) ΔH1= -134 kJ mol-1
ii.CH2=CHCH,3(g)+Cl2(g)![]() CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ mol-1
CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ mol-1
已知:相關化學鍵的鍵能數據如下表所示:
化學鍵 | C=C | C—C | C—Cl | Cl—Cl |
E/( kJ mol-1) | 611 | x | 328 | 243 |
請回答下列問題:
(1)由反應i計算出表中x=_____________。
(2)一定溫度下,密閉容器中發生反應i和反應ii,達到平衡后增大壓強,CH2C1CHC1CH3的產率______(填“增大”“減小”或“不變”),理由是_________________________________。
(3)T1℃時,向10L恒容的密閉容器中充入1 mol CH2=CHCH2C1和2 mol HC1,只發生反應CH2=CH CH2Cl (g)+HCl(g)![]() CH2ClCHClCH3(g) ΔH3。 5min反應達到平衡,測得 05 min內,用CH2ClCHClCH3表示的反應速率 v(CH2ClCHClCH3)=0.016 mol·L-1 min-1。
CH2ClCHClCH3(g) ΔH3。 5min反應達到平衡,測得 05 min內,用CH2ClCHClCH3表示的反應速率 v(CH2ClCHClCH3)=0.016 mol·L-1 min-1。
①平衡時,HCl的體積分數為_________(保留三位有效數字)。
②保持其它條件不變,6 min時再向該容器中充入0.6 mol CH2=CHCH2Cl、0.2molHC1和0.1mol CH2ClCHClCH3,則起始反應速率 v正(HCl)___ V逆(HCl) (填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于晶體說法的正確組合是

①分子晶體中都存在共價鍵
②在晶體中只要有陽離子就一定有陰離子
③金剛石、SiC、NaF、NaCl、H2O、H2S晶體的熔點依次降低
④離子晶體中只有離子鍵沒有共價鍵,分子晶體中肯定沒有離子鍵
⑤CaTiO3晶體中(晶胞結構如上圖所示)每個Ti4+和12個O2-緊鄰
⑥SiO2晶體中每個硅原子與兩個氧原子以共價鍵相結合
⑦晶體中分子間作用力越大,分子越穩定
⑧氯化鈉熔化時離子鍵被破壞
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知充分燃燒a g乙炔氣體時生成1 mol二氧化碳氣體和液態水,并放出熱量b kJ,則乙炔燃燒的熱化學方程式正確的是
A. 2C2H2(g)+5O2(g)![]() 4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1
4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1
B. 2C2H2(g)+5O2(g)![]() 4CO2(g)+2H2O(g) ΔH=-4b kJ·mol-1
4CO2(g)+2H2O(g) ΔH=-4b kJ·mol-1
C. 2C2H2(g)+5O2(g)![]() 4CO2(g)+2H2O(l) ΔH=-4b kJ·mol-1
4CO2(g)+2H2O(l) ΔH=-4b kJ·mol-1
D. 2C2H2(g)+5O2(g)![]() 4CO2(g)+2H2O(l) ΔH=+4b kJ·mol-1
4CO2(g)+2H2O(l) ΔH=+4b kJ·mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com