
甲、乙、丙、丁、戊、己為原子序數依次增大的短周期主族元素。甲、丙處于同一主族,丙、丁、戊處于同一周期,乙元素最高化合價與最低價的代數和為0;丙、丁、戊的最高價氧化物的水化物之間都能發生反應。用化學用語回答下列問題:
(1)甲的陰離子的結構示意圖為 ;用電子式表示乙與戊形成化合物的過程 。
(2)丙、丁、戊的離子半徑由大到小的順序為 ;乙、戊、己的氫化物的還原性最弱的是 。
(3)寫出由甲乙兩元素形成的化合物中,既含有極性鍵又含有非極性鍵,且相對分子質量最小的物質的結構式 ;該物質與空氣在酸性條件下可構成燃料電池,該電池放電時,負極的反應式為 。
(4)丙、丁的最高價氧化物的水化物之間發生反應的離子方程式為 。由甲、丙、戊、己中部分元素形成的兩種化合物的水溶液之間可以發生反應,該化學方程式為: 。
(5)按下圖電解丙和己形成化合物的飽和溶液,該裝置可用于家庭用水的消毒。寫出該電解池中發生反應的總反應方程式: 。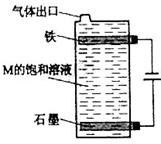
(1) 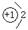 (1分)
(1分) 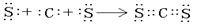 (2分)
(2分)
(2)S2->Na+>Al3+ (2分) HCl(2分)
(3)H-C≡C-H (1分) C2H2 + 4H2O ? 10e-= 2CO2+10H+(2分)
(4)Al(OH)3+OH- =AlO2- +2H2O (2分); NaHS+HCl= NaCl+H2S 或 Na2S + H 2S =2 NaHS(2分)
(5)NaCl+H2O NaClO+H2↑ (2分)
NaClO+H2↑ (2分)
解析試題分析:根據丙、丁、戊處于同一周期,且丙、丁、戊的最高價氧化物的水化物之間都能發生反應,可知丁為Al,該三種元素處于第三周期,氫氧化鋁能夠與強堿和強酸反應,結合題意,原子序數依次增大的短周期主族元素,推出丙為Na,戊為S,己為Cl;根據乙元素最高化合價與最低價的代數和為0,乙為C元素,甲、丙處于同一主族,甲為H元素。(1)氫的陰離子最外層有2個電子,碳和硫之間以共價鍵形成CS2;(2)根據電子層數越多半徑越大,電子層排布相同的離子,離子半徑大小與核電荷數大小成反比,即S2->Na+>Al3+ ,氫化物的還原性與非金屬性成反比例,非金屬性越強,其氫化物的還原性越弱,其還原性順序:H2S>CH4>HCl;(3)甲、乙兩元素形成的化合物屬于烴類,含有極性鍵又含有非極性鍵,且相對分子質量最小的物質,含2個碳,含H個數最少,綜合判斷為乙炔,結構簡式為:H-C≡C-H ,乙炔燃料電池,負極是乙炔失去電子發生氧化反應,酸性條件下電極反應式為: C2H2 + 4H2O ? 10e-= 2CO2+10H+;(4)氫氧化鈉與氫氧化鋁反應離子方程式為Al(OH)3+OH- =AlO2- +2H2O ,H、Na、S、Cl形成的化合物,應該是硫化物(H2S、NaHS或Na2S)和氯化物(HCl和NaCl),其中能發生反應的是NaHS+HCl= NaCl+H2S或Na2S + H 2S =2 NaHS;(5)電解飽和氯化鈉溶液,陽極在裝置的下部,陽極反應生成的氯氣往上溢出的過程中與陰極附近的氫氧化鈉反應生成次氯酸鈉,起到消毒作用,總電解反應為NaCl+H2O NaClO+H2↑。
NaClO+H2↑。
考點:元素周期律、離子方程式書寫、電解池反應原理知識。


 桃李文化快樂暑假武漢出版社系列答案
桃李文化快樂暑假武漢出版社系列答案 優秀生快樂假期每一天全新寒假作業本系列答案
優秀生快樂假期每一天全新寒假作業本系列答案科目:高中化學 來源: 題型:填空題
利用化石燃料開采、加工過程產生的H2S廢氣制取氫氣,既價廉又環保。
(1)工業上可用組成為K2O·M2O3·2RO2·nH2O的無機材料純化制取的氫氣。
①已知元素M、R均位于元素周期表中第三周期,兩種元素原子的質子數之和為27,則R的原子結構示意圖為________。
②常溫下,不能與M單質發生反應的是________(填序號)。
a.CuSO4溶液 b.Fe2O3 c.濃硫酸 d.NaOH溶液 e.Na2CO3固體
(2)利用H2S廢氣制取氫氣的方法有多種。
①高溫熱分解法
已知:H2S(g) H2(g)+
H2(g)+ S2(g)
S2(g)
在恒容密閉容器中,控制不同溫度進行H2S分解實驗。以H2S起始濃度均為c mol·L-1測定H2S的轉化率,結果見下圖。圖中a為H2S的平衡轉化率與溫度關系曲線,b曲線表示不同溫度下反應經過相同時間且未達到化學平衡時H2S的轉化率。據圖計算985℃時H2S按上述反應分解的平衡常數K=________;說明隨溫度的升高,曲線b向曲線a逼近的原因:____________________________________。
②電化學法
該法制氫過程的示意圖如下。反應池中反應物的流向采用氣、液逆流方式,其目的是______________________________;
反應池中發生反應的化學方程式為____________________。反應后的溶液進入電解池,電解總反應的離子方程式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F均為短周期元素,且原子序數依次增大,A是原子半徑最小的元素,B的最高價氧化物的水化物可與其氫化物反應形成離子化合物甲;A與D可以按照原子個數比4∶1形成化合物乙,且乙分子中含有18個電子,E與B同主族,C的陽離子與F的陰離子相差一個電子層,且可形成離子個數比為2∶1的離子化合物丙。
(1)D的原子結構示意圖為 ________ ,丙的電子式為___________ ,E在周期表中的位置為 。
(2)下列說法正確的有 。
①化合物乙分子中只含有極性共價鍵
②C、D、E、F原子半徑由大到小的順序為C>D>E>F
③B、E形成的氫化物中,B的氫化物更穩定
④化合物甲和化合物丙都含有離子鍵和共價鍵
(3)將F燃燒的產物通入BaCl2和HNO3的混合溶液中,生成白色沉淀并放出無色氣體,請用一個離子方程式表示該反應 __________________ 。
(4)寫出一個由以上元素構成的10電子微粒與18電子微粒反應的離子方程式 ____________________________ 。
(5)甲溶液顯 (填“酸性”、“堿性”或“中性”),原因是 (用離子方程式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
)已知甲、乙、丙、丁、戊、己為短周期元素形成的六種粒子,它們的電子總數都為18,請回答下列問題:
(1)甲為雙核單質分子,可與水發生置換反應,甲的電子式為 。
(2)乙為兩種元素形成的雙核離子,含該離子的水溶液中加入適量氯水出現渾濁,該反應的離子方程式為 。
(3)丙為含兩種元素的分子,且原子個數比為1∶1,實驗室中可以用丙制備氧氣,反應的化學方程式為 。
(4)戊屬于烴,已知1 g戊在氧氣中完全燃燒放出52 kJ的熱量,戊燃燒的熱化學方程式為 。
(5)己為兩種元素組成的六原子分子,常用作火箭的燃料,則己的化學式為 ______________ ,分子中含有的化學鍵為 (填“離子鍵”或“共價鍵”)。己與丙反應可生成對環境沒有影響的兩種物質,一種是大氣的主要成分,另一種在常溫下是無色液體,該反應的化學方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F是元素周期表中前20號元素,它們的原子序數依次增大。A、B可分別與C組成常見化合物AC、AC2、BC、BC2;D元素的焰色反應呈黃色;E、F兩元素單質的沸點與元素原子序數的關系如圖(圖中原子序數連續)。
(1)A在元素周期表中的位置是 。
(2)B2的電子式為 ,C、D、F對應的簡單離子半徑由小到大的順序為 (用離子符號表示)。
(3)C、F的單質或兩元素之間形成的化合物可作水消毒劑的有 (寫出其中兩種物質的化學式)。
(4)化合物Y由C、E兩元素組成,將Y、B單質與A單質按1∶1∶3在一定條件下反應可得到Z和AC,Z的化學式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
X、Y、Z、W是元素周期表前四周期常見的四種元素,原子序數依次增大。X原子核外有兩種形狀的電子云,四種伸展方向,常溫下以雙原子分子存在,性質穩定;Y的單質是生活中常見的合金材料成分之一,原子核外只有一個未成對電子,Z原子的半徑比X大,其基態原子最外層的p電子是該層s電子的兩倍,W是最常見的黑色金屬之一。
(1)Z位于元素周期表中的位置是 ,W3+的最外層電子排布式是______,X的氧化物XO2與H2O比較,熔點較高的是______ (填化學式)。
(2)加熱條件下,Z的單質與足量的X的最高價氧化物的水化物的濃溶液反應,生成Z的最髙價含氧酸,寫出此反應的化學方程式 。.
(3)比較Y、W性質的活潑性 (用一個化學反應方程式表示)。
(4)2013年初,全國各地多個城市都遭遇“十面霾伏”,造成“陰霾天”的主要根源之一是汽車尾氣和燃煤尾氣排放出來的固體小顆粒PM2.5。汽車尾氣凈化的主要原理為:2NO(g)+2CO(g) 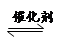 2CO2(g)+N2(g)。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示。
2CO2(g)+N2(g)。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示。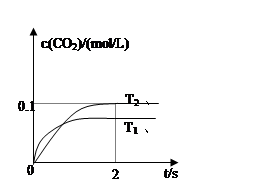
據此判斷:
該反應為 反應(放熱、吸熱);在T2溫度下,0~2s內的平均反應速率:υ(N2)= ;
(5)當固體催化劑的質量一定時,增大其表面積可提高化學反應速率。若催化劑的表面積S1>S2,
在上圖中畫出c(CO2)在T1、S2條件下達到平衡過程中的變化曲線。
(6)若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。
(下圖中υ正、K、n、w分別表示正反應速率、平衡常數、物質的量和質量)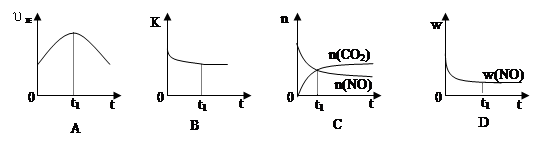
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、X、Y、Z元素的原子序數依次增大,根據信息完成問題:
| 元素A | 各能級上的電子數相等 |
| 元素C | 某種核素原子的質量數為18,中子數為10 |
| 元素X | 單質是良好的半導體材料 |
| 元素Y | 其單質為淡黃色晶體,常用來處理打碎的水銀溫度計 |
| 元素Z | 3d能級上有4個未成對電子 |
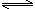 H+(aq)+CH3COO—(aq) △H=+akJ/mol
H+(aq)+CH3COO—(aq) △H=+akJ/mol查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E是短周期的五種主族元素。A元素的某種原子,其核內沒有中子;B元素的基態原子2p軌道上只有一對成對電子;C與B處于同一周期,且原子半徑小于B;D與C是同主族元素;E元素的一價陽離子和C元素的陰離子具有相同的電子層結構。根據上述信息回答下列問題:
(1)B元素的原子結構示意圖是 ;C元素原子的電子排布圖是 ;D元素原子的價電子排布式是 ;
(2)A元素分別與C、D兩元素形成的化合物的穩定性由強到弱的順序是(用化學式表示) ;(3)由B、D、E三種元素組成的某種化合物的水溶液能使pH試紙先變藍后褪色,寫出該化合物的化學式 ;用一個離子方程式表明該化合物水溶液使pH試紙先變藍后褪色的原因 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
短周期元素Q、R、T、W在元素周期表中的位置如圖所示,其中,T所處的周期序數與主族序數相等,請回答下列問題: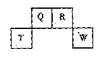
(1)T的原子結構示意圖為
(2)元素的非金屬性為(原子的得電子能力):Q ______ W(填“強于”或“弱于”)。
(3)W的單質與其最高價氧化物的水化物濃溶液共熱能發生反應,生成兩種物質,其中一種是氣體,反應的化學方程式為 。
(4)原子序數比R多1的元素的一種氫化物能分解為它的另一種氫化物,此分解反應的化學方程式是 。
(5)R有多種氧化物,其中甲的相對分子質量最小。在一定條件下,2L的甲氣體與0.5L的氧氣相混合,若該混合氣體被足量的NaOH溶液完全吸收后沒有氣體殘留,所生成的R的含氧酸鹽只有一種,則該含氧酸鹽的化學式是
(6)在298K下,Q、T的單質各1mol完全燃燒,分別放出熱量aKJ和bKJ。又知一定條件下,T的單質能將Q從它的最高價氧化物中置換出來,若此置換反應生成3molQ的單質,則該反應在298K下的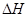 = ( 注:題中所涉單質均為最穩定單質)。
= ( 注:題中所涉單質均為最穩定單質)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com