
【題目】已知HF 和HCN 都是一元弱酸,但Ka(HF)>Ka(HCN)。現有100mL0.1mol/L 的NaF 溶液(代號“甲”)和100mL 0.1mol/L 的NaCN 溶液(代號“乙”),下列有關甲、乙兩種溶液的說法中不正確的是( )
A. 溶液pH:甲<乙 B. 溶液中弱酸分子濃度:c(HF)>c(HCN)
C. 甲溶液中:c(HF)=c(OH-)-c(H+) D. 乙溶液中: c(Na+)=c(CN-)+c(HCN)
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】復分解反應能夠發生是因為在這些反應物中含有一些“特殊”的陰、陽離子,它們能相互結合。如反應“BaCl2+Na2SO4![]() BaSO4↓+2NaCl”中,實際參加反應的離子是Ba2+和SO42-,而Cl、Na+則是“旁觀者”,并沒有參加反應。請你反應“K2CO3+2HCl=2KCl+CO2↑+H2O”中實際參加反應的離子是________;該反應的離子方程式是____________________________。請根據你的想象,在下圖右邊的容器中畫出體現NaOH溶液和稀鹽酸反應產物的示意圖。
BaSO4↓+2NaCl”中,實際參加反應的離子是Ba2+和SO42-,而Cl、Na+則是“旁觀者”,并沒有參加反應。請你反應“K2CO3+2HCl=2KCl+CO2↑+H2O”中實際參加反應的離子是________;該反應的離子方程式是____________________________。請根據你的想象,在下圖右邊的容器中畫出體現NaOH溶液和稀鹽酸反應產物的示意圖。
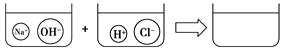 ________
________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式碳酸鎂[4MgCO3·Mg(OH)2·4H2O]是重要的無機化工產品。一種由白云石[主要成分為CaMg(CO3)2,還含少量SiO2、Fe2O3等]為原料制備堿式碳酸鎂(國家標準中CaO的質量分數≤0.43%)的實驗流程如下:
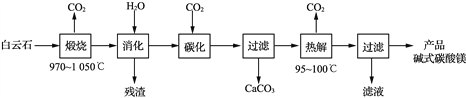
(1) “煅燒”時發生主要反應的化學方程式為____________________________。
(2)常溫常壓下“碳化”可使鎂元素轉化為Mg(HCO3)2,“碳化”時終點pH對最終產品中CaO含量及堿式碳酸鎂產率的影響如圖1和圖2所示。
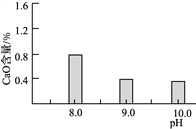
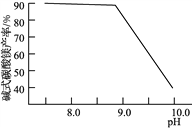
圖1 CaO含量與碳化終點pH的關系 圖2 堿式碳酸鎂產率與碳化終點pH的關系
①應控制“碳化”終點pH約為________,發生的主要反應的化學方程式為______________________和____________________。
②圖2中,當pH=10.0時,鎂元素的主要存在形式是____________(寫化學式)。
(3)“熱解”生成堿式碳酸鎂的化學方程式為________________________________。
(4)該工藝為達到清潔生產,可以循環利用的物質是____________(寫化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通過反應 ,可制備有機中間體異氰酸苯酯。
,可制備有機中間體異氰酸苯酯。
(1) Ni3+基態核外電子排布式為________。
(2)異氰酸苯酯分子中碳原子雜化軌道類型是________,1 mol異氰酸苯酯分子中含有σ鍵數目為________。
(3)Na、O、C、N四種元素的第一電離能從大到小的順序為_________________________。
(4) C2H5OH的沸點高于![]() ,這是因為__________________。
,這是因為__________________。
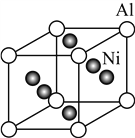
(5) Ni與Al形成的一種合金可用于鑄造飛機發動機葉片,其晶胞結構如右圖所示,該合金的化學式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.尿素[CO(NH2)2]是一種非常重要的高效氮肥,工業上以NH3、CO2為原料生產尿素,該反應實際為兩步反應:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)寫出工業上以NH3、CO2為原料合成尿素的熱化學方程式:_________________________
(2)某實驗小組模擬工業上合成尿素的條件,在一體積為0.5 L密閉容器中投入4 mol氨和1mol二氧化碳,實驗測得反應中各組分的物質的量隨時間的變化如下圖所示:
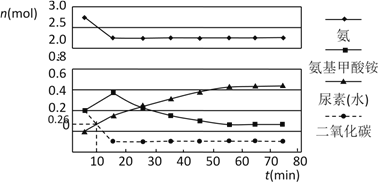
已知總反應的快慢由慢的一步決定,則合成尿素總反應的快慢由第_________步反應決定,總反應進行到_________min時到達平衡。
(3)電解尿素[CO(NH2)2]的堿性溶液制純凈氫氣的過程中同時產生氮氣。電解時,陽極的電極反應式為________________________________。
Ⅱ.用焦炭還原NO2的反應為:2NO2(g)+2C(s )![]() N2(g)+2CO2(g),在恒溫條件下,1 mol NO2和足量C發生該反應,測得平衡時NO2和CO2的物質的量濃度與平衡總壓的關系如圖所示:
N2(g)+2CO2(g),在恒溫條件下,1 mol NO2和足量C發生該反應,測得平衡時NO2和CO2的物質的量濃度與平衡總壓的關系如圖所示:
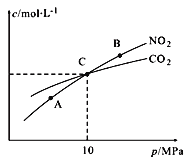
①A、B兩點的濃度平衡常數關系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②計算C點時該反應的壓強平衡常數Kp(C)=______(Kp是用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是部分短周期元素原子半徑與原子序數的關系圖,下列說法正確的是( )
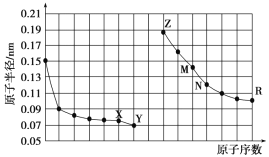
A. M、N的氧化物都能與Z、R的最高價氧化物對應水化物反應
B. Y的單質能從含R簡單離子的水溶液中置換出R單質
C. X、M兩種元素組成的化合物熔點很高
D. 簡單離子的半徑:R>M>X
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在無色透明溶液中,下列各組中的離子一定能大量共存的是( )
A.K+、H+、SO42-、MnO4-B.Na+、Ca2+、Cl-、NO3-
C.Ag+、H+、Cl-、CH3COO-D.Ba2+、K+、OH-、SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Fe2O3+2Al![]() Al2O3+2Fe所屬基本反應類型是______。在該反應中______元素的化合價升高,該元素的原子______電子,被______。該反應中,Fe2O3發生了________反應,Al發生了______反應,______是氧化劑,__是還原劑,______是氧化產物,_____是還原產物。
Al2O3+2Fe所屬基本反應類型是______。在該反應中______元素的化合價升高,該元素的原子______電子,被______。該反應中,Fe2O3發生了________反應,Al發生了______反應,______是氧化劑,__是還原劑,______是氧化產物,_____是還原產物。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com