
【題目】對于反應2SO2+O2![]() 2SO3的敘述不正確的是( )
2SO3的敘述不正確的是( )
A.該反應是可逆反應,在相同條件下,反應可同時向兩個方向進行
B.1mol氧氣與2mol二氧化硫混合發生反應能生成2mol三氧化硫
C.在該反應中二氧化硫作還原劑,氧氣作氧化劑
D.該反應有0.4mol電子發生轉移時,生成三氧化硫0.2mol
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】在某一容積為2L的恒容密閉容器中,A、B、C、D四種氣體物質發生可逆反應,其物質的量n(mol)隨時間t(min)的變化曲線如圖所示。回答下列問題:
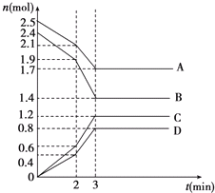
(1)該反應的化學方程式為______。
(2)前2min內用A的濃度變化表示的化學反應速率為_______, 4min時,v正(A)______v逆(D) (填“>”“<”或“=”)。
(3)在2min時,圖象發生改變的原因可能是_____(填字母)
A 增大B的物質的量 B 降低溫度
C 加入催化劑 D 減小A的物質的量
(4)能說明該反應已達到平衡狀態的標志是_______(填字母)。
A 消耗5mol B的同時生成4molD
B 反應速率4v(B) = 5v (D)
C 容器內D的濃度不再隨時間而發生變化
D 容器內壓強不再隨時間而發生變化
E 容器內混合氣體的密度不再隨時間而發生變化
(5)由圖示求得平衡時A的轉化率為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向濃度相等、體積均為50ml的A、B兩份氫氧化鈉溶液中分別通入一定量的二氧化碳后,再稀釋至100ml。
(1)向氫氧化鈉溶液中通入一定量的二氧化碳后,溶液中溶質的可能組成有:①______;②_______;
③_______;④_______。
(2)向稀釋后的溶液中逐滴加入0.1mol/L的鹽酸溶液,產生二氧化碳的體積(標準狀況)與所加鹽酸溶液的體積關系如圖所示。
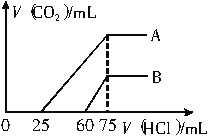
①A曲線表明,向原溶液中通入二氧化碳后,所得溶質與HCl反應產生二氧化碳的最大體積是_______mL(標準狀況)。
②B曲線表明,向原溶液中通入二氧化碳后,所得溶液中溶質的化學式為___________。
③原氫氧化鈉溶液中NaOH的物質的量濃度為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉晶體(Na2S2O3·5H2O,M=248 g·mol1)可用作定影劑、還原劑。回答下列問題:
(1)已知:Ksp(BaSO4)=1.1×1010,Ksp(BaS2O3)=4.1×105。市售硫代硫酸鈉中常含有硫酸根雜質,選用下列試劑設計實驗方案進行檢驗:
試劑:稀鹽酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
實驗步驟 | 現象 |
①取少量樣品,加入除氧蒸餾水 | ②固體完全溶解得無色澄清溶液 |
③___________ | ④___________,有刺激性氣體產生 |
⑤靜置,___________ | ⑥___________ |
(2)利用K2Cr2O7標準溶液定量測定硫代硫酸鈉的純度。測定步驟如下:
①溶液配制:稱取1.2000 g某硫代硫酸鈉晶體樣品,用新煮沸并冷卻的蒸餾水在__________中溶解,完全溶解后,全部轉移至100 mL的_________中,加蒸餾水至____________。
②滴定:取0.00950 mol·L1的K2Cr2O7標準溶液20.00 mL,硫酸酸化后加入過量KI,發生反應: Cr2O72+6I+14H+![]() 3I2+2Cr3++7H2O。然后用硫代硫酸鈉樣品溶液滴定至淡黃綠色,發生反應:I2+2S2O32
3I2+2Cr3++7H2O。然后用硫代硫酸鈉樣品溶液滴定至淡黃綠色,發生反應:I2+2S2O32![]() S4O62+2I。加入淀粉溶液作為指示劑,繼續滴定,當溶液__________,即為終點。平行滴定3次,樣品溶液的平均用量為24.80 mL,則樣品純度為_________%(保留1位小數)。
S4O62+2I。加入淀粉溶液作為指示劑,繼續滴定,當溶液__________,即為終點。平行滴定3次,樣品溶液的平均用量為24.80 mL,則樣品純度為_________%(保留1位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化工中把電解飽和食鹽水的工業生產叫氯堿工業,其生產流程如下:

除去食鹽水中的Ca2+、Mg2+、SO42—,應分別加入下列沉淀劑:①NaOH(aq)、
②Na2CO3(aq)、③BaCl2(aq),加入沉淀劑的順序為 (填序號);加入鹽酸的作用為 。
(2)下圖為實驗室電解飽和食鹽水的實驗裝置。X、Y均為石墨電極,兩極周圍溶液均滴有幾滴酚酞試液。

①電解一段時間后,X電極及附近溶液能觀察到的現象是 ;
Y電極上的電極反應式為 ,檢驗該極產生的氣體的方法是 。
②電解飽和食鹽水的離子方程式為 ;若飽和食鹽水體積為200mL,且忽略電解過程中的體積變化及氣體溶解,當兩極共收集到氣體(共兩種)44.8mL(標準狀況)時,溶液的pH= 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4 mol A氣體和2 mol B氣體在2 L的容器中混合并在一定條件下發生如下反應:2A(g)+B(g)2C(g)。若經2 s時測得C的濃度為0.6 mol·L-1,填寫下列空白:
(1)用物質A表示反應的平均速率為_________。
(2)用物質B表示反應的平均速率為_________。
(3)2 s時物質A的轉化率為_________。
(4)2 s時物質B的體積分數為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通過海水晾曬可得粗鹽,粗鹽除NaCl外,還含有MgCl2、CaCl2、Na2SO4以及泥沙等雜質。以下是制備精鹽的實驗方案,各步操作流程如下:
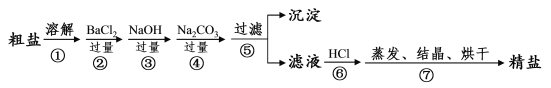
(1)在第①步粗鹽溶解操作中要用玻璃棒攪拌,作用是___。
(2)第②步操作的目的是除去粗鹽中的___(填化學式,下同),第⑥步操作的目的是除去濾液中___。
(3)第⑤步“過濾”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___、___(填化學式),寫出操作②和操作③的相關化學方程式___、___。
(4)在第③步操作中,選擇的除雜的試劑不能用KOH代替NaOH,理由是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵氮化合物(FexNy)在磁記錄材料領域有著廣泛的應用前景。某FexNy的制備需鐵、氮氣、丙酮和乙醇參與。
(1)Fe3+基態核外電子排布式為___。
(2)丙酮(CH3CCH3O)分子中碳原子軌道的雜化類型是__,1mol丙酮分子中含有σ鍵的數目為___。
(3)C、H、O三種元素的電負性由小到大的順序為____。
(4)乙醇的沸點高于丙酮,這是因為______。
(5)某FexNy的晶胞如圖1所示,Cu可以完全替代該晶體中a位置Fe或者b位置Fe,形成Cu替代型產物Fe(x-n)CunNy。FexNy轉化為兩種Cu替代型產物的能量變化如圖2所示,其中更穩定的Cu替代型產物的化學式為____。
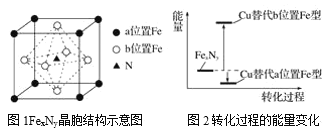
1-溴丙烷是一種重要的有機合成中間體,沸點為71℃,密度為1.36g·cm-3。實驗室制備少量1溴丙烷的主要步驟如下:步驟1:在儀器A中加入攪拌磁子、12g正丙醇及20 mL水,冰水冷卻下緩慢加入28mL濃H2SO4;冷卻至室溫,攪拌下加入24gNaBr。
步驟2:如圖所示搭建實驗裝置,緩慢加熱,直到無油狀物餾出為止。
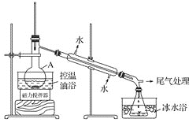
步驟3:將餾出液轉入分液漏斗,分出有機相。
步驟4:將分出的有機相轉入分液漏斗,依次用12mLH2O、12mL 5% Na2CO3溶液和12 mL H2O洗滌,分液,得粗產品,進一步提純得1溴丙烷。
(1)儀器A的名稱是___;加入攪拌磁子的目的是攪拌和___。
(2)反應時生成的主要有機副產物有2溴丙烷和____。
(3)步驟2中需向接受瓶內加入少量冰水并置于冰水浴中的目的是_____。
(4)步驟2中需緩慢加熱使反應和蒸餾平穩進行,目的是___。
(5)步驟4中用5%Na2CO3溶液洗滌有機相的操作:向分液漏斗中小心加入12 mL5%Na2CO3溶液,振蕩,___,靜置,分液。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com