
某校化學興趣小組為測定空氣中二氧化硫的含量,用NaOH溶液吸收SO2,反應的方程式如下:2NaOH+SO2═Na2SO4+H2O.用NaOH溶液吸收100L已除去CO2的空氣樣品,溶液質量增加了0.64g.已知此時空氣的密度為1.3g/L,求:
(1)被吸收的SO2的質量.
(2)發生反應的NaOH的質量.
(3)空氣中SO2的質量分數(計算結果精確到0.01%).
科目:初中化學 來源: 題型:計算題
合成氨工業生產中所用催化劑的主要成分是FeO和Fe2O3,且FeO與Fe2O3的質量比為9:20時,其催化活性最大.以Fe2O3為原料制備該催化劑時,可加入適量木炭粉,發生如下反應:2Fe2O3+C 4FeO+CO2↑.試計算應向160gFe2O3粉末中加入木炭粉的質量.
4FeO+CO2↑.試計算應向160gFe2O3粉末中加入木炭粉的質量.
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
某化學興趣小組為測定一種石灰石樣品中碳酸鈣的質量分數,進行如下實驗:
①稱取25.0g石灰石樣品,平均分成兩份,并分別加工成塊狀和粉末狀;
②將兩份樣品分別投入兩個錐形瓶中,各加入足量的相同溶質質量分數的稀鹽酸(樣品所含雜質不溶于水也不與酸反應),測得生成二氧化碳的質量與反應時間的關系如圖所示。請回答: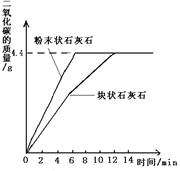
(1)由圖中曲線分析得出,影響該化學反應速率的因素是: ;請另外舉出—個生活或生產中控制化學反應速率的實例: 。
(2)每份樣品充分反應后.生成二氧化碳的質量為 .
(3)若每份樣品中加入l00.0g稀鹽酸,恰好完全反應,求反應后所得溶液中溶質的質量分數。(要求寫出計算過程.不考慮水、氯化氫的逸出.結果精確到0.1%)
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
在一燒杯中盛有24.3g Na2SO4和NaCl組成的固體混合物,加入100g水使Na2SO4和NaCl全部溶解。向其中逐漸滴加溶質質分數為20%的氯化鋇溶液,生成沉淀的總質量與所滴入氯化鋇溶液的質量關系曲線如圖所示。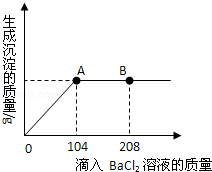
(1)請分析當BaCl2溶液滴加到B點時,溶液中的溶質是 。
(2)請計算當滴加BaCl2溶液至圖中A點時,所得溶液的溶質質量分數(計算結果保留一位小數)。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
甘肅祁連山水泥廠是我省規模較大的水泥廠,該廠的化驗室為了測定某礦山石灰石中碳酸鈣的質量分數,取石灰石樣品與足量的10%的稀鹽酸在燒杯中反應(假設石灰石樣品中雜質不與稀鹽酸反應也不溶于水).有關實驗數據如下表:
| | 反應前 | 反應后 | |
| 實驗數據 | 燒杯和稀鹽酸的質量 | 石灰石樣品的質量 | 燒杯和其中混合物的質量 |
| 134.4g | 10g | 141.1g |
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
現有一定質量含有少量泥沙等不溶性雜質和少量Na2SO4,MgCl2,CaCl2等可溶性雜質的粗鹽樣品,某實驗小組利用化學實驗室常用儀器對粗鹽樣品進行提純,提純步驟如下: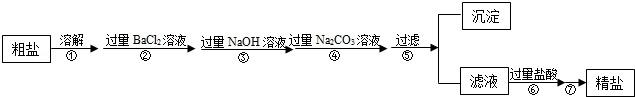
請根據提純步驟回答下列問題.
(1)步驟⑦的操作名稱為 .
(2)請寫出實驗步驟②中所涉及的化學方程式 .
(3)步驟⑥中加入過量鹽酸的目的是 .
(4)步驟②和步驟④ (填“可以”或“不可以”)顛倒,理由是 .
(5)檢驗步驟④中Na2CO3溶液已過量的方法是 .
(6)加碘食鹽相關信息如圖所示.
食鹽中的碘酸鉀(KIO3)在酸性條件下,可以將碘化鉀(KI)變成碘(I2),化學方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向裝有碘化鉀和淀粉混合液的試管中,滴入稀鹽酸將溶液酸化,再加入食鹽,若食鹽中有碘化鉀,則加入食鹽后的實驗現象 .
②小強同學欲測定加碘鹽中碘元素的質量分數,實驗步驟如下:取10g食鹽樣品于試管中加水溶解,加入過量KI的和淀粉混合溶液,再滴入稀鹽酸將溶液酸化使其充分反應后,調節溶液呈中性,再向試管中滴加硫代硫酸鈉溶液(Na2S2O3),發生化學反應方程式為:2Na2S2O3+I2═Na2S4O6+2NaI
當加入質量分數為0.237%Na2S2O3溶液2g時,I2恰好反應完全,通過計算判斷該食鹽樣品是否合格(已知Na2S2O3的相對分子質量為158.請寫出計算過程).
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
工業上侯氏制堿法得到的純堿產品中常含有少量的氯化鈉雜質,化驗員要對每批次的純堿產品進行檢驗.在實驗室中取27g純堿樣品,平均分成五份依次加入到盛有100g稀鹽酸的錐形瓶中(錐形瓶的質量為60g),每次充分反應后都進行稱量,得到的實驗數據如下表: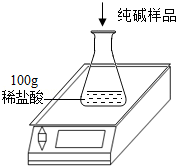
| | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入純堿樣品的質量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 電子天平的示數/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
在工業上用純堿和石灰石為原料制備燒堿,主要流程如圖所示: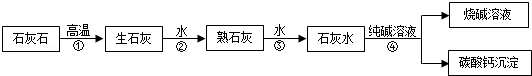
(1)在①﹣④四個過程中,發生了分解反應的是 (填序號).
(2)檢驗燒堿溶液中含有少量Na2CO3的具體方法是 .
(3)在室溫下,將53g質量分數為10%的Na2CO3溶液與3000g澄清石灰水充分混合,恰好完全反應.則這時所得NaOH溶液的質量是多少?(計算結果精確至0.1g)
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
某校化學興趣小組的同學為了制取氫氧化鎂,他們取9.5gl氯化鎂固體全部溶解在40.5g水中制成不飽和溶液,然后向其中加入55.8g某溶質質量分數的氫氧化鈉溶液恰好完全應.請你幫他們計算該小組制得的氫氧化鎂的質量和反應所得溶液中溶質的質量分數.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com