
【題目】2018年10月28日,國人為之驕傲的第一艘001A型國產航母第三次海試,標志著我國在航海及軍事領域取得重大突破。請運用所學知識填空:
(1)合金是航母的主體材料,如鋁合金,以其質輕、硬度大、極強的抗腐蝕性能在航母制造中備受青睞。常溫下,鋁具有很強抗腐蝕性的原因是_____。
(2)航母的外殼用涂料覆蓋是為了防止鋼鐵材料與_____接觸而生銹。
(3)建造航母用到鈦合金。工業制鈦過程中有一個反應的化學方程式為TiF4+2H2SO4![]() 4HF+2X+TiO2,則X的化學式為_____。
4HF+2X+TiO2,則X的化學式為_____。
【答案】通常情況下,鋁能和空氣中的氧氣反應生成致密的氧化鋁保護膜 水和氧氣 SO3
【解析】
(1)常溫下,單質鋁在空氣中不容易被銹蝕的原因是:通常情況下,鋁能和空氣中的氧氣反應生成致密的氧化鋁保護膜。故填:通常情況下,鋁能和空氣中的氧氣反應生成致密的氧化鋁保護膜。
(2)航母的外殼用涂料覆蓋是為了防止鋼鐵材料與水和氧氣接觸而生銹。故填:水和氧氣。
(3)由TiF4+2H2SO4![]() 4HF+2X+TiO2可知,反應前后鈦原子都是1個,氟原子都是4個,氫原子都是4個,反應前硫原子是2個,反應后應該是2個,包含在2X中,反應前氧原子是8個,反應后應該是8個,其中6個包含在2X中,因此X的化學式為SO3。
4HF+2X+TiO2可知,反應前后鈦原子都是1個,氟原子都是4個,氫原子都是4個,反應前硫原子是2個,反應后應該是2個,包含在2X中,反應前氧原子是8個,反應后應該是8個,其中6個包含在2X中,因此X的化學式為SO3。
故填:SO3。


 考前必練系列答案
考前必練系列答案科目:初中化學 來源: 題型:
【題目】(5分)A、B、C、D、E為初中化學常見的五種物質,它們之間存在如圖所示的關系(“→”表示物質經一步反應可轉化為另一種物質,“—”表示相連兩物質能發生化學反應,部分反應物、生成物及反應條件已略去)。請回答下列問題:
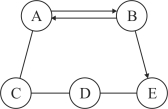
(1)若A、B為組成元素相同的氣體,E為大理石的主要成分,則B的化學式為 ,物
質D的類別為 (填“酸”、“堿”、“鹽”或“氧化物”)。
(2)若A是能供給人類呼吸的氣體,B是一種最常用的溶劑,D的水溶液顯藍色。
則C—D反應的基本類型是 ,
D—E反應的化學方程式是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】正確寫出化學用語。
(1)兩個氫原子___;
(2)氧分子___;
(3)寫出氯化鐵的化學式并標出鐵元素的化合價___;
(4)有水生成的分解反應___.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】明明同學利用實驗室存放的一瓶氫氧化鈉固體配制溶液做酸堿中和實驗。
(1)已知:水的密度為1.0g/mL。實驗室配制100g溶質質量分數為5%的氫氧化鈉溶液,需要稱取氫氧化鈉5g,需要量取水________mL。量取時的操作如右圖所示,該操作對所配制溶液溶質質量分數的影響是________________。

(2)明明用配制的氫氧化鈉溶液做中和反應實驗,發現有氣泡產生。于是明明判斷氫氧化鈉變質了。請用化學方程式說明氫氧化鈉變質、滴加鹽酸產生氣泡的原因______________。
(3)為探究氫氧化鈉是否完全變質,明明設計了兩個實驗方案。
方案1:取少量上述氫氧化鈉溶液樣品,滴加幾滴酚酞溶液,溶液變成紅色
方案2:取少量上述氫氧化鈉溶液樣品,加入飽和石灰水,靜置,取上層清液,滴加幾滴酚酞溶液。發現溶紅色。
于是明明認為樣品中還會有氫氧化鈉,沒有完全變質。
①康康認為明明的兩個實驗方案都不能達到目的,他的理由是_________________。
②請你設計一個方案來驗證氫氧化鈉是否完全變質。_____________________
(4)康康將方案2進行了定量化處理,來檢測氫氧化鈉固體的變質程度。取10g樣品溶于90g水中,向其中滴加過量飽和石灰水,對沉淀過濾洗滌、烘干后稱量為0.5g。則樣品中氫氧化鈉的質量分數是_____________?
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水是重要的物質,在實驗室中常用于溶解物質、配制溶液.
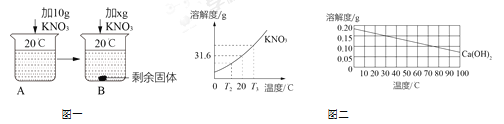
(1)向50g水中溶解一定量KNO3固體的操作如下,請根據如圖一實驗現象及溶解度曲線回答:當x=__________g時,B中恰好沒有固體剩余;
(2)某同學從一瓶久置的氫氧化鈣固體(溶解度曲線如圖二所示)樣品中取出0.2g,加入到30℃時100g水中,充分溶解后過濾,稱得剩余固體0.08g.請你判斷:濾液為__________(選填“飽和”或“不飽和”).
(3)若硝酸鉀中混有少量的氫氧化鈣,可以采取__________的方法提純硝酸鉀.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】酸、堿、鹽是幾類重要的化合物。
(1)打開盛有濃鹽酸和濃硫酸的試劑瓶蓋,立即就能把它們區分開來的原因是_____。
(2)100 g質量分數為10%的稀硫酸和100 g質量分數為10%的氫氧化鈉溶液充分反應后,溶液的pH_____7(填“大于”“小于”或“等于”)。
(3)在“創新實驗裝置”的競賽中,某化學興趣小組的同學設計了如圖所示的裝置。
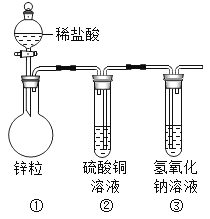
①寫出裝置甲中發生反應的化學方程式_____。
②丙裝置中會出現什么現象_____。
(4)某同學為了除去NaCl溶液中CaCl2、MgCl2、Na2SO4雜質制取精鹽,制作流程如圖所示:[提示:Mg(OH)2、BaSO4、BaCO3難溶于水]
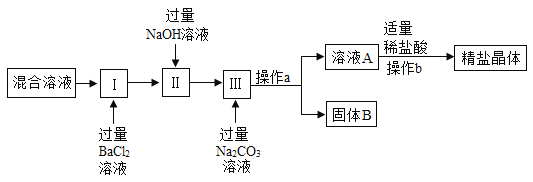
①寫出第I步中加入過量BaCl2溶液所發生反應的化學方程式_____。
②操作a的名稱為_____。
③通過操作a所得溶液A中除氯化鈉外,還含有的溶質有哪些_____?
(5)向20 g含有氯化鈉雜質的碳酸鈉固體中加入100 g稀鹽酸,恰好完全反應,得到115.6g不飽和溶液。求所用稀鹽酸的溶質質量分數_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】自來水廠凈水過程的主要操作流程如圖.
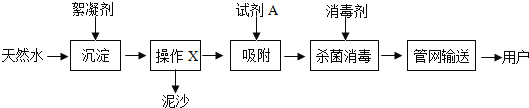
資料:常用的絮凝劑有明礬[KAl(SO4)12H2O],消毒劑有液氯(Cl2)
回答下列問題:
(1)操作X的名稱是____,試劑A的名稱是____。
(2)明礬作絮凝劑是因為與水反應生成氫氧化鋁膠狀物.氫氧化鋁的化學式為____.液氯與水中雜質反應生成一些對人體有害的物質,例如三氯甲烷(CHCl3).三氯甲烷屬于____(填“有機物”或“無機物”)
(3)高鐵酸鉀(K2FeO4)能作消毒劑與絮凝劑.它殺菌時會生成氫氧化鐵膠狀物.高鐵酸鉀中鐵元素的化合價是____.
(4)自來水廠的凈水過程____(填“能”或“不能”)將硬水軟化成軟水.生活中將硬水軟化的方法是____,經過此法后,水中的部分Ca2+、Mg2+轉化為沉淀,即通常所說的水垢,水垢的主要成分為____.
(5)自來水中通常都含有Cl﹣,可以在水樣中滴加少量稀硝酸和____檢驗,若出現____現象,說明水中含有Cl﹣.
(6)實驗室用自來水制取蒸餾水的蒸餾燒瓶里,通常要加入幾粒沸石或碎瓷片,作用是____
(7)電解氫氧化鈉稀溶液與電解水的原理均可表示為:2H2O![]() 2H2↑+O2↑。電解一定質量氫氧化鈉稀溶液的過程中,下列說法正確的是_____
2H2↑+O2↑。電解一定質量氫氧化鈉稀溶液的過程中,下列說法正確的是_____
A 溶液中鈉元素質量變大 B 溶液中氫、氧元素質量比不變
C 溶液中氫元素質量分數減小 D 溶液的pH減小
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】“雙吸劑”是一種常見袋裝食品的保鮮劑,能吸收空氣中的氧氣、二氧化碳、水蒸氣等。化學興趣小組的同學在某食品袋中發現一包“雙吸劑”,其標簽如圖所示。同學們對這包久置的“雙吸劑”固體樣品很好奇,設計實驗進行探究。

(提出問題)久置“雙吸劑”固體的成分是什么?
(查閱資料)
鐵與氯化鐵溶液在常溫下發生反應生成氯化亞鐵:Fe+2FeCl3═3FeCl2。
(作出猜想)久置固體中一定有活性炭可能含有及________________。
(實驗探究)下表是小組同學設計的實驗方案和記錄的實驗報告,請你補充完整:
實驗操作 | 實驗現象 | 實驗結論 |
①取3g固體樣品仔細觀察,用磁鐵吸固體,置于燒杯中,加20 mL水,用溫度計測量溶解前后液體溫度,過濾,所得濾液備用。 | 固體樣品中有黑色粉末, 較多白色固體及少量紅棕色固體,少量黑色粉末可以被磁 鐵吸引,溫度計溫度無明顯變化,得到無色濾液 | 樣品中____________ |
②取少量①中無色濾液,滴加無色酚酞。 | 溶液有無色變為紅色 | 樣品中一定含Ca(OH)2 |
③取少量固體樣品放入試管 中,加適量的試劑Y,用帶導管的單孔橡皮塞塞緊試管口,導管另一端伸入澄清石灰水中。 | 試管中固體逐漸減少,有大量無色氣體產生,得到淺綠色溶液,有少量黑色固體不溶,澄清的石灰水變渾濁。 | 樣品中含有活性炭、CaCO3 |
(實驗釋疑)確定了久置“雙吸劑”固體的成分后,幾位同學又提出了以下問題:
Ⅰ步驟③中加入試劑 Y 后,溶液卻不呈黃色的原因是_______________。
Ⅱ查閱資料得知,鐵粉作脫氧劑時,為了達到更好的脫氧效果,會向其中加入少量的氯化鈉。請設計實驗說明氯化鈉存在時鐵粉脫氧效果更好:__________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com