
【題目】下表是氯化鈉、硝酸鉀在不同溫度時的溶解度。據此判斷:下列說法不正確的是( )
溫度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | 氯化鈉 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
硝酸鉀 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
A.氯化鈉和硝酸鉀的溶解度曲線在20℃~30℃溫度范圍內會相交
B.在20℃時, 向68g飽和氯化鈉溶液中加入32g水,此時溶液中溶質的質量分數為18%
C.從含有少量氯化鈉的飽和硝酸鉀溶液中得到較多的硝酸鉀晶體,可采用冷卻熱飽和溶液使其結晶的方法
D.分別將20℃時一定質量的飽和氯化鈉溶液、飽和硝酸鉀溶液升溫至40℃,此時硝酸鉀溶液中溶質的質量分數大于氯化鈉溶液
【答案】D
【解析】A、氯化鈉和硝酸鉀的溶解度在20℃~30℃溫度范圍內分別從36g--36.3g、31.6g--45.8g,所以曲線會相交,A不符合題意;
B、在20℃時,氯化鈉的溶解度是36g,所以68g的變化溶液中含有氯化鈉18g,所以向68g飽和氯化鈉溶液中加入32g水,此時溶液中溶質的質量分數為 ![]() ×100%=18%,B不符合題意;
×100%=18%,B不符合題意;
C、硝酸鉀的溶解度隨溫度的升高而增大,所以從含有少量氯化鈉的飽和硝酸鉀溶液中得到較多的硝酸鉀晶體,通常可采用冷卻熱飽和溶液使其結晶的方法,C不符合題意;
D、升高溫度,氯化鈉、硝酸鉀的溶解度增大,20℃時的飽和氯化鈉溶液的溶質質量分數大于飽和硝酸鉀溶液的溶質質量分數,所以分別將20℃時的飽和氯化鈉溶液、飽和硝酸鉀溶液升溫至40℃,飽和氯化鈉溶液的溶質質量分數仍大于飽和硝酸鉀溶液的溶質質量分數,D符合題意。
故答案為:D,
在溶解度曲線中,某點的定義是考試重點;根據圖像比較溶解度的大小:溫度相同,點高溶大,相交點表示物質溶解度相等。當雜質的溶解度隨溫度變化較大是,采用蒸發結晶,當雜質溶解度隨溫度變化較小時,冷卻熱飽和溶液結晶。


科目:初中化學 來源: 題型:
【題目】黃銅是Cu—Zn合金,為測定其中Zn的質量分數,某學習小組精確稱取0.50 g合金樣品,設計了如下裝置并進行實驗:已知:H2的密度近似為0.090 g·L—1。
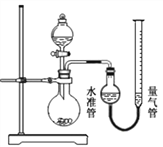
【實驗步驟】:
①______;②裝入藥品和水,連接裝置;③記錄量氣管中水面讀數為5 mL;④打開分液漏斗活塞,逐滴滴入稀硫酸溶液,至不再產生氣泡為止,關閉活塞;⑤待溫度降至室溫時,記錄量氣管中水面讀數為49 mL;⑥處理剩余藥品,整理實驗臺。
【實驗分析及數據處理】:
(1)完善實驗步驟中的所缺部分__________________;
(2)檢查氣密性的方法:打開分液漏斗活塞,向量氣管中加入水,使水準管和量氣管中水面相平,關閉活塞,降低量氣管,若兩側水面高度差_____(填“改變”或“不變”),則氣密性良好;
(3)為了準確地測量氫氣體積,在讀取量氣管中液面讀數的過程中,應注意_______(填字母編號)。
A.讀數時視線與凹液面最低處相平
B.讀數前應上下移動水準管,待兩管液面相平再讀數
C.保持水準管靜止,待水準管中液面不再上升時再讀數
(4)計算此Cu—Zn合金樣品中Zn的質量分數(3分,精確到小數點后3位); ________________;
【實驗反思】:
(5)造成實驗結果偏大的原因可能是______。
A.實驗過程加入NaOH溶液的體積 B.沒有冷卻至室溫就開始讀數
C.裝置漏氣
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】四種物質在一定的條件下充分混合反應,測得反應前后各物質的質量分數如圖所示.則有關說法中不正確的( )

A.丁一定是化合物
B.乙可能是這個反應的催化劑
C.生成的甲、丙兩物質的質量比為8: 1
D.參加反應的丁的質量一定等于生成甲和丙的質量之和
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】含有較多_______________________________的水叫硬水,_______________________________叫軟水。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水是一切生命體生存所必需的物質,凈化水時加入_________可以除去水中的異味和色素;生活中降低水的硬度常用的方法是_______;電解水實驗證明了水由氫元素和氧元素組成的理論依據是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】有關物質組成及化學規律的發現對化學的發展做出了重要貢獻。
(1)法國化學家拉瓦錫為化學學科的發展做出了巨大貢獻,下列有關發現與他有密切關系的是。
A. 空氣的組成 B. 質量守恒定律 C. 水的組成 D. 酸堿指示劑
(2)在密閉容器內加入下列兩種物質,并稱量加入前后的總質量(含密閉容器),能驗證質量守恒定律的是 (填標號)。
A.蔗糖和水
B.氯化鈉溶液和硝酸鉀溶液
C.氯化鋇溶液和稀硫酸
(3)在氧氣中點燃紅磷的實驗過程,固體質量變化如圖所示。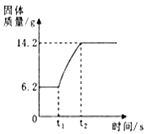
①從燃燒條件分析,固體質量在t1前沒有發生變化的原因是。
②該反應的化學方程式為。
③參加反應的氧氣質量為g。
(4)某學習小組擬在實驗室里利用空氣和鎂粉為原料制取少量氮化鎂(Mg3N2)。
查閱資料可知Mg、Mg3N2能發生如下反應:
①2Mg+O2 ![]() 2MgO; ②3Mg+N2
2MgO; ②3Mg+N2 ![]() Mg3N2; ③2Mg+CO2
Mg3N2; ③2Mg+CO2 ![]() 2MgO+C
2MgO+C
④Mg+H2O ![]() MgO+H2↑ ⑤Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
MgO+H2↑ ⑤Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
實驗中所用的裝置和藥品如圖所示(鎂粉、還原鐵粉均已干燥,裝置內所發生的反應是完全的,整套裝置的末端與干燥管相連)。回答下列問題: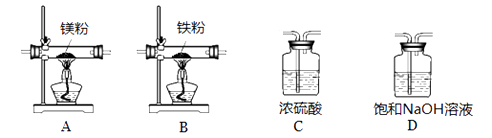
①連接并檢查實驗裝置的氣密性,實驗開始時,將空氣通入實驗裝置,則氣流流經裝置的順序是(填裝置序號)。D裝置中發生反應的化學方程式為
②通氣后,如果同時點燃A、B裝置的酒精燈,對實驗結果有何影響?。
③設計一個實驗,驗證產物是否含氮化鎂:
實驗操作和實驗現象 | 實驗結論 |
產物中含有氮化鎂 |
④思維拓展:空氣中N2的含量遠大于O2的含量,而鎂條在空氣中燃燒生成的MgO的質量卻遠大于Mg3N的質量,請給出合理的解釋。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】從硫化氫的化學式H2S獲得的下列認識中,錯誤的是
A.硫化氫屬于化合物
B.硫化氫由氫、硫兩種元素組成
C.硫化氫中氫、硫元素質量比為1:16
D.硫酸(H2SO4)中含有硫化氫(H2S)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com