
某化學興趣小組對一包干燥的紅色粉末組成進行探究,該紅色粉末可能由Cu 、Fe2O3兩種固體中的一種或兩種組成。
【提出猜想】紅色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查閱資料】(1)白色無水CuSO4遇水變藍
(2)Cu在FeCl3溶液中發生反應:2FeCl3+Cu=2FeCl2+CuCl2
【實驗探究】
[甲組同學]:定性檢測該紅色粉末的物質組成
(1)小云取少量紅色粉末于試管中,滴加足量稀鹽酸,充分振蕩后觀察,發現固體全部溶解,得有色溶液。則猜想 一定不成立,其中一定發生反應的化學方程式為 。
(2)小偉向小云得到的有色溶液中插入一根潔凈的鐵絲,反應充分后,觀察到
現象,得出猜想③成立。
[乙組同學]:定量測定該紅色粉末中氧化鐵的質量分數
實驗步驟:小晨稱取該紅色粉末5.0g裝入硬質玻璃管中,按下圖進行實驗。開始時緩緩通入CO氣體,過一段時間后再高溫加熱使其充分反應。待反應完全后,停止加熱,仍繼續通CO氣體直至玻璃管冷卻。反應前后稱量相關物質的總質量(裝置內空氣中的水蒸氣、CO2忽略不計),其數據如下表:
| | 反應前 | 反應后 |
| Ⅰ 組 | 玻璃管和紅色粉末的總質量為48.3 g | 玻璃管和固體物質的總質量為47.1 g |
| Ⅱ 組 | 洗氣瓶和瓶中所盛物質的總質量為258.6 g | 洗氣瓶和瓶中所盛物質的總質量為261.9 g |
 學業測評一課一測系列答案
學業測評一課一測系列答案科目:初中化學 來源: 題型:計算題
相同質量的M、N兩種活潑金屬,分別與足量的稀鹽酸在室溫下發生反應(M、N在生成物中的化合價均為+2價),生成H2的質量m和反應時間t的關系如圖所示。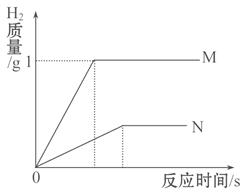
(1)金屬活動性順序是M比N________(填“強”或“弱”);相對原子質量是M比N的________(填“大”或“小”)。
(2)M與稀鹽酸反應結束后,消耗稀鹽酸中溶質的質量為________g。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
向碳酸鈉和氯化鈉的混合物15.6 g中加入100 g稀鹽酸,恰好完全反應后,得到111.2 g溶液。試計算:
(1)產生二氧化碳多少克?
(2)所得溶液中溶質的質量分數是多少?
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
某興趣小組為探究“氧化鐵和銅粉”混合物中銅的質量分數,稱取一定質量的混合物,按照下圖實驗裝置進行實驗: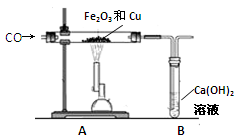
(1)實驗時要“先通一氧化碳氣體,后加熱” 的目的是 。
(2)裝置A中發生反應的方程式為 。
(3)實驗裝置B中的現象是 ,發生反應的化學方程式為 。
(4)該裝置的設計有一明顯不當之處,你的改進方案是 。
[定量分析]
該興趣小組按照科學的方案完成實驗后,對充分反應后的管內固體X進行如下后續實驗探究: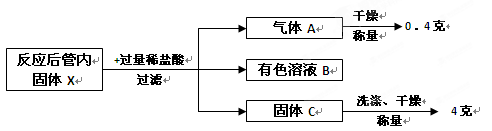
回答下列問題:
(1)寫出固體X與稀鹽酸反應的方程式: 。
(2)有色溶液B中含有的溶質: (填化學式)。
(3)根據以上實驗流程,計算原混合物“氧化鐵和銅粉”中銅的質量分數為 。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
將50g木炭粉與氧化銅組成的黑色固體混合物放入試管中高溫加熱,待反應完成后,冷卻稱得剩余固體的質量為39g。試通過計算確定剩余的39g固體的組成。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
已知燒杯中裝有200g硫酸和硫酸鋅混合溶液,其中含硫酸鋅12.1g.向燒杯中逐漸加入鋅粒,放出氣體質量與加入鋅粒質量的關系如圖所示.當恰好完全反應時,所得的溶液為不飽和溶液.請計算:
(1)m=_________(2)原混合溶液中H2SO4的質量分數為_________.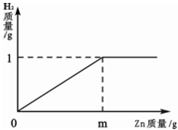
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
某同學對某地工業廢水(含有硫酸和鹽酸)中的H2SO4進行測定.取50g該廢水于燒杯中,加入足量的BaCl2溶液,充分反應中,過濾、洗滌、干燥得到BaSO4固體11.65g.通過計算回答下列問題:
(1)50g該廢水中H2SO4的質量
(2)若改用KOH溶液來測定50g該廢水中H2SO4的含量,結果會 (填“偏高”、“偏低”、“不變”),理由是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com