
氮及其化合物與我們的吃、穿、住、行、健康等都有著密切的聯系,也是高中化學學習中重要的一部分。請回答下列問題:
I.(1)現有一支15mL的試管,充滿NO倒置于水槽中,向試管中緩緩通入一定量氧氣,當試管內液面穩定時,剩余氣體3mL。則通入氧氣的體積可能為 。
 (2)一定條件下,某密閉容器中發生反應:4NH3(g)+5O2(g)
4NO(g)+6H2O(g)。
(2)一定條件下,某密閉容器中發生反應:4NH3(g)+5O2(g)
4NO(g)+6H2O(g)。
|
起始濃度( mol/L) |
C(NH3) |
C(O2) |
C(NO) |
C(H2O) |
|
甲 |
1 |
2 |
0 |
0 |
|
乙 |
4 |
8 |
0 |
0 |
|
丙 |
0.2 |
x |
y |
z |
①恒溫恒容下,平衡時NH3的轉化率甲 乙。(填“>”、“=”、或“<”)
②恒溫恒容下,若要使丙與甲平衡時各組分濃度相同,則x= ,y= ,z= .
(3)向容積相同、溫度分別為T1和T2的兩個密閉容器中分別充入等量NO2,發生反應:2NO2(g) N2O4(g)△H<0。恒溫恒容下反應相同時間后,分別測定體系中NO2的百分含量分別為a1和a2;已知T1< T2,則a1_
a2。
N2O4(g)△H<0。恒溫恒容下反應相同時間后,分別測定體系中NO2的百分含量分別為a1和a2;已知T1< T2,則a1_
a2。
A.大于 B.小于 C.等于 D.以上都有可能
(4)2.24L(標準狀況)氨氣被200 mL l mol/L HNO3溶液吸收后,反應后溶液中的離子濃度關系是 。
Ⅱ.三氟化氮(NF3)是一種新型的電子材料,它在潮濕的空氣中與水蒸氣能發生氧化還原反應,其生成物有HF、 NO、 HNO3。根據要求回答下列問題:
(1)寫出該反應的化學方程式: 。反應過程中,氧化劑和還原劑物質的量之比為 。
(2)若反應中生成0.2mol HNO3,轉移的電子數目為 。
14分)Ⅰ.(10分)(1)9mL和14.25mL(2分)
(2)① >(1分) ② 1,0.8,1.2(各1分)
(3)D(2分)
(4)c(NO-3)>c(H+)>c(NH+4)>c(OH-)(2分)
Ⅱ . (4分)
(1)3NF3+5H2O=9HF+2NO+HNO3 (2分) 2:1 (1分)
(2)2.408×1023 或0.4NA (1分)(寫成物質的是不給分)
【解析】
試題分析:I.(1)4NO+3O2+2H2O=4HNO3,剩余氣體3mL,過量氣體可能是O2或NO,若是O2過量,NO全部參加反應,根據4NO~3O2,V(O2)= 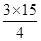 +3=14.25mL,若是NO過量,參加反應的NO為12ml,根據4NO~3O2,V(O2)=
+3=14.25mL,若是NO過量,參加反應的NO為12ml,根據4NO~3O2,V(O2)=  =9mL;
=9mL;
(2)①恒溫恒容,乙中投料是甲中投料的4倍,等同于增大壓強,平衡逆向移動,因此甲>乙;
②根據等效平衡可知,丙中轉化為起始量與甲中的起始量相同,則
4NH3(g)+5O2g)⇌4NO(g)+6H2O(g),
起始1 2
丙 0.2 x y z
則0.2+y=1, x + y =2
z =
y =2
z =  y
y
解得y =0.8,x=1,z=1.2;
(3)恒溫恒容下反應相同時間,T1<T2,兩個密閉容器中分別充入等量NO2,在T1下,達到平衡時,所用時間為t1,在T2時,在t1時間時已達到平衡,因為升高溫度,平衡逆向移動,所以a1>a2,選擇時間小于t1,在相同時間內,在T2時,尚未達到平衡,反應正向移動,則有a1小于或等于a2,故答案為:D;
(4)2.24L(標準狀況)氨氣被200 mL l mol/L HNO3溶液吸收后,得到硝酸銨和硝酸的混合溶液,且二者物質的量相等,二者中都含有NO3-,它濃度最大,NH4+水解,因此C(H+)>C(NH4+),C(OH-)最小,c(NO-3)>c(H+)>c(NH+4)>c(OH-);
Ⅱ.3NF3+5H2O=9HF+2NO+HNO3,NF3既是氧化劑又是還原劑,其中N化合價是+3價,體現氧化性有2mol降到+2價,體現還原性有1mol升到+5價,氧化劑和還原劑物質的量之比為2:1,反應中每有1mol硝酸生成,轉移電子2mol, 若反應中生成0.2mol HNO3,轉移的電子數目為0.4NA。
考點:考查化學反應原理、鹽的水解、氧化還原反應、方程式的書寫


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:閱讀理解
| 起始濃度(mol. L-1) | c( NH3) | c( O2) | c( NO) | c( H20) |
| 甲 | 1 | 2 | 0 | 0 |
| 乙 | 2 | 4 | 0 | 0 |
| 丙 | 0.5 | x | y | z |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 起始濃度(mol. L-1) | c( NH3) | c( O2) | c( NO) | c( H20) |
| 甲 | 1 | 2 | 0 | 0 |
| 乙 | 2 | 4 | 0 | 0 |
| 丙 | 0.5 | x | y | z |
查看答案和解析>>
科目:高中化學 來源:江西省模擬題 題型:填空題
 4NO(g)+6H2O(g)
4NO(g)+6H2O(g) 
 N2O4(g) △H<0。恒溫恒容下反應相同時間后,分別測定體系中NO2的百分含量分別為a1和
N2O4(g) △H<0。恒溫恒容下反應相同時間后,分別測定體系中NO2的百分含量分別為a1和查看答案和解析>>
科目:高中化學 來源:模擬題 題型:填空題
 4NO(g)+6H2O(g)
4NO(g)+6H2O(g) 
 N2O4(g) △H<0。恒溫恒容下反應相同時間后,分別測定體系中NO2的百分含量分別為a1和
N2O4(g) △H<0。恒溫恒容下反應相同時間后,分別測定體系中NO2的百分含量分別為a1和查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com