
(16分)碳及其化合物與人類生產(chǎn)、生活密切相關(guān)。請(qǐng)回答下列問題:
(1)在化工生產(chǎn)過程中,少量CO的存在會(huì)引起催化劑中毒。為了防止催化劑中毒,常用SO2將CO氧化SO2被還原為S。
已知: C(s)+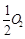 (g)=CO(g)ΔH1=-126.4kJ/mol ①
(g)=CO(g)ΔH1=-126.4kJ/mol ①
C(s)+O2(g)=CO2(g) ΔH2= -393.5kJ·mol-1 ②
S(s)+O2(g)=SO2(g) ΔH3= -296.8kJ·mol-1 ③
則SO2氧化CO的熱化學(xué)反應(yīng)方程式:
(2)CO可用于合成甲醇,反應(yīng)方程式為CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。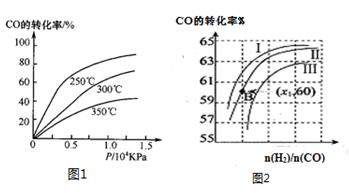
①CO在不同溫度下的平衡轉(zhuǎn)化率與壓強(qiáng)的關(guān)系如圖1所示,該反應(yīng)ΔH 0(填“>”或“ <”)。
圖2表示CO的轉(zhuǎn)化率與起始投料比[ n(H2)/n(CO)]、溫度的變化關(guān)系,曲線I、II、III對(duì)應(yīng)的平衡常數(shù)分別為K1、K2、K3,則K1、K2、K3的大小關(guān)系為 ;測(cè)得B(X1,60)點(diǎn)氫氣的轉(zhuǎn)化率為40%,則x1= 。
②在恒容密閉容器里按體積比為1:2充入一氧化碳和氫氣,一定條件下反應(yīng)達(dá)到平衡狀態(tài)。當(dāng)改變反應(yīng)的某一個(gè)條件后,下列變化能說明平衡一定向正反應(yīng)方向移動(dòng)的是 (填序號(hào))。
| A.正反應(yīng)速率先增大后減小 | B.逆反應(yīng)速率先增大后減小 |
| C.化學(xué)平衡常數(shù)K值增大 | D.反應(yīng)物的體積百分含量增大 |
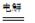 CH3CHOH+CH3CHOOH。
CH3CHOH+CH3CHOOH。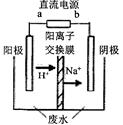
(16分)
(1) SO2(g)+2CO(g)=S(s)+2CO2(g) ΔH=-237.4kJ·mol-1(3分)
(2)①<(1分) K1>K2>K3(2分) 3 (2分)
②A C (2分) ③4.5 L2·mol-2 (不帶單位不扣分)(2分)
(3)①CH3CHO-2e-+H2O═CH3COOH+2H+ (2分) ②0.19(2分)
解析試題分析:(1)根據(jù)蓋斯定律得,目標(biāo)方程式=②×2-①×2-③,ΔH=(-393.5kJ·mol-1)×2-(-126.4kJ/mol)×2-(-296.8kJ·mol-1)=-237.4kJ·mol-1,所以所求熱化學(xué)方程式為SO2(g)+2CO(g)=S(s)+2CO2(g) ΔH=-237.4kJ·mol-1;
(2)①由圖1可知,溫度升高CO的轉(zhuǎn)化率降低,說明升高溫度,平衡逆向移動(dòng),正向是放熱反應(yīng),ΔH<0;n(H2)/n(CO)一定時(shí),CO的轉(zhuǎn)化率Ⅰ>Ⅱ>Ⅲ,轉(zhuǎn)化率高的平衡常數(shù)大,所以K1、K2、K3的大小關(guān)系為K1>K2>K3測(cè)得B(X1,60)點(diǎn)氫氣的轉(zhuǎn)化率為40%,CO的轉(zhuǎn)化率是60%,設(shè)B點(diǎn)時(shí)CO、H2的物質(zhì)的量分別是m、n,可得60%m=40%n/2,所以n/m=3,即x1=3;
②A、增大反應(yīng)物濃度,正反應(yīng)速率先增大后減小,說明平衡正向移動(dòng),正確;B、增大生成物濃度,逆反應(yīng)速率先增大后減小,說明平衡逆向移動(dòng),錯(cuò)誤;C、降低溫度,K值增大,說明生成物濃度增大,反應(yīng)物濃度減小,平衡正向移動(dòng),正確;D、減小壓強(qiáng),平衡逆向移動(dòng),反應(yīng)物的體積百分含量增大,錯(cuò)誤;E、恒容條件時(shí)混合氣體的密度增大,說明容器中氣體質(zhì)量增加,可能是反應(yīng)物也可能是生成物,平衡移動(dòng)方向不確定,錯(cuò)誤,答案選AC;
③設(shè)平衡時(shí)CO的濃度是x,則氫氣的濃度是2x-1,生成甲醇的濃度是1-x,根據(jù)題意得:x/(2x-1)=2:1,x=2/3mol/L,所以K=(1-x)/x·(2x-1)2=4.5 L2·mol-2
(3)①陽極發(fā)生氧化反應(yīng),乙醛被氧化為乙酸,氫氧根離子被氧化為氧氣,則陰極發(fā)生還原反應(yīng),乙醛被還原為乙醇,同時(shí)氫離子被還原為氫氣,所以陽極電極反應(yīng)式除生成氧氣外,還有CH3CHO-2e-+H2O═CH3COOH+2H+
②陰極反應(yīng)是CH3CHO+2e-+2H+=CH3CH2OH,所以注入1m3乙醛的含量為300mg/L的廢水,陰極區(qū)乙醛的去除率可達(dá)60%,生成乙醇的質(zhì)量是1000L×300mg/L×60%×10-3g/mg÷44g/mol×46g/mol=188.2g=0.19kg。
考點(diǎn):考查蓋斯定律的應(yīng)用,化學(xué)平衡圖像的分析及平衡理論應(yīng)用,電化學(xué)原理的應(yīng)用



| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:填空題
、隨著人類對(duì)溫室效應(yīng)和資源短缺等問題的重視,如何降低大氣中CO2的含量及有效地開發(fā)利用CO2,引起了普遍的重視。
(1)目前工業(yè)上有一種方法是用CO2來生產(chǎn)甲醇:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
下圖表示該反應(yīng)進(jìn)行過程中能量(單位為kJ·mol-1)的變化。該反應(yīng)是 (填“吸熱”或“放熱”)反應(yīng)。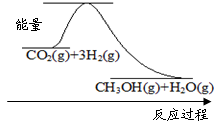
(2)某溫度下,若將6mol CO2和8 mol H2充入2L的密閉容器中,測(cè)得H2的物質(zhì)的量隨時(shí)間變化的曲線如下圖實(shí)線所示(圖中字母后的數(shù)字表示對(duì)應(yīng)的坐標(biāo))。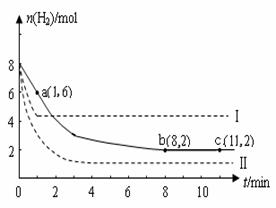
①在反應(yīng)進(jìn)行的0~1min內(nèi),該反應(yīng)的平均速率v(H2)= 。
②如果改變影響化學(xué)平衡的一個(gè)因素(如:溫度、濃度、壓強(qiáng)),反應(yīng)將向著能夠減弱這種改變的方向進(jìn)行(如增大H2的濃度,反應(yīng)向右進(jìn)行以減弱外界條件增大H2的濃度的影響)直至達(dá)到新的平衡。若上述反應(yīng)體系不改變反應(yīng)物的物質(zhì)的量,僅分別改變某一實(shí)驗(yàn)條件再進(jìn)行兩次實(shí)驗(yàn),測(cè)得H2的物質(zhì)的量隨時(shí)間變化如圖中虛線所示,曲線I改變的實(shí)驗(yàn)條件是 ,曲線Ⅱ改變的實(shí)驗(yàn)條件是 。
(3)下列各項(xiàng)中,不能夠說明CO2(g)+3H2(g)  CH3OH(g)+H2O(g)已達(dá)到平衡的是 (單選)。
CH3OH(g)+H2O(g)已達(dá)到平衡的是 (單選)。
| A.恒溫、恒容條件下,容器內(nèi)的壓強(qiáng)不發(fā)生變化 |
| B.一定條件下,CH3OH消耗的速率和CH3OH生成的速率相等 |
| C.一定條件下,H2O(g)的濃度保持不變 |
| D.一定條件下,單位時(shí)間內(nèi)消耗1 mol CO2,同時(shí)生成1 mol CH3OH |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(14分)
已知CO(g)+H2O(g) CO2(g)+H2(g)反應(yīng)的平衡常數(shù)和溫度的關(guān)系如下:
CO2(g)+H2(g)反應(yīng)的平衡常數(shù)和溫度的關(guān)系如下:
| |溫度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常數(shù) | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 ΔH=+8.0kJ·mol-1
ΔH=+8.0kJ·mol-1 ΔH=+90.4kJ·mol-1
ΔH=+90.4kJ·mol-1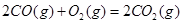 ΔH=-556.0kJ·mol-1
ΔH=-556.0kJ·mol-1 ΔH=-483.6kJ·mol-1
ΔH=-483.6kJ·mol-1 與
與 反應(yīng)生成
反應(yīng)生成 熱化學(xué)方程式 。
熱化學(xué)方程式 。查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(12分)超音速飛機(jī)在平流層飛行時(shí),尾氣中的NO會(huì)破壞臭氧層。科學(xué)家正在研究利用催化技術(shù)將尾氣中的NO和CO轉(zhuǎn)變成CO2和N2,化學(xué)方程式如下:
2NO+2CO 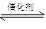 2CO2+N2
2CO2+N2
為了測(cè)定在某種催化劑作用下的反應(yīng)速率,在某溫度下用氣體傳感器測(cè)得不同時(shí)間的NO和CO濃度如下表:
| 時(shí)間/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/ mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/ mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
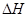 0(填寫“>”、“<”、“=”)。
0(填寫“>”、“<”、“=”)。| 實(shí)驗(yàn)編號(hào) | T/℃ | NO初始濃度 mol·L-1 | CO初始濃度 mol·L-1 | 催化劑的比表面積 ㎡·g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | | | 5.8×10-3 | 124 |
| Ⅲ | 350 | 1.2×10-3 | | |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(8分)某溫度時(shí),在一個(gè)2 L的密閉容器中,X、Y、Z三種氣體物質(zhì)的物質(zhì)的量隨時(shí)間的變化曲線如圖所示。根據(jù)圖中數(shù)據(jù),試填寫下列空白: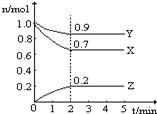
(1)該反應(yīng)的化學(xué)方程式為 ______ __ 。
(2)該反應(yīng)是由 開始的。(①正反應(yīng) ②逆反應(yīng) ③正逆反應(yīng)同時(shí)。)
(3)該反應(yīng)第 ______ 分鐘到達(dá)平衡狀態(tài)。
(4)反應(yīng)開始至3 min,氣體X的平均反應(yīng)速率為 _______。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
合理利用資源,降低碳的排放,實(shí)施低碳經(jīng)濟(jì)是今后經(jīng)濟(jì)生活主流方向。
⑴下列措施不利于有效減少二氧化碳排放的是 。
A.植樹造林,保護(hù)森林,保護(hù)植被
B.加大對(duì)煤和石油的開采,并鼓勵(lì)使用石油液化氣
C.推廣使用節(jié)能燈和節(jié)能電器,使用空調(diào)時(shí)夏季溫度不宜設(shè)置過低,冬天不宜過高
D.倡導(dǎo)出行時(shí)多步行和騎自行車,建設(shè)現(xiàn)代物流信息系統(tǒng),減少運(yùn)輸工具空駛率
⑵科學(xué)家致力于二氧化碳的“組合轉(zhuǎn)化”技術(shù)研究,如將CO2和H2以1∶4比例混合通入反應(yīng)器,適當(dāng)條件下反應(yīng)可獲得一種能源。完成以下化學(xué)方程式:CO2+4H2 +2H2O。
+2H2O。
⑶CO2合成生產(chǎn)燃料甲醇(CH3OH)是碳減排的新方向。進(jìn)行如下實(shí)驗(yàn):某溫度下在1 L的密閉容器中,充2 mol CO2和6 mol H2,發(fā)生:CO2(g)+3H2(g ) CH3OH(g)+H2O(g)能判斷該反應(yīng)已達(dá)化學(xué)反應(yīng)限度標(biāo)志的是 (填字母)。
CH3OH(g)+H2O(g)能判斷該反應(yīng)已達(dá)化學(xué)反應(yīng)限度標(biāo)志的是 (填字母)。
A.CO2百分含量保持不變
B.容器中H2濃度與CO2濃度之比為3:1
C.容器中混合氣體的質(zhì)量保持不變
D.CO2生成速率與CH3OH生成速率相等
現(xiàn)測(cè)得CO2和CH3OH(g)的濃度隨時(shí)間變化如左下圖所示。從反應(yīng)開始到平衡,氫氣的平均反應(yīng)速率v(H2)= mol/(L·min)。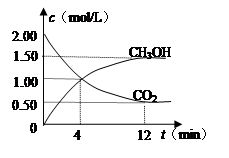
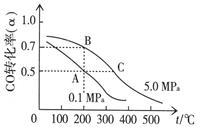
⑷CO在催化作用下也能生成甲醇:CO(g)+2H2(g)  CH3OH(g);已知密閉容器中充有10 mol CO與20 mol H2,CO的平衡轉(zhuǎn)化率(α)與溫度、壓強(qiáng)的關(guān)系如右上圖所示。
CH3OH(g);已知密閉容器中充有10 mol CO與20 mol H2,CO的平衡轉(zhuǎn)化率(α)與溫度、壓強(qiáng)的關(guān)系如右上圖所示。
①若A、C兩點(diǎn)都表示達(dá)到的平衡狀態(tài),則自反應(yīng)開始到達(dá)平衡狀態(tài)所需的時(shí)間tA tC(填“大于”、“小于”或“等于”)。
②若A、B兩點(diǎn)表示在某時(shí)刻達(dá)到的平衡狀態(tài),此時(shí)在A點(diǎn)時(shí)容器的體積為VAL,則A、B兩點(diǎn)時(shí)容器中,n(A)總︰n(B)總= 。
⑸以KOH為電解質(zhì)的甲醇燃料電池總反應(yīng)為:2CH3OH+3O2+4KOH= 2K2CO3+6H2O,通入甲醇的電極為燃料電池的負(fù)極,正極發(fā)生的電極反應(yīng)式為 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(14分)已知CO2、SO2、NOx是對(duì)環(huán)境影響較大的氣體,請(qǐng)你運(yùn)用所學(xué)知識(shí)參與環(huán)境治理,使我們周圍的空氣更好。
(1)硫酸生產(chǎn)中,SO2催化氧化生成SO3,反應(yīng)混合體系
中SO3的百分含量和溫度的關(guān)系如右圖所示(曲線上
點(diǎn)均為平衡狀態(tài))。由圖可知: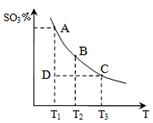
①2SO2(g) + O2(g) 2SO3(g)的△H____0(填“>”或“<”),若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(dòng)(填“向左”、“向右”或“不移動(dòng)”);
2SO3(g)的△H____0(填“>”或“<”),若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(dòng)(填“向左”、“向右”或“不移動(dòng)”);
②若溫度為T1時(shí),反應(yīng)進(jìn)行到狀態(tài)D時(shí),v(正)_______v(逆)(填“>”、“<”或“=”);
③硫酸廠的SO2尾氣用過量的氨水吸收,對(duì)SO2可進(jìn)行回收及重新利用,反應(yīng)的化學(xué)方程式為 、 ;
④新型氨法煙氣脫硫技術(shù)是采用氨水吸收煙氣中的SO2,再用一定量的磷酸與上述吸收產(chǎn)物反應(yīng)。其優(yōu)點(diǎn)除了能回收利用SO2外,還能得到一種復(fù)合肥料,該復(fù)合肥料可能的化學(xué)式為:________(只要求寫一種);
(2)汽車尾氣(含有烴類、CO、NOx等物質(zhì))是城市空氣的污染源。治理的方法之一是在汽車的排氣管上裝一個(gè)“催化轉(zhuǎn)換器”(用鉑、鈀合金作催化劑)。其前半部反應(yīng)方程式為:
2CO+2NO  2CO2+N2。它的優(yōu)點(diǎn)是 ;
2CO2+N2。它的優(yōu)點(diǎn)是 ;
(3)有人設(shè)想用圖所示裝置,運(yùn)用電化學(xué)原理將CO2、SO2轉(zhuǎn)
化為重要化工原料。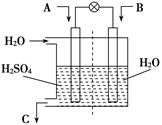
①若A為CO2,B為H2,C為CH3OH,則正極電極反應(yīng)式為
;
②若A為SO2,B為O2,C為H2SO4。科研人員希望每分鐘
從C處獲得100 mL 10 mol/L H2SO4,則A處通入煙氣(SO2
的體積分?jǐn)?shù)為1%)的速率為 L/min(標(biāo)準(zhǔn)狀況)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
溴及其化合物廣泛應(yīng)用于醫(yī)藥、農(nóng)藥、纖維、塑料組燃劑等,回答下列問題:
(1)海水提溴過程中,向濃縮的海水中通入 ,將其中的Br - 氧化,再用空氣吹出溴;然后用碳酸鈉溶液吸收溴,溴歧化為Br-和BrO3-,其離子方程式為 。
(2)溴與氯能以共價(jià)鍵結(jié)合形成BrCl。BrCl分子中, 顯正電性。BrCl與水發(fā)生反應(yīng)的化學(xué)方程式為 。
(3)CuBr2分解的熱化學(xué)方程式為:
2CuBr2(s)="2CuBr(s)+" Br2(g) △H=+105.4kJ/mol-1
在密閉容器中將過量CuBr2于487K下加熱分解,平衡時(shí)p(Br2)為4.66×103Pa。
①如反應(yīng)體系的體積不變,提高反應(yīng)溫度,則p(Br2)將會(huì) (填“增大”、“不變”或“減小”)。
②如反應(yīng)溫度不變,將反應(yīng)體系的體積增加一倍,則p(Br2)的變化范圍為 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
鎳具有優(yōu)良的物理和化學(xué)特性,是許多領(lǐng)域尤其是高技術(shù)產(chǎn)業(yè)的重要原料。羰基法提純粗鎳涉及的兩步反應(yīng)依次為:
反應(yīng)Ⅰ Ni(S)+4CO(g)
 Ni(CO)4(g)△H1<0
Ni(CO)4(g)△H1<0
反應(yīng)Ⅱ Ni(CO)4(g)  Ni(S)+4CO(g) △H2
Ni(S)+4CO(g) △H2
(1)在溫度不變的情況下,要提高反應(yīng)Ⅰ中Ni(CO)4的產(chǎn)率,可采取的措施有 、 。
(2)已知350K下的2L密閉容器中裝有100g粗鎳(純度98.5%,所含雜質(zhì)不與CO反應(yīng)),通入6 molCO氣體發(fā)生反應(yīng)Ⅰ制備Ni(CO)4,容器內(nèi)剩余固體質(zhì)量和反應(yīng)時(shí)間的關(guān)系如圖所示,10min后剩余固體質(zhì)量不再變化。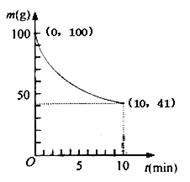
①反應(yīng)Ⅰ在0~10min的平均反應(yīng)速率v(Ni(CO)4)= 。
②若10min達(dá)到平衡時(shí)在右端得到29.5g純鎳,則反應(yīng)Ⅰ的平衡常數(shù)K1為多少?(寫出計(jì)算過程)
(3)反應(yīng)Ⅱ中 △H2 0(填“>”、“<”、“=”);若反應(yīng)Ⅱ達(dá)到平衡后,保持其他條件不變,降低溫度,重新達(dá)到平衡時(shí) 。(雙選)
a.平衡常數(shù)K增大 b.CO的濃度減小 c.Ni的質(zhì)量減小 d.v逆[Ni(CO)4]增大
(4)用吸收H2后的稀土儲(chǔ)氫合金作為電池負(fù)極材料(用MH)表示),NiO(OH)作為電池正極材料,KOH溶液作為電解質(zhì)溶液,可制得高容量,長(zhǎng)壽命的鎳氫電池。電池充放電時(shí)的總反應(yīng)為:
NiO(OH)+MH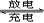 Ni(OH)2+M 電池充電時(shí),陽極的電極反應(yīng)式為 。電池充電時(shí)陰極上發(fā)生 (填“氧化”或“還原”)反應(yīng)
Ni(OH)2+M 電池充電時(shí),陽極的電極反應(yīng)式為 。電池充電時(shí)陰極上發(fā)生 (填“氧化”或“還原”)反應(yīng)
查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com