
【題目】已知:①RNO2![]() RNH2;
RNH2;
②![]() +HOSO3H
+HOSO3H![]() +H2O;
+H2O;
③苯環上原有的取代基對新導入的取代基進入苯環的位置有顯著影響。 以下是用苯作原料制備某些化合物的轉化關系圖:

(1)A是一種密度比水______ (填“小”或“大”)的無色液體;A轉化為B的化學方程 式是______。
(2)在“![]() ”的所有反應中屬于取代反應的是_________(填字母),屬于加成反應的是________(填字母);用1H核磁共振譜可以證明化合 物D中有__________種處于不同化學環境的氫。
”的所有反應中屬于取代反應的是_________(填字母),屬于加成反應的是________(填字母);用1H核磁共振譜可以證明化合 物D中有__________種處于不同化學環境的氫。
(3) B 中 苯 環 上 的 二 氯 代 物 有 _____種 同 分 異 構 體 ; CH3NH2 的 所 有 原 子_____(填“可能”或“不可能”)在同一平面上。
【答案】 大 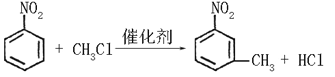 ab c 3 6 不可能
ab c 3 6 不可能
【解析】苯與濃硝酸發生硝化反應生成A,A為硝基苯,A與一氯甲烷反應生成B,B在Fe/HCl發生信息①的反應生成為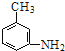 ,B中引入的甲基在硝基的間位,故B為
,B中引入的甲基在硝基的間位,故B為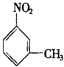 ,苯與溴發生取代反應生成C,C為溴苯,溴苯在濃硫酸條件下生成D,D與氫氣發生加成反應生成
,苯與溴發生取代反應生成C,C為溴苯,溴苯在濃硫酸條件下生成D,D與氫氣發生加成反應生成![]() ,可以知道C與濃硫酸反應發生對位取代,故D為
,可以知道C與濃硫酸反應發生對位取代,故D為![]() 。
。
(1)由分析可以知道A為硝基苯,其密度大于水;A轉化為B是硝基苯與一氯甲烷反應生成 ,反應方程式為
,反應方程式為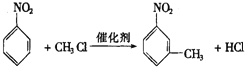 ;正確答案:大;
;正確答案:大; 。
。
(2)在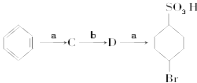 中,苯與溴發生取代反應生成C,C為溴苯,溴苯在濃硫酸條件下生成D,D與氫氣發生加成反應生成
中,苯與溴發生取代反應生成C,C為溴苯,溴苯在濃硫酸條件下生成D,D與氫氣發生加成反應生成![]() ,可以知道C與濃硫酸反應發生對位取代,故D為
,可以知道C與濃硫酸反應發生對位取代,故D為![]() ,所以a為取代反應,b為取代反應,c為加成反應;有機物D為
,所以a為取代反應,b為取代反應,c為加成反應;有機物D為![]() ,1H核磁共振譜有3種處于不同化學環境的氫;正確答案:ab;c;3。
,1H核磁共振譜有3種處于不同化學環境的氫;正確答案:ab;c;3。
(3)由以上分析可以知道B為 ,其苯環上二氯代物有:
,其苯環上二氯代物有: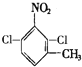 、
、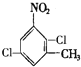 、
、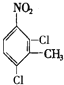 、
、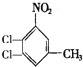 、
、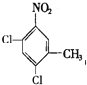 、
、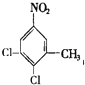 ,所以苯環上的二氯代物有6種;CH3NH2 中甲基為四面體結構,所以所有原子不是在同一平面上;正確答案:6;不可能。
,所以苯環上的二氯代物有6種;CH3NH2 中甲基為四面體結構,所以所有原子不是在同一平面上;正確答案:6;不可能。


科目:高中化學 來源: 題型:
【題目】NA為阿伏加德羅常數的值,下列說法不正確的是
A. 標準狀況下3.6 g H2O含有的電子數為2NA
B. 2.8 g乙烯與聚乙烯的混合物含有的極性鍵為0.4NA
C. 0.l moI Cl2與足量的鐵粉充分反應轉移的電子數為0.2NA
D. 1 L 0.2 mol/l的K2Cr2O7溶液中![]() 的數目為0.2NA
的數目為0.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現在污水治理越來越引起人們重視,可以通過膜電池除去廢水中的乙酸鈉和對氯苯酚( ![]() ),其原理如圖所示,下列說法正確的是( )
),其原理如圖所示,下列說法正確的是( )

A. 當外電路中有0.2mole―轉移時,A極區增加的H+個數為0.2NA
B. A極的電極反應式為 ![]()
C. 該裝置為電解池,電流方向從A極沿導線經小燈泡流向B極
D. B 極接電池的正極,發生還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨氣是一種重要的工業原料,可以制備如下圖所示的一系列物質(部分產物未標出)
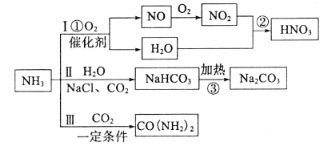
(1)線路Ⅰ為硝酸的制備
寫出反應①的化學方程式________;反應②中氧化劑與還原劑的物質的量之比為_______,工業尾氣中的氮氧化物常采用堿液法吸收,若NO與NO2按物質的量之比1:1被足量NaOH溶液完全吸收后只得到一種鈉鹽,該鈉鹽的化學式是_______。
(2)路線為Ⅱ純堿的制備
寫出反應③的化學方程式________,最終得到的純堿中可能含有NaCl,檢驗是否存在NaCl的實驗方案是________
(3)路線Ⅲ為尿素的制備
寫出合成尿素的化學方程式________
(4)實驗室中需要少量氨氣,寫出制備氨氣的化學方程式________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通常情況下,NCl3是一種油狀液體,其分子空間構型與NH3相似,下列對NCl3和NH3的有關敘述正確的是( )
A. 分子中N—Cl鍵鍵長與CCl4分子中C—Cl鍵鍵長相等
B. 在氨水中,大部分NH3與H2O以氫鍵(用“…”表示)結合形成NH3·H2O分子,則NH3·H2O的結構式為: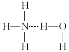
C. NCl3分子是非極性分子
D. NBr3比NCl3易揮發
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將下列各組物質, 分別按等物質的量混合后加水溶解, 有沉淀生成的是( )
A. AlCl3、Ba(OH)2、HNO3B. CaCl2、NaHCO3、HCl
C. Na2CO3、NaAlO2、NaOHD. AlCl3、K2SO4、HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有一混合物的水溶液,只可能含有以下離子中的若干種:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,現取三份100mL該溶液進行如下實驗:(已知:NH4++OH-![]() NH3↑+H2O)
NH3↑+H2O)
(1)第一份加入AgNO3溶液有沉淀產生;
(2)第二份加足量NaOH溶液加熱后,收集到0.08mol氣體;
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,經足量鹽酸洗滌干燥后,沉淀質量為4.66g。根據上述實驗,回答以下問題。
(1)由第一份進行的實驗推斷該混合物是否一定含有Cl-?________(答是或否)
(2)由第二份進行的實驗得知混合物中應含有_____(填離子符號),其物質的量濃度為______。
(3)由第三份進行的實驗可知12.54g沉淀的成分為________。
(4)綜合上述實驗,你認為以下結論正確的是_________。
A.該混合液中一定有K+、NH4+、CO32-、SO42-,可能含Cl-,且n(K)≥0.04mol
B.該混合液中一定有NH4+、CO32-、SO42-,可能含有K+、Cl-
C.該混合液中一定有NH4+、CO32-、SO42-,可能含有Mg2+、K+、Cl-
D.該混合液中一定有NH4+、SO42-,可能含有Mg2+、K+、Cl-
(5)我國政府為消除碘缺乏病,規定在食鹽中必須加入適量的碘酸鉀。檢驗食鹽中是否加碘,可利用如下反應:KIO3+KI+H2SO4=K2SO4+I2+H2O
①配平該方程式,并且用單線橋法表示該方程式電子轉移的方向和數目:________。
②該反應中氧化劑和還原劑的物質的量之比為_____________。
③如果反應中轉移0.5mol電子,則生成I2的物質的量為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】500mLNaNO3和Cu(NO3)2的混合溶液中c(Na+)為0.2 mol·L-1,用Pt作電極電解此溶液,當通電一段時間后,兩極均收集到2.24 L氣體(標準狀況下),假定電解后溶液體積仍為500 mL,下列說法正確的是
A. 原混合溶液中c(NO3-)=0.4 mol·L-1
B. 假設上述電解進行了5min,則通過的電量為0.2 ×NA×1.60×10-19C
C. 電解得到的Cu的質量為12.8g
D. 電解后溶液中pH=1,要想恢復原狀,可加0.05mol的CuCO3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com