
【題目】下列有關物質性質與用途具有對應關系的是
A. Si的熔點高,可用作半導體材料 B. Cl2具有強氧化性,可用于漂白有色有機物質
C. Na2CO3溶液呈堿性,可用于洗滌油污 D. Al2O3硬度很大,可用于制造耐火材料
科目:高中化學 來源: 題型:
【題目】下列物質中不能用化合反應的方法制得的是
①SiO2 ②H2SiO3 ③Al(OH)3 ④Fe(OH)3 ⑤FeCl2
A. ①③ B. ②③ C. ①④ D. ④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】青蒿素是一種有效的抗瘧藥。常溫下,青蒿素為無色針狀晶體,難溶于水,易溶于有機溶劑,熔點為156~157℃。提取青蒿素的方法之一是乙醚浸取法,提取流程如下:

請回答下列問題:
(l)對青蒿進行破碎的目的是__________________。
(2)操作I用到的玻璃儀器是__________,操作Ⅱ的名稱是_______。
(3)用下列實驗裝置測定青蒿素的化學式,將28.2g青蒿素放在燃燒管C中充分燃燒:

① 儀器各接口的連接順序從左到右依次為_______(每個裝置限用一次)。A裝置中發生的化學反應方程式為_________________。
② 裝置C中CuO的作用是_________________。
③ 裝置D中的試劑為_________________。
④ 已知青蒿素是烴的含氧衍生物,用合理連接后的裝置進行實驗.測量數據如下表:
裝置質量 | 實驗前/g | 實驗后/g |
B | 22.6 | 42.4 |
E(不含干燥管) | 80.2 | 146.2 |
則青蒿素的最簡式為__________。
(4)某學生對青蒿素的性質進行探究。將青蒿素加入含有NaOH 、酚酞的水溶液中,青蒿素的溶解度較小,加熱并攪拌,青蒿素的溶解度增大,且溶液紅色變淺,與青蒿素化學性質相似的物質是______(填字母代號)。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)配制稀硫酸時,先將濃硫酸加入燒杯中,后倒入蒸餾水(______)
(2)稱取2.0 g NaOH固體,可先在托盤上各放一張濾紙,然后在右盤上添加2 g砝碼,左盤上添加NaOH固體(_______)
(3)按照下圖操作,配制一定濃度的NaCl溶液(_____)

(4)按照下圖操作,配制0.10 mol·L-1 NaOH溶液(______)
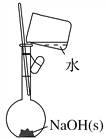
(5)配制溶液定容時,俯視容量瓶刻度會使溶液濃度偏高(_______)
(6)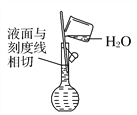 配制溶液(_______)
配制溶液(_______)
(7)因為Ca(OH)2能制成澄清石灰水,所以可配制2.0 mol·L-1的Ca(OH)2溶液(_____)
(8)配制0.100 0 mol·L-1氯化鈉溶液時,將液體轉移到容量瓶中需用玻璃棒引流(_______)
(9)用容量瓶配制溶液,定容時俯視刻度線,所配溶液濃度偏小(________)
(10)用固體NaCl配制0.5 mol·L-1的溶液,所用的儀器有:燒杯、玻璃棒、膠頭滴管、容量瓶(_______)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】前四周期元素A、B、C、D、E的原子序數依次增大,A的質子數等于周期數,B與C的 P軌道均有三個成單電子,D的最高正價與最低負價代數和為4,E的最外層只有一個電子, 內層軌道處于全充滿狀態。試回答下列問題。
(1)基態E原子的電子排布式為_________;C和D的第一電離能較大的________(填元素符號)。
(2)DO32-中D原子的雜化類型為_________;A、D和氧元素組成的液態化合物A2DO4中存在的作用力有_____________。
(3)結構式為A—B=B—A的分子中σ鍵和π鍵的數目比為________;B2分子和NO+離子互為等離子體,則NO+的電子式為___________。
(4)向EDO4溶液中加入過量稀氨水,其化學方程式為_______________;產物中陽離子的配體是_____________(填化學式)。
(5)D(黑球)和E(白球)形成某種晶體的晶胞如圖所示。已知該晶體的晶胞邊長為516Pm,則黑球和白球之間最近距離為________pm(精確到0.1,已知![]() =1.732)若ED中D2-被O2-代替,形成的晶體只能采取NaCl型堆積,試從晶體結構分析其不同及原因__________。
=1.732)若ED中D2-被O2-代替,形成的晶體只能采取NaCl型堆積,試從晶體結構分析其不同及原因__________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的值,下列說法正確的是
A. 標準狀況下,22.4L乙醇的分子數約為NA
B. 14gN2和CO的混合氣體中所含原子數為NA
C. 48gO2和O3的混合氣體中所含的原子數為3NA
D. 1mo1·L-1的MgC12溶液中,C1-離子的數目為2 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于膠體的說法正確的是( )
A. 依據丁達爾效應可將分散系分為溶液、膠體與濁液
B. 向污水中投放明礬,生成能凝聚懸浮物的膠體:Al3++3H2O![]() Al(OH)3(膠體)+3H+
Al(OH)3(膠體)+3H+
C. H+、K+、S2-、Br-能在Fe(OH)3膠體中大量共存
D. 沸水中滴加適量飽和FeCl3溶液,形成帶電的膠體,導電能力增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d、e均為周期表前四周期元素,原子序數依次增大,相關信息如下表所示。
a | 原子核外電子分占3個不同能級,且每個能級上排布的電子數相同 |
b | 基態原子的p軌道電子數比s軌道電子數少1 |
c | 在周期表所列元素中電負性最大 |
d | 位于周期表中第4縱行 |
e | 基態原子M層全充滿,N層只有一個電子 |
請回答:
(1)d屬于_____區的元素,其基態原子的價電子排布圖為_____。
(2)b與其同周期相鄰元素第一電離能由大到小的順序為_____(用元素符號表示)。
(3)c的氫化物水溶液中存在的氫鍵有_____種,任意畫出一種:_____。
(4)a與其相鄰同主族元素的最高價氧化物的熔點高低順序為_____ (用化學式表示)。若將a元素最高價氧化物水化物對應的正鹽酸根離子表示為A,則A的空間構型為_____;A的中心原子的軌道雜化類型為_____;與A互為等電子體的一種分子為_____ (填化學式)。
(5)向e的硫酸鹽中加入氨水首先形成藍色沉淀,繼續滴加氨水沉淀溶解,得到深藍色的透明溶液,試用離子方程式解釋產生這一現象的原因:____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2 L恒容密閉容器中,發生反應 2NO(g)+O2(g)![]() 2NO2(g)。
2NO2(g)。
⑴某溫度時,按物質的量比2∶1充入NO和O2開始反應,n(NO)隨時間變化如表:
時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
0~4s內以O2濃度變化表示的反應速率__________1~5s內以NO濃度變化表示的反應速率(選填“小于”、“大于”、“等于”)。
⑵該反應的平衡常數表達式為K=______。能說明該反應已達到平衡狀態的是_____。
A.氣體顏色保持不變 B.氣體平均相對分子質量保持不變
C.υ逆(NO)=2υ正(O2) D.氣體密度保持不變
⑶已知:K300℃>K400℃。下列措施能使該反應的反應速率增大且平衡向正反應方向移動的是________。
A.升高溫度 B.充入Ar使壓強增大 C.充入O2使壓強增大 D.選擇高效催化劑
⑷將amolNO和bmolO2發生反應,要使反應物和生成物物質的量之比為1∶2,則a/b的取值范圍是_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com