
甲醇可作為燃料電池的原料。通過下列反應可以制備甲醇:CO ( g ) + 2H2 ( g )  CH3OH ( g ) △H=-90.8 kJ·mol-1 在一容積可變的密閉容器中充入10 mol CO 和20 molH2,CO 的平衡轉化率隨溫度(T)、壓強(P)的變化如圖所示,當達到平衡狀態(tài)A 時,容器的體積為20 L。
CH3OH ( g ) △H=-90.8 kJ·mol-1 在一容積可變的密閉容器中充入10 mol CO 和20 molH2,CO 的平衡轉化率隨溫度(T)、壓強(P)的變化如圖所示,當達到平衡狀態(tài)A 時,容器的體積為20 L。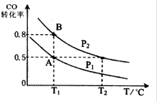
(1)該反應的化學平衡常數(shù)表達式為 。
(2)如反應開始時仍充入10mol CO 和20mol H2,則在平衡狀態(tài)B時容器的體積V(B)= L。
(3)關于反應CO(g)+2H2(g) CH3OH(g)在化學平衡狀態(tài)時的描述正確的是 (填字母)。
CH3OH(g)在化學平衡狀態(tài)時的描述正確的是 (填字母)。
A.CO的含量保持不變 B.容器中CH3OH濃度與CO濃度相等
C.2V正(CH3OH)=V正(H2)D.容器中混合氣體的平均相對分子質量保持不變
(4)CO(g)+2H2(g) CH3OH(g),按照相同的物質的量 投料,測得CO在不同溫度下的平衡轉化率與壓強的關系如圖所示。下列說法正確的是 。
CH3OH(g),按照相同的物質的量 投料,測得CO在不同溫度下的平衡轉化率與壓強的關系如圖所示。下列說法正確的是 。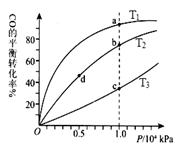
A.溫度:T1 < T2 <T3
B.正反應速率:ν(a)>ν(c); ν(b)>ν(d)
C.平衡常數(shù): K(a) ="K(c)" ; K(b) >K(d)
D.平均摩爾質量:M(a)<M(c); M(b)>M(d)
(5)已知CO2(g)+H2(g) CO(g)+H2O(g) △H=" +" 41.3 kJ·mol-1,試寫出由
CO(g)+H2O(g) △H=" +" 41.3 kJ·mol-1,試寫出由
CO2和H2制取甲醇的熱化學方程式 。
(1)K=C(CH3OH)/C2(H2)?C(CO) (2)4 (3)A C D (4) A
(5)CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H=-49.5 kJ·mol-1
CH3OH(g) +H2O(g) △H=-49.5 kJ·mol-1
解析試題分析:(1)根據(jù)平衡常數(shù)的定義可得到該反應的化學平衡常數(shù)的表達式為K==C(CH3OH)/C2(H2)?C(CO)。(2)若密閉容器中充入10 mol CO 和20 molH2,當達到平衡狀態(tài)A 時,CO的轉化率為0.5,此時各物質的物質的量為CO為5mol;H2為10mol; CH3OH為5mol。n(氣體)=20mol,容器的體積為20 L。如反應開始時仍充入10mol CO 和20mol H2,在達到平衡狀態(tài)B時CO的轉化率為0.8,則此時各物質的物質的量為CO為2mol,H2為4mol, CH3OH為8mol。n(氣體)=14mol。由于A、B是在相同溫度下程度的。所以化學平衡常數(shù)不變設第二次達到平衡時容器的體積為V。則 ,解得v=4(L)。(3) A.CO的含量保持不變,則各組分的物質的量,總物質的量不變。可逆反應達到平衡狀態(tài)。正確。B.容器中CH3OH濃度與CO濃度相等,這只是一個很特殊的情況,這時反應可能達到平衡,也可能未達到平衡狀態(tài)。錯誤。C.在任何時刻2V正(CH3OH)=V正(H2),若2V正(CH3OH)=V逆(H2),則V正(H2)=V逆(H2),反應達到平衡。正確。D.由于該反應是個反應前后氣體體積不等的反應,如果反應未達到平衡,則氣體的物質的量就會發(fā)生改變,混合氣體的平均相對分子質量也就會隨著改變。若容器中混合氣體的平均相對分子質量保持不變,則氣體的物質的量不變。故反應達到平衡狀態(tài)。正確。(4)A.由于該反應的正反應是放熱反應,所以在其它條件不變的情況下,升高溫度,平衡向吸熱反應方向移動,也就是向逆反應方向移動,這時反應物的轉化率降低。因為CO的平衡轉化率a>b>c,所以溫度:T1 < T2 <T3。正確。B.在其它條件不變時,升高溫度,化學反應速率加快。由于溫度T1 < T2 <T3,所以速率:ν(c)>ν(a);在其它條件相同時,增大壓強,化學反應速率加快。由于壓強b>d,所以速率:ν(b)>ν(d).錯誤。C.化學 平衡常數(shù)只與溫度有關,與其它條件無關。由于溫度T1 < T2 <T3。升高溫度,平衡向逆反應方向移動,K減小。K(a) >K(c) ; K(b) =K(d)。錯誤。D.升高溫度,平衡向逆反應方向移動,平衡時氣體的物質的量增大,氣體的平均摩爾質量減小。由于溫度T1 < T3,所以平衡時n(c)總> n(a)總,M(a)>M(c);在相同的溫度下,增大壓強,平衡正向移動,平衡時氣體的物質的量減小。所以平衡時n(d)總> n(b)總,M(b)>M(d).錯誤。(5)將CO2(g)+H2(g)
,解得v=4(L)。(3) A.CO的含量保持不變,則各組分的物質的量,總物質的量不變。可逆反應達到平衡狀態(tài)。正確。B.容器中CH3OH濃度與CO濃度相等,這只是一個很特殊的情況,這時反應可能達到平衡,也可能未達到平衡狀態(tài)。錯誤。C.在任何時刻2V正(CH3OH)=V正(H2),若2V正(CH3OH)=V逆(H2),則V正(H2)=V逆(H2),反應達到平衡。正確。D.由于該反應是個反應前后氣體體積不等的反應,如果反應未達到平衡,則氣體的物質的量就會發(fā)生改變,混合氣體的平均相對分子質量也就會隨著改變。若容器中混合氣體的平均相對分子質量保持不變,則氣體的物質的量不變。故反應達到平衡狀態(tài)。正確。(4)A.由于該反應的正反應是放熱反應,所以在其它條件不變的情況下,升高溫度,平衡向吸熱反應方向移動,也就是向逆反應方向移動,這時反應物的轉化率降低。因為CO的平衡轉化率a>b>c,所以溫度:T1 < T2 <T3。正確。B.在其它條件不變時,升高溫度,化學反應速率加快。由于溫度T1 < T2 <T3,所以速率:ν(c)>ν(a);在其它條件相同時,增大壓強,化學反應速率加快。由于壓強b>d,所以速率:ν(b)>ν(d).錯誤。C.化學 平衡常數(shù)只與溫度有關,與其它條件無關。由于溫度T1 < T2 <T3。升高溫度,平衡向逆反應方向移動,K減小。K(a) >K(c) ; K(b) =K(d)。錯誤。D.升高溫度,平衡向逆反應方向移動,平衡時氣體的物質的量增大,氣體的平均摩爾質量減小。由于溫度T1 < T3,所以平衡時n(c)總> n(a)總,M(a)>M(c);在相同的溫度下,增大壓強,平衡正向移動,平衡時氣體的物質的量減小。所以平衡時n(d)總> n(b)總,M(b)>M(d).錯誤。(5)將CO2(g)+H2(g) CO(g)+H2O(g) △H=" +" 41.3 kJ/mol和 CO ( g ) + 2H2 ( g )
CO(g)+H2O(g) △H=" +" 41.3 kJ/mol和 CO ( g ) + 2H2 ( g )  CH3OH ( g ) △H=-90.8 kJ/mol相加可得CO2和H2制取甲醇的熱化學方程式:CO2(g) +3H2(g)
CH3OH ( g ) △H=-90.8 kJ/mol相加可得CO2和H2制取甲醇的熱化學方程式:CO2(g) +3H2(g)  CH3OH(g) +H2O(g) △H=-49.5 kJ/mol.
CH3OH(g) +H2O(g) △H=-49.5 kJ/mol.
考點:考查化學平衡常數(shù)的表達式、熱化學方程式的書寫及平衡狀態(tài)的判斷、外界條件對化學反應速率、化學平衡的影響等知識。


科目:高中化學 來源: 題型:填空題
2SO2(g)+O2(g)=2SO3(g)反應過程的能量變化如圖所示。已知1 mol SO2(g)氧化為1 mol SO3(g)的ΔH=-99 kJ·mol-1。請回答下列問題: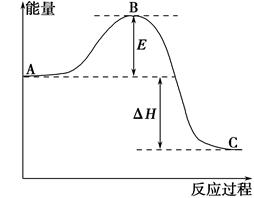
(1)圖中A、C分別表示________、________;
(2)E表示________;E的大小對該反應的反應熱________(填“有”或“無”)影響。
(3)該反應通常用V2O5作催化劑,加V2O5會使圖ΔH________(填“變大”、“變小”或“不變”),理由是_____________________________________。
(4)圖中ΔH=________kJ·mol-1;
(5)已知單質硫的燃燒熱為296 kJ·mol-1,計算由S(s)生成3 mol SO3(g)的ΔH=________(要求計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2013年全國各地都遭遇“十面霾伏”。其中,機動車尾氣和燃煤產生的煙氣對空氣質量惡化貢獻較大。
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g)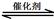 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態(tài)的是 (填代號)。
(下圖中υ正、K、n、w分別表示正反應速率、平衡常數(shù)、物質的量、質量分數(shù))
(2)機動車尾氣和煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g)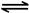 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
(3)用NH3催化還原NOX也可以消除氮氧化物的污染。如圖,采用NH3作還原劑,煙氣以一定的流速通過兩種不同催化劑,測量逸出氣體中氮氧化物含量,從而確定煙氣脫氮率(注:脫氮率即氮氧化物轉化率),
反應原理為:NO(g) +NO2(g)+2NH3(g)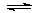 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。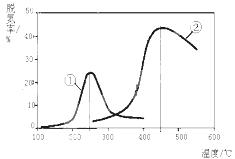
①該反應的△S 0,△H 0(填“>”、“=”或 “<”)。
②對于氣體反應,用某組分(B)的平衡壓強(pB)代替物質的量濃度(cB)也可以表示平衡常數(shù)(記作KP),
則上述反應的KP= 。
③以下說法正確的是 。
A.第②種催化劑比第①種催化劑脫氮率高
B.相同條件下,改變壓強對脫氮率沒有影響
C.催化劑①、②分別適合于250℃和450℃左右脫氮
(4)NO2、O2和熔融NaNO3可制作燃料電池,其原理見圖。該電池在使用過程中石墨I電極上生成氧化物Y,其電極反應為 。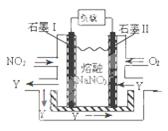
(5)硝酸工業(yè)尾氣中氮氧化物(NO和NO2)可用尿素〔CO(NH2)2〕溶液除去。反應生成對大氣無污染的氣體。1 mol尿素能吸收工業(yè)尾氣中氮氧化物(假設NO、NO2體積比為1:1)的質量為___________g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1) 在一定溫度下,測得0.1 mol·L-1CH3COOH溶液的PH為3.0。則CH3COOH在水中的電離為 ,此溫度CH3COOH的電離平衡常數(shù)為 。
(2) 在25℃時,Kw=1.0×10-14,測得0.1 mol·L-1 Na2A溶液的pH=7。則H2A在水溶液中的電離方程式為 ,該溫度下,將0.01 mol·L-1 H2A溶液稀釋到20倍后,溶液的pH= 。
(3) 已知HCN(aq)+NaOH(aq)=NaCN(aq)+ H2O(l) ΔH=-12.1 kJ·mol-1;
HCl(aq) +NaOH(aq)=NaCl(aq) + H2O(l) ΔH=-57.3 kJ·mol-1。
則在水溶液中HCN H++CN-電離的ΔH為 kJ·mol-1
H++CN-電離的ΔH為 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2013年霧霾天氣多次肆虐我國中東部地區(qū)。其中,汽車尾氣和燃煤尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g)+2CO (g)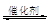 2CO2 (g) +N2 (g)在密閉容器中發(fā)生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如圖所示。據(jù)此判斷:
2CO2 (g) +N2 (g)在密閉容器中發(fā)生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如圖所示。據(jù)此判斷:
①該反應的平衡常數(shù)表達式為 。
②該反應的ΔH 0(選填“>”、“<”)。
③當固體催化劑的質量一定時,增大其表面積可提高化 學反應速率。若催化劑的表面積S1>S2,在圖中畫出c(CO2)在T2、S2條件下達到平衡過程中的變化曲線。
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環(huán)境問題。
① 煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOx可以消除氮氧化物的污
染。
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) 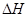 =-867kJ·mol-1
=-867kJ·mol-1
2NO2(g)  N2O4(g)
N2O4(g) 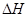 =-56.9kJ·mol-1
=-56.9kJ·mol-1
寫出CH4催化還原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的熱化學方程式 。
②將燃煤產生的二氧化碳回收利用,可 達到低碳排放的目的。下圖是通過光電轉化原理以廉價原料制備新產品的示意圖。寫出上述光電轉化過程的化學反應方程式 。催化劑a、b之間連接導線上電子流動方向是 (填a→b或b→a) 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學反應中既有物質變化,又有能量變化,釋放或吸收熱量是化學反應中能量變化的主要形式之一。已知C(石墨)、H2(g)燃燒的熱化學方程式分別為:
① C(石墨)+ O2(g)=CO(g)
O2(g)=CO(g)  ="-111.0" KJ·mol-1
="-111.0" KJ·mol-1
② H2(g)+  O2(g) =H20(g)
O2(g) =H20(g)  ="-242.0" kJ·mol-1
="-242.0" kJ·mol-1
③ C(石墨)+O2(g)=CO2(g)  ="-394.0" kJ·mol-1
="-394.0" kJ·mol-1
請解答下列問題:
(1)化學反應中有能量變化的本質原因是反應過程中有 的斷裂和形成。上述三個反應都是 (填“吸熱”或“放熱”)反應。
(2)在熱化學方程式中,需要標明反應物及生成物的狀態(tài)的原因是 ;在①中,02的化學計量數(shù)“1/2”是表示 (填字母)。
a.分子個數(shù) b.物質的量 c.氣體的體積
(3)反應2H20(g)=2H2(g)+02(g)的 = KJ·mol-1。
= KJ·mol-1。
(4)若C(金剛石)+02(g)=C02(g)的 ="-395.0" kJ·mol-1,則穩(wěn)定性:金剛石 (填“>”、“<”或“=”)石墨。
="-395.0" kJ·mol-1,則穩(wěn)定性:金剛石 (填“>”、“<”或“=”)石墨。
(5)已知形成H20(g)中的2 mol H-O鍵能放出926.0 kJ的能量,形成1 mol 02(g)中的共價鍵能放出498.0 kJ的能量,則斷裂1 mol H2(g)中的H-H鍵需要的能量 KJ。
(6)工業(yè)制氫氣的一個重要途徑是用CO(g)與H2O(g)反應生成C02(g)和H2(g),則該反應的熱化學方程式是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
國家擬于“十二五”期間將SO2的排放量減少8%,研究SO2綜合利用意義重大。
(1)已知25℃時:SO2(g)+2CO(g)=2CO2(g)+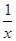 Sx(s) △H=akJ/mol
Sx(s) △H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+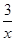 Sx(s) △H=bkJ/mol。
Sx(s) △H=bkJ/mol。
則CO與Sx生成COS反應的熱化學方程式是________________________。
(2)有人設想按如圖所示裝置用廢氣中的SO2生產硫酸。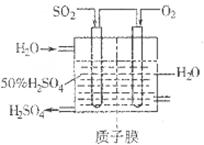
寫出SO2電極的電極反應式__________________________。
(3)提高反應2SO2(g)+O2(g)  2SO3(g) △H<0中SO2的轉化率是控制SO2排放的關鍵措施之一。某課外活動小組進行了如下探究:
2SO3(g) △H<0中SO2的轉化率是控制SO2排放的關鍵措施之一。某課外活動小組進行了如下探究:
①T1溫度時,在2L的密閉容器中加入4.0molSO2和2.0molO2,5 min后反應達到平衡,二氧化硫的轉化率為50%,前5 min內SO2的平均反應速率為___________。
②在①中的反應達到平衡后,改變下列條件,能使SO2的轉化率及SO3的平衡濃度都比原來增大的是
_________(填序號)。
a.溫度和容器體積不變,充入1.0molHe (g)
b.溫度和容器體積不變,充入2molSO2和lmolO2
c.溫度和容器體積不變,充入1.0molSO2
d.在其他條件不變時,減小容器的容積
③在其他條件不變的情況下,探究起始時氧氣物質的量對2SO2(g)+O2(g)  2SO3(g)反應的影響,實驗結果如圖所示。(圖中T表示溫度,n表示物質的量):在a、b、c三點所處的平衡狀態(tài)中,SO2的轉化率最高的是____,溫度T1______T2(填“>”“<”或“=”)。
2SO3(g)反應的影響,實驗結果如圖所示。(圖中T表示溫度,n表示物質的量):在a、b、c三點所處的平衡狀態(tài)中,SO2的轉化率最高的是____,溫度T1______T2(填“>”“<”或“=”)。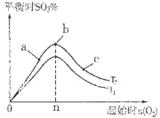
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化工行業(yè)的發(fā)展必須符合國家節(jié)能減排的總體要求。請回答下列問題:
(1)已知C(s)+H2O(g)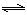 CO(g)+H2(g),則該反應的平衡常數(shù)表達式為 。
CO(g)+H2(g),則該反應的平衡常數(shù)表達式為 。
(2)已知在一定溫度下,
C(s)+CO2(g) 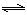 2CO(g) △H1
2CO(g) △H1
CO(g)+H2O(g) 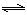 H2(g)+CO2(g) △H2
H2(g)+CO2(g) △H2
C(s)+H2O(g)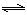 CO(g)+H2(g) △H3
CO(g)+H2(g) △H3
則△H1、△H2、△H3之間的關系是: 。
(3)通過研究不同溫度下平衡常數(shù)可以解決某些實際問題。已知等體積的一氧化碳和水蒸氣進入反應時,會發(fā)生如下反應: CO(g)+H2O(g) 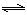 H2(g)+CO2(g),該反應平衡常數(shù)隨溫度的變化如表所示。
H2(g)+CO2(g),該反應平衡常數(shù)隨溫度的變化如表所示。
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數(shù)K | 9.94 | 9 | 1 |
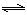 2NO2(g) △H>0在溫度為T1、T2時,平衡體系中NO2的體積分數(shù)隨壓強變化曲線如圖所示。下列說法正確的是 :
2NO2(g) △H>0在溫度為T1、T2時,平衡體系中NO2的體積分數(shù)隨壓強變化曲線如圖所示。下列說法正確的是 :
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫酸鹽主要來自地層礦物質,多以硫酸鈣、硫酸鎂的形態(tài)存在。
(1)已知:①Na2SO4(s)=Na2S(s)+2O2(g) ; ΔH1=" +1011.0" kJ · mol-1
②C(s)+O2(g)=CO2(g) ; ΔH2=-393.5 kJ · mol-1
③2C(s)+O2(g)="2CO(g)" ;ΔH3=-221.0 kJ · mol-1
則反應④Na2SO4(s)+4C(s)=Na2S(s)+4CO(g);ΔH4= kJ · mol-1,該反應能自發(fā)進行的原因是 ;工業(yè)上制備Na2S不用反應①,而用反應④的理由是 。
(2)已知不同溫度下2SO2+O2 2SO3的平衡常數(shù)見下表。
2SO3的平衡常數(shù)見下表。
| 溫度(℃) | 527 | 758 | 927 |
| 平衡常數(shù) | 784 | 1.0 | 0.04 |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com