
I.�ƌW(xu��)��һֱ�����ڡ��˹��̵����ķ����о���Ŀǰ�ϳɰ��ļ��g(sh��)ԭ��鵪��͚���ڸߜظ߉������l�������ɰ��⣬һ���l���£���һ��2L�����]�����г���2molN2��6molH2������(y��ng)�_(d��)ƽ��r����NH3�ĝ�Ȟ�0.5mol/L�����ų�QkJ������ԓ����(y��ng)�ğữ�W(xu��)����ʽ�ɱ�ʾ��______��
II.��֪��N2O4(g) 2NO2(g) ��H����57.20kJ/mol��
2NO2(g) ��H����57.20kJ/mol��
��1000C�r����0.100molN2O4���w����lL���ݳ�յ����]�����У�ÿ��һ���r�g��ԓ������(n��i)�����|(zh��)����M(j��n)�з����õ��±픵(sh��)��(j��)��
| �r�g��s�� | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol | 0.000 | 0.060 | c2 | 0.120 | 0.120 |

 N2O4(g)(g) ��H����57.20kJ/mol����غ����·���(y��ng)��ͬ�r�g�քe�y���wϵ��NO2�İٷֺ����քe��a1��a2����֪T1<T2,�ta1____a2(�x��A��B��C��D��գ���
N2O4(g)(g) ��H����57.20kJ/mol����غ����·���(y��ng)��ͬ�r�g�քe�y���wϵ��NO2�İٷֺ����քe��a1��a2����֪T1<T2,�ta1____a2(�x��A��B��C��D��գ�����(14��)��. N2(g)+3H2(g) 2NH3(g) ��H����2QkJ/mol��2�֣�
2NH3(g) ��H����2QkJ/mol��2�֣�
��. ��1��K��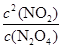 ��
�� 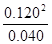 �� ���� �� ��ÿ��1�֣���3�֣�
�� ���� �� ��ÿ��1�֣���3�֣�
��2��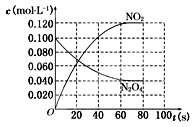 (2�֣�
(2�֣�
��3�� 0.001mol/(L��s)��1�֣���4�� 40% (2�֣� B C��2�֣� ��5�� D��2�֣�
����ԇ�}��������.����(y��ng)�_(d��)ƽ��r����NH3�ĝ�Ȟ�0.5mol/L�����ų�QkJ������������0.5mol/L��2L��1mol����r�ų�QkJ����������ԓ����(y��ng)�ğữ�W(xu��)����ʽ��N2(g)+3H2(g) 2NH3(g) ��H����2QkJ/mol��
2NH3(g) ��H����2QkJ/mol��
��.��1�����W(xu��)ƽ�ⳣ��(sh��)����һ���l���£���(d��ng)���淴��(y��ng)�_(d��)��ƽ���B(t��i)�r���������ȵă�֮�e�ͷ���(y��ng)���ȵă�֮�e�ı�ֵ�����Ը���(j��)����ʽ��֪��ԓ����(y��ng)��ƽ�ⳣ��(sh��)K��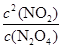 ������(j��)���Д�(sh��)��(j��)��֪��20s�r����NO2��0.060mol���t����(j��)����ʽ��֪������N2O4�����|(zh��)������0.030mol�����c1��0.100mol��0.030mol��0.070mol������(y��ng)��20s�M(j��n)�е�40s�r����N2O4��0.070mol��0.050mol��0.020mol.����(j��)����ʽ��֪������NO2��0.040mol������c2��0.060mol��0.040mol��0.100mol������c1��c2������(y��ng)�M(j��n)�е�60s�r����(y��ng)�_(d��)��ƽ���B(t��i)������c3��c4��
������(j��)���Д�(sh��)��(j��)��֪��20s�r����NO2��0.060mol���t����(j��)����ʽ��֪������N2O4�����|(zh��)������0.030mol�����c1��0.100mol��0.030mol��0.070mol������(y��ng)��20s�M(j��n)�е�40s�r����N2O4��0.070mol��0.050mol��0.020mol.����(j��)����ʽ��֪������NO2��0.040mol������c2��0.060mol��0.040mol��0.100mol������c1��c2������(y��ng)�M(j��n)�е�60s�r����(y��ng)�_(d��)��ƽ���B(t��i)������c3��c4��
��2������(j��)���Д�(sh��)��(j��)��֪��ƽ��r����NO2��0.120mol����������N2O4��0.060mol���tN2O4��ƽ������0.040mol�����Դ˷���(y��ng)��N2O4��NO2�ĝ���S�r�g׃���������� ��
��
��3���ķ���(y��ng)�_ʼ���_(d��)�����W(xu��)ƽ��r��������������ƽ������(y��ng)���ʞ�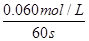 ��0.001mol/(L��s)��
��0.001mol/(L��s)��
��4�� 2NO2(g) N2O4(g)
N2O4(g)
��ʼ��ȣ�mol/L�� 0.200 0
�D(zhu��n)����ȣ�mol/L�� 2x x
ƽ���ȣ�mol/L�� 0.200��2x x
�tԓ����(y��ng)��ƽ�ⳣ��(sh��)��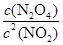 ��
��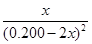
�����淴��(y��ng)��ƽ�ⳣ��(sh��)��������(y��ng)ƽ�ⳣ��(sh��)�ĵ���(sh��)������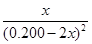 ��
��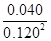 �����x��0.04������NO2���D(zhu��n)���ʣ�
�����x��0.04������NO2���D(zhu��n)���ʣ�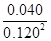 ��100%��40%��
��100%��40%��
A���pСNO2�ĝ�ȣ��ஔ(d��ng)�ڽ��͉���(qi��ng)��ƽ�����淴��(y��ng)�����Ƅӣ�NO2�D(zhu��n)���ʽ��ͣ�A�����_��B������(y��ng)�şᣬ���͜ض�ƽ����������(y��ng)�����Ƅӣ�NO2�D(zhu��n)��������B���_��C������NO2�ĝ�ȣ��ஔ(d��ng)������(qi��ng)��ƽ����������(y��ng)�����Ƅӣ�NO2�D(zhu��n)��������C���_��D�����ߜضȣ�ƽ����ƽ�����淴��(y��ng)�����Ƅӣ�NO2�D(zhu��n)���ʽ��ͣ�D�����_��E���ٳ���һ������He��ƽ�ⲻ�Ƅӣ�E�����_�����xBC��
��5�����ߜض�ƽ�����淴��(y��ng)�M(j��n)�У�ƽ��r���������ĺ������ض�Խ�߷���(y��ng)����Խ�죬���_(d��)ƽ��ĕr�gԽ�̣���(j��)�������������������c�r�g�P(gu��n)ϵ�D��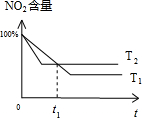 ���ɈD��֪��t1�r��a1��a2��t1�r��֮ǰa1��a2��t1�r��֮��a1��a2���ʴ𰸞�D��
���ɈD��֪��t1�r��a1��a2��t1�r��֮ǰa1��a2��t1�r��֮��a1��a2���ʴ𰸞�D��
���c������ữ�W(xu��)����ʽ�ĕ���������(y��ng)���ʺ�ƽ�ⳣ��(sh��)�����P(gu��n)Ӌ�㣻���l����ƽ���B(t��i)��Ӱ푵�


 ������I(y��)��ٿ옷������������ϵ�д�
������I(y��)��ٿ옷������������ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��������Ȼ�����Ҫ�ɷ֣������a(ch��n)�����Б�(y��ng)�÷dz��V����һ�N���W(xu��)���|(zh��)��
��1��һ���l���£��ü�����������������NOx������Ⱦ����֪��
��CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)�� ��H1
��CH4(g) + 4NO2(g) =" 4NO(g)" + CO2(g) + 2H2O(g)����H2
�F(xi��n)��һ������ͬ�l����H2�������ܶȞ�17��NO�cNO2�Ļ�Ϛ��w����16g������w��߀ԭԓ��Ϛ��w��ǡ�����ɵ��⡢������̼?x��)��w��ˮ���⣬���ų�1042.8kJ������
��ԓ��Ϛ��w��NO��NO2�����|(zh��)����֮�Ȟ�
����֪�����ữ�W(xu��)����ʽ�С�H1=��1160kJ/mol���t��H2=
����һ���l����NO���w���Էֽ��NO2���w��N2���w������ԓ����(y��ng)�ğữ�W(xu��)����ʽ ��
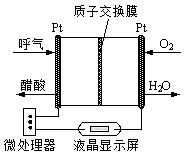
��2���Լ����ȼ�ϵ�����늳أ���ɱ��������Ԛ��ȼ�ϵĂ��y(t��ng)ȼ��늳أ�Ŀǰ�õ��V�����о����D��Ŀǰ�о��^���һ��w������ȼ��늳ع���ԭ��ʾ��D���ش����І��}��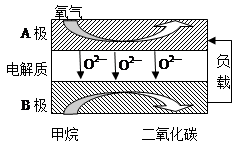
��B�O��늳� �O��늘O����(y��ng)ʽ��
������ԓȼ��늳����Դ����ʯī��늘O늽�100mL 1mol/L�������~��Һ������ꖘO��늘O����(y��ng)ʽ ����(d��ng)�ɘO�ռ����Ě��w�w�e��ȕr����Փ�����ĵļ�����w�e�� ����(bi��o)�r�£������H�����ĵļ����w�e�����㵽��(bi��o)�r������Փ�ϴ���ԭ��� .
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
(14��)CO2��һ�N��Ҫ�Ĝ��Қ��w���о�CO2�����Ì����M(j��n)��̼����Ę�(g��u)��������Ҫ�����x��
��1������ʯ��ʯīȼ������(y��ng)�е�����׃����D��ʾ��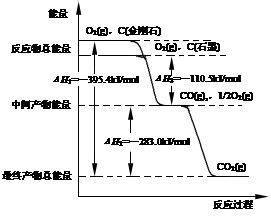
����ͨ����r�£�����ʯ��ʯī�У� �������ʯ����ʯī��������(w��n)����ʯī��ȼ����� kJ��mol��1��
��ʯī�cCO2����(y��ng)����CO�ğữ�W(xu��)����ʽ�� ��
��2������늻��W(xu��)���Ɍ�CO2�D(zhu��n)������顣ԇ�����Ԛ������ˮ��Һ��늽��|(zh��)�r��ԓ�D(zhu��n)����늘O����(y��ng)����ʽ ��
��3��CO2��ԭ��߀�ɺϳɶ�N���|(zh��)�����I(y��)�ϳ���CO2(g) �cH2(g)��ԭ�Ϻϳ��Ҵ���
����֪��H2O(l)=H2O(g) ��H=+44kJ��mol��1
CO(g)+H2O(g) CO2(g)+H2(g) ��H=��41.2kJ��mol��1
CO2(g)+H2(g) ��H=��41.2kJ��mol��1
2CO(g)+4H2 (g)  CH3CH2OH(g)+H2O(g) ��H= ��256.1kJ��mol��1��
CH3CH2OH(g)+H2O(g) ��H= ��256.1kJ��mol��1��
�t��2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(l) ��H= ��
CH3CH2OH(g)+3H2O(l) ��H= ��
���D��һ�N�ԟ������ԭ�Ϻϳ��Ҵ��Ĺ���ԭ��ʾ��D��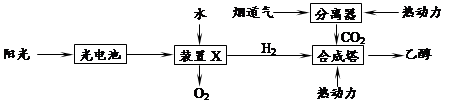
���������̵ķ����������f�����_���� ��
| A��ԓ�������ٰ���4�N��ʽ�������D(zhu��n)�� |
| B���b��X��ꎘO����(y��ng)�飺2H2O��4e��=4H++O2�� |
| C���ϳ����������Ҵ��ķ���(y��ng)�ǻ��Ϸ���(y��ng) |
| D�������O(sh��)Ӌ�w�F(xi��n)�˾Gɫ���W(xu��)˼�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
(1)���������ڃ����՚⡢���ˮ������̎�����I(y��)�U�������Ư�ׄ���
�ٳ��������c���K����㞡�����������І��|(zh��)����(y��ng)���磺
6Ag(s)+O3(g)��3Ag2O(s)����H����235��8 kJ/mol��
��֪��2 Ag2O(s)��4Ag(s)+O2(g)����H��+62.2kJ/mol���tO3�D(zhu��n)����O2�ğữ�W(xu��)����ʽ�� ���ڿƌW(xu��)��P��Tatapudi��������ʹ�������ԗl����늽�ˮ�ķ����Ƶó�����������ꖘO�܇���ˮ�Юa(ch��n)����ꎘO����������t�����^�����䣬ꎘO늘O����(y��ng)ʽ�� ��
| �r�g/min���(mol/L) | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0��30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.l7 |
 N2(g)+CO2(g)��ij�о�С�M��ij���]���������(���O(sh��)�����w�e��׃�����wԇ���w�e���Բ�Ӌ)�м���NO�������Ļ���̿�����(T1��)�l���·���(y��ng)������(y��ng)�M(j��n)�е���ͬ�r�g�y�ø����|(zh��)�ĝ�����£�
N2(g)+CO2(g)��ij�о�С�M��ij���]���������(���O(sh��)�����w�e��׃�����wԇ���w�e���Բ�Ӌ)�м���NO�������Ļ���̿�����(T1��)�l���·���(y��ng)������(y��ng)�M(j��n)�е���ͬ�r�g�y�ø����|(zh��)�ĝ�����£��鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
���I(y��)�����a(ch��n)����⁵ķ����ܶࡣ����F�V����Ҫ�ɷ�FeTiO3����၆�F������Ҫԭ��ұ����������a(ch��n)�Ĺ�ˇ���̈D���£�������F�V�c������l(f��)������(y��ng)�Ļ��W(xu��)����ʽ�飺
FeTiO3��2H2SO4��TiOSO4��FeSO4��2H2O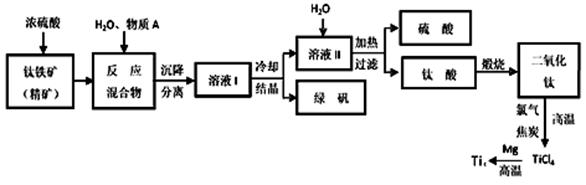
�ش����І��}��
��1����F�V�͝����ᷴ��(y��ng)����______________________ ���x�����߀ԭ����(y��ng)��������߀ԭ����(y��ng)������
��2���������a(ch��n)�����м������|(zh��)A��Ŀ���Ƿ�ֹFe2�������������|(zh��)A��________�������Ƃ�TiO2���^���У����õ��ĸ��a(ch��n)��Ϳɻ������õ����|(zh��)�քe��__________��___________��
��3������(y��ng)TiCl4��2Mg��2MgCl2��Ti��Ar������M(j��n)�������_______________��
��4���ɶ��������ȡ���Ȼ�����漰�ķ���(y��ng)�У�
TiO2 (s)+ 2Cl2 (g) +2C(s) ��TiCl4(g) + 2CO(g) ��H1 = ��72 kJ?mol-1
TiO2(s) + 2Cl2 (g) ��TiCl4(g) + O2 (g) ��H2 =+38.8kJ?mol��1
C(s)��CO2(g)��2CO(g)? ��H3 =+282.8kJ?mol��1
�ٷ���(y��ng)C(s)��CO2(g)��2CO(g)�ڸߜ����܉��l(f��)�M(j��n)�е�ԭ����______________________��
�ڷ���(y��ng)C(s)��O2(g)��CO2 (g)�Ħ�H��_______________��
��5���о��l(f��)�F(xi��n)��������ʯī��ꖘO��⁾W(w��ng)��ꎘO������CaF2-CaO��늽��|(zh��)�������D��ʾ�b�ë@�ý����}�������}��߀ԭ����߀ԭ��������Ƃ������ٌ���ꖘO���l(f��)������(y��ng)��늘O����(y��ng)ʽ��________________________________��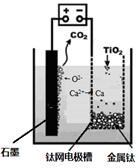
�����Ƃ�����ǰ��CaO�Ŀ�����׃����ԭ���ǣ�Ո�Y(ji��)�ϻ��W(xu��)���Z��ጣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
��֪�w�e��2L�ĺ������]�����аl(f��)������(y��ng)��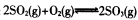 ��Ո����(j��)���W(xu��)����(y��ng)�����P(gu��n)ԭ��ͬ�����І��}
��Ո����(j��)���W(xu��)����(y��ng)�����P(gu��n)ԭ��ͬ�����І��}
��1��һ���l���£�����2 mol SO2��g����2 mol O2��g����20 s�y��SO2���w�e�ٷֺ�����12��5%���t��SO2��ʾԓ����(y��ng)���@20s��(n��i)�ķ���(y��ng)���ʞ�____���˕r��ԓ���]������(n��i)��Ϛ��w�ĉ���(qi��ng)�Ƿ���(y��ng)ǰ��____����
��2������Ĕ����������Дࣨ1���п��淴��(y��ng)�_(d��)��ƽ���B(t��i)����(j��)���ǣ�����̖��____��
��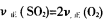
�ڻ�Ϛ��w���ܶȲ�׃
�ۻ�Ϛ��w��ƽ�����������|(zh��)����׃
�ܸ����w�ĝ�ȶ����ٰl(f��)��׃��
��3���D��ʾԓ����(y��ng)�����ʣ�v���S�r�g��t����׃�����P(gu��n)ϵ���t���в�ͬ�r�g���У�SO3�İٷֺ�����ߵ��ǣ� ��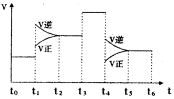

��(j��)�D���������J(r��n)��t3�r��׃�����l�������� ��
t6�r�����w�e��׃���wϵ�г�������SO3���ٴ�ƽ���
SO2���w�e�ٷֺ�����t6�r �����\��С�����ڡ�����
��4���D��P�ǿ�����ƽ�л��ӵĻ���������ͬ�ضȕr����A�����г���4 mol SO3��g�����P(gu��n)�]K����B�����г���2 mol SO3��g�����������քe�l(f��)������(y��ng)��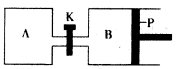
��֪��ʼ�r����A��B���w�e����aL��ԇ�ش�
�ٷ���(y��ng)�_(d��)��ƽ��r����B���w�e��1��2a L������B��SO3�D(zhu��n)
���ʞ�____
�������_K��һ�Εr�g�������_(d��)��ƽ�⣬����B���w�e�� __L���Bͨ���К��w�w�e���Բ�Ӌ���Ҳ����]�ضȵ�Ӱ푣���
��5����֪���|(zh��)���ȼ������H=-296kJ/mol����(j��ng)�y����S��s������120gSO3��g���ɷş�592��5kJ��Ո����SO2��g����������SO3��g���ğữ�W(xu��)����ʽ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�Da��1 mol NO2��1 mol CO����(y��ng)����CO2��NO�^��������׃��ʾ��D���Db�Ƿ���(y��ng)�е�CO��NO�ĝ���S�r�g׃����ʾ��D������(j��)�D��ش����І��}��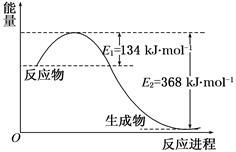
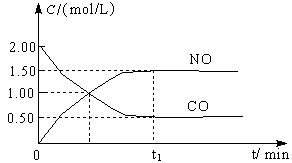
a b
(1)����NO2��CO����(y��ng)�ğữ�W(xu��)����ʽ ��
(2)�ķ���(y��ng)�_ʼ��ƽ�⣬��NO2���׃����ʾƽ������(y��ng)����v(NO2)�� ��
(3)�˜ض���ԓ����(y��ng)��ƽ�ⳣ��(sh��)K= ���ضȽ��ͣ�K ���׃����׃С����׃����
(4)���ڜضȺ��ݷe��ͬ���������]�����У�����ͬ��ʽͶ�뷴��(y��ng)��y�÷���(y��ng)�_(d��)��ƽ�ⅼ�����P(gu��n)��(sh��)��(j��)���±���
| �� �� | �� | �� | �� |
| ����(y��ng)��Ͷ���� | 1 mol NO2 1 mol CO | 2 mol NO 2 mol CO2 | 1 mol NO2��1 mol CO 1 mol NO��1 mol CO2 |
| ƽ��rc(NO) /mol��L-1 | 1.5 | 3 | m |
| ����׃�� | �ų�a kJ | ����b kJ | �ų�c kJ |
| CO��NO���D(zhu��n)���� | ��1 | ��2 | ��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�ؾ�ʯ��BaSO4������Ҫ�Ļ���ԭ�ϣ��Ƃ�������^���w[Ba(OH)2��8H2O]���������£�
��1�������џ��r�l(f��)������(y��ng)�ğữ�W(xu��)����ʽ��____________________________��
��2�������������^���w�c�Ȼ��@���w��Ϸ���(y��ng)�Ļ��W(xu��)����ʽ��_____________________��
��3����z�y�џ��r�a(ch��n)����CO���Ɍ��џ��a(ch��n)���Ě��wͨ��PbCl2��Һ�У����F(xi��n)��ɫ�����ͮa(ch��n)��һ�N�oɫ�oζ��ʹ����ʯ��ˮ׃����Ě��w��ԇ����ԓ����(y��ng)�Ļ��W(xu��)����ʽ��_____��
��4����BaSO4�����м����Na2CO3��Һ�����?j��n)��裬��ȥ�ό���Һ�����̎����Σ���ʹBaSO4ȫ���D(zhu��n)����BaCO3���l(f��)���ķ���(y��ng)�ɱ�ʾ�飺
BaSO4(s)+CO32��(aq) BaCO3(s)+SO42��(aq)
BaCO3(s)+SO42��(aq)
�F(xi��n)��0.20 mol BaSO4������1.0L 2.0mol?L��1�Na2CO3��Һ̎�������O(sh��)c(SO42��)��ʼ��0
ƽ��r��K=4.0x10��2����(y��ng)�_(d��)��ƽ��r�l(f��)���D(zhu��n)����BaSO4�����|(zh��)������(����Ӌ���^�̽Y(ji��)������2λ��Ч��(sh��)��)
��5��ԇ��ƽ��ĽǶȽ��BaSO4���D(zhu��n)����BaCO3��ԭ��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ������}
��14�֣�
���\�i�U늳��е�̼������̼�ۡ�Fe��Cu��Ag��MnO2�����|(zh��) ����ԭ�ϻ���MnO2�Ĺ�ˇ�������£�
I. ��̼�������|(zh��)��ɣ�������ϡHNO3�ܽ���ن��|(zh��)���^�V���ÞV��a��
II. ���V��a�ڿ՚����Ɵ���ȥ̼�ۣ��õ���MnO2��
III.���MnO2�м�������H2O2��Һ��MnO2�ܽ�����Mn2+���К��w���ɣ�
IV. ��III������Һ��pH�s��6���о����μ�0.50 mol?L-1 Na2CO3��Һ���^�V���ÞV��b������Ҫ�ɷ֞�MnCO3��
V. �V��b��(j��ng)ϴ�졢����Ɵ����Ƶ��^����MnO2��
��1������Ag�c����ϡHNO3����(y��ng)����NO�Ļ��W(xu��)����ʽ�� ��
��2����֪II���Ɵ��^����ͬ�r�l(f��)������(y��ng)��
MnO2(s) + C(s) ="==" MnO(s) + CO (g) ��H = +24.4kJ ? mol �C1 ��
MnO2(s) + CO(g) ="==" MnO(s) + CO2(g) ��H = -148.1 kJ ? mol �C1 ��
����MnO2��C����(y��ng)����MnO��CO2�ğữ�W(xu��)����ʽ�� ��
��3��H2O2�����к��еĻ��W(xu��)�I��͞� �� ��
��4��III��MnO2�ܽ���x�ӷ���ʽ�� ���ܽ�һ������MnO2��H2O2�Č��H����������Փֵ�ߣ��û��W(xu��)����ʽ���ԭ�� ��
��5��IV�У����Ğ顰��0.50 mol?L-1 Na2CO3��Һ�о����μ�III������Һ�����V��b�Е������^��Mn(OH)2�����������ԭ�� ��
��6��V��MnCO3�ڿ՚����Ɵ��Ļ��W(xu��)����ʽ�� ��
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com