
【題目】短周期元素A、B、C、D、E、F的原子序數逐漸增大,A和B同周期,A和F同族,A原子最外層電子數是內層電子數的二倍,B元素族序數是周期數的三倍,B的簡單陰離子與C、D、E的簡單陽離子電子層結構相同.請回答下列有關問題:
(1)F在元素周期表中的位置是 .
(2)C2B2的電子式是;AB2的結構式是 .
(3)B、C、D、E離子半徑由大到小的順序為(用離子符號回答); C、D、E最高價氧化物對應水化物的堿性由強到弱的順序為(用化學式表示,且用“>”符號連接回答).
(4)C、E最高價氧化物對應水化物能夠相互反應,則反應的離子方程式為 .
【答案】
(1)第三周期第ⅣA族
(2)![]() ;O=C=O
;O=C=O
(3)O2﹣>Na+>Mg2+>Al3+;NaOH>Mg(OH)2>Al(OH)3
(4)Al(OH)3+OH﹣=AlO2﹣+2 H2O
【解析】解:(1)硅在元素周期表中的位置是第三周期第ⅣA族,所以答案是:第三周期第ⅣA族;(2)過氧化鈉的電子式是 ![]() ;二氧化碳的結構式是O=C=O,所以答案是:
;二氧化碳的結構式是O=C=O,所以答案是: ![]() ; O=C=O;(3)電子層數越多,離子半徑越大,電子層數相同時,核電荷數越多,離子半徑越小,所以B、C、D、E離子半徑的由大到小的順序為O2﹣>Na+>Mg2+>Al3+ , 元素的金屬性越強,對應的最高價氧化物對應水化物的堿性就越強,金屬性Na>Mg>Al,所以堿性NaOH>Mg(OH)2>Al(OH)3 , 所以答案是:O2﹣>Na+>Mg2+>Al3+; NaOH>Mg(OH)2>Al(OH)3;(4)鈉、鋁最高價氧化物對應水化物能夠相互反應,即氫氧化鈉和氫氧化鋁反應,其離子方程式為Al(OH)3+OH﹣=AlO2﹣+2 H2O,所以答案是:Al(OH)3+OH﹣=AlO2﹣+2 H2O.
; O=C=O;(3)電子層數越多,離子半徑越大,電子層數相同時,核電荷數越多,離子半徑越小,所以B、C、D、E離子半徑的由大到小的順序為O2﹣>Na+>Mg2+>Al3+ , 元素的金屬性越強,對應的最高價氧化物對應水化物的堿性就越強,金屬性Na>Mg>Al,所以堿性NaOH>Mg(OH)2>Al(OH)3 , 所以答案是:O2﹣>Na+>Mg2+>Al3+; NaOH>Mg(OH)2>Al(OH)3;(4)鈉、鋁最高價氧化物對應水化物能夠相互反應,即氫氧化鈉和氫氧化鋁反應,其離子方程式為Al(OH)3+OH﹣=AlO2﹣+2 H2O,所以答案是:Al(OH)3+OH﹣=AlO2﹣+2 H2O.


 金鑰匙試卷系列答案
金鑰匙試卷系列答案科目:高中化學 來源: 題型:
【題目】某實驗室合成了一種可溶的金屬氯化物(RClx),為了測定該金屬氯化物的成分,研究人員做了以下實驗:取物質的量濃度為0.05molL﹣1的金屬氯化物(RClx) 溶液20mL,使之恰好與20mL 0.15molL﹣1的AgNO3溶液完全反應.則該氯化物的化學式為( )
A.RCl
B.RCl2
C.RCl3
D.RCl4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下向10 mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的變化曲線如圖所示。下列說法正確的是( )

A. a 點所示溶液中 c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b 兩點所示溶液中水的電離程度相問
C. b點所示溶液中c(A-)>c(HA)
D. pH=7時,c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組以烴A為主要原料,采用以下路線合成藥物X和高聚物Y:

已知: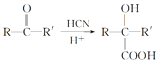 (R或R′可以是烴基或H原子)。
(R或R′可以是烴基或H原子)。
請回答下列問題:
(1)X的分子式為____________,X中的含氧官能團有____________。
(2)若反應①、反應②的原子利用率均為100%,則A的名稱為________。
(3)E的結構簡式為________________,反應③的條件是________,反應⑤的反應類型是________。
(4)寫出反應④的化學方程式: ___________________________________。
(5)寫出同時符合下列條件的E的所有同分異構體的結構簡式:________。
①屬于酚類化合物,且是苯的對位二元取代物;
②能發生銀鏡反應和水解反應。
(6)以CH3CHO為原料可合成Y,請設計合成路線(無機試劑及溶劑任選)____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】肼(N2H4)是一種高能燃料,常溫下為無色具有強烈的吸水性的有毒液體。熔點(2℃),沸點(113.5℃)。N2H4水溶液的堿性弱于氨水;N2H4有強還原性。化學小組同學在實驗室中用過量NH3和NaC1O溶液反應制取N2H4并探究其性質。回答下列問題:

(1)A中反應容器的名稱為_____________
(2)用上圖裝置制取肼,其連接順序為________(按氣流方向,用小寫字母表示)。
(3)裝置A中生成N2H4·H2O,則發生反應的化學方程式為_________________,裝置D的作用是_______________。
(4)用化學用語解釋N2H4水溶液呈堿性的原因:__________________________________
(5)發射火箭時,肼為燃料,雙氧水為氧化劑,兩者反應生成氮氣和氣態水。已知1.6g液態肼 在上述反應中釋放64.22kJ 的熱量,寫出該反應的熱化學方程式:_______________________
(6)將A中得到的粗產品和燒堿混合,逐漸通入氮氣以除空氣,目的為_______________加熱至堿液溫度近110℃,待燒堿完全溶解后,冷卻到60℃左右,進行 至蒸餾液含肼量90%~94%,再經分餾、除去水分后,冷凝,制得98%~99.5%的無水肼。則空白處應填寫(_____)
A.加壓蒸餾 B.常壓蒸餾 C.真空蒸餾
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,反應C(s)+H2O(g)![]() CO(g)+H2(g)在密閉容器中進行,下列條件的改變對其反應
CO(g)+H2(g)在密閉容器中進行,下列條件的改變對其反應
速率幾乎無影響的是
A. 增加CO的量
B. 將容器的體積縮小一半
C. 保持體積不變,充入N2使體系壓強增大
D. 保持壓強不變,充入N2使容器體積變大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000 mol/L
CH3COOH溶液滴定曲線如右圖。下列說法正確的是

A. 點①所示溶液中:c(CH3COO-)+ c(OH-) =c(CH3COOH)+ c(H+)
B. 點②所示溶液中:c(Na+) =c(CH3COOH)+ c(CH3COO-)
C. 點③所示溶液中:c(Na+)> c(OH-)> c(CH3COO-)> c(H+)
D. 滴定過程中可能出現:c(CH3COOH)> c(CH3COO-)> c(H+)> c(Na+)> c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有反應 3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g),在一體積可調的密閉容器中進行,采取下列措施對其反應速率幾乎無影響的是( )
Fe3O4(s)+4H2(g),在一體積可調的密閉容器中進行,采取下列措施對其反應速率幾乎無影響的是( )
A.增加H2的量
B.將容器體積縮小一半
C.保持容器內體積不變,充入Ar使體系壓強增大
D.充入Ar,保持容器內壓強不變
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com