
(14分)為回收利用廢釩催化劑(含有V2O5、VOSO4及不溶性殘渣),科研人員最新研制了一種離子交換法回收釩的新工藝,主要流程如下:
部分含釩物質在水中的溶解性如下:
| 物質 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 難溶 | 難溶 | 易溶 |

 VO2++H2O+V3+,電池充電時陽極的電極反應式為 。
VO2++H2O+V3+,電池充電時陽極的電極反應式為 。 ⑴3V2O5+10Al=5Al2O3+6V ⑵VOSO4
⑶NH4+ +VO3—= NH4VO3↓ 4 80 ℃
⑷2VO2+ +H2C2O4+2H+ = 2VO2++2CO2↑+2H2O
⑸VO2++H2O-e-= VO2+ +2H+ (2,2,2,2,2,2,2)
解析試題分析:⑴用鋁熱劑法冶煉金屬釩,反應物有V2O5和Al,生成物有V和Al,可采用化合價升降法將其配平。
⑵根據表中的信息知,只有VOSO4溶于水,故濾液中含釩的主要成分為VOSO4。
⑶根據表中的信息知,NH4VO3難溶于水,故該工藝中反應③為NH4+ 與VO3—反應生成NH4VO3沉淀。
通過觀察兩圖知控制氯化銨系數(shù)為4(太大時釩的沉淀率提高不大,但導致銨鹽的利用率不高),控制溫度為80 ℃(該溫度下釩的沉淀率最高)。
⑷首先根據得失電子守恒有2VO2+ +H2C2O4―― 2VO2++2CO2↑,再根據電荷守恒有2VO2+ +H2C2O4+2H+ ――2VO2++2CO2↑(用硫酸酸化,添加H+滿足電荷守恒),最后根據原子守恒得2VO2+ +H2C2O4+2H+ = 2VO2++2CO2↑+2H2O。
⑸電池充電時陽極上VO2+發(fā)生氧化反應生成VO2+ ,首先根據得失電子守恒有VO2+-e―――VO2+ ,再根據電荷守恒有VO2+-e――― VO2+ +2H+,最后根據原子守恒得VO2++H2O-e-= VO2+ +2H+。
考點:本題以回收釩的化工流程圖為素材,考查化學方程式、離子方程式、電極反應式等的配平與書寫,以及讀圖能力。


 學而優(yōu)銜接教材南京大學出版社系列答案
學而優(yōu)銜接教材南京大學出版社系列答案 小學課堂作業(yè)系列答案
小學課堂作業(yè)系列答案 金博士一點全通系列答案
金博士一點全通系列答案科目:高中化學 來源: 題型:單選題
在化學能與電能的轉化過程中,下列敘述正確的是 ( )
| A.電解飽和食鹽水時,陽極得到Cl2 和NaOH(aq) |
| B.教材所示的銅-鋅原電池在工作時,Zn2+ 向銅片附近遷移 |
| C.電鍍時,電鍍槽里的負極材料發(fā)生氧化反應 |
| D.原電池與電解池連接后,電子從原電池負極流向電解池陽極 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)利用如圖裝置,可以模擬鐵的電化學防護。若X為碳棒,為減緩鐵的腐蝕,開關K應該置于 處。若X為鋅,開關K置于M處,該電化學防護法稱為 。
(2)肼(N2H4)又稱聯(lián)氨,是一種可燃性液體,其燃燒熱較大且燃燒產物對環(huán)境無污染,故可以用作火箭燃料。肼—空氣燃料電池是一種堿性燃料電池,電解質溶液是20%—30%的KOH溶液。該電池放電時,通入肼的一極為 極,該極的電極反應式是 ,電池工作一段時間后,電解質溶液的pH將 (填“增大”、“減小”、“不變”)。
(3)碘被稱為 “智力元素”,科學合理地補充碘可防止碘缺乏病。碘酸鉀(KIO3)是國家規(guī)定的食鹽加碘劑,它的晶體為白色,可溶于水。碘酸鉀在酸性介質中與過氧化氫或碘化物作用均生成單質碘。以碘為原料,可通過電解制備碘酸鉀。(陰、陽兩極均用惰性電極,陰極室與陽極室用陽離子交換膜隔開)請回答下列問題:電解前,先將一定量的精制碘溶于過量氫氧化鉀溶液,溶解時發(fā)生反應:
3I2+6KOH=5KI+KIO3+3H2O,將該溶液加入陽極區(qū)。另將氫氧化鉀溶液加入陰極區(qū),電解槽用水冷卻。電解時,陽極上發(fā)生反應的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(13分)(1)將鋅、銅用導線連接后浸入2mol/L的稀硫酸中,正極電極反應式為_________________,發(fā)生 反應(填氧化或還原);電子從 經外電路到 (填鋅或銅),溶液中H+ 向 移動(填正極或負極)。
(2)根據反應2Fe3+ + Cu = 2Fe2++Cu2+ 設計原電池,所需負極材料為 ,溶液中Fe3+向 (填“負極”或“正極”)遷移,負極反應式為 ;正極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(9分)鋰錳電池的體積小、性能優(yōu)良,是常用的一次電池。該電池反應原理如圖所示,其中電解質LiCIO4。溶于混合有機溶劑中,Li+通過電解質遷移入MnO2晶格中,生成LiMnO2。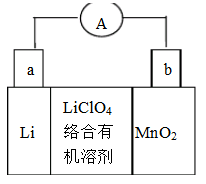
回答下列問題:
(1)外電路的電流方向是由____極流向____極。(填字母)
(2)電池正極反應式為____。
(3)是否可用水代替電池中的混合有機溶劑?____(填“是”或“否”),原因是____________。
(4)MnO2可與KOH和KClO3,在高溫下反應,生成K2MnO4,反應的化學方程式為_______________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物質的量之比為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(6分)(1)甲烷通常用來作燃料,其燃燒反應的化學方程式是 。
(2) 若用甲烷—氧氣構成燃料電池,電解質溶液為KOH溶液,試寫出該電池的正極的電極反應式 ;負極的電極反應式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(9分)
新型高效的甲烷燃料電池采用鉑為電極材料,兩電極上分別通入CH4和O2 ,電解質為KOH溶液。某研究小組將兩個甲烷燃料電池串聯(lián)后作為電源,進行飽和氯化鈉溶液電解實驗,如圖所示。
回答下列問題:
(1)甲烷燃料電池正極、負極的電極反應分別為 、 。
(2)閉合K開關后,a、b電極上均有氣體產生.其中b電極上得到的是 ,電解氯化鈉溶液的總反應方程式為 ;
(3)若每個電池甲烷通入量為1 L(標準狀況),且反應完全,則理論上通過電解池的電量為
(法拉第常數(shù)F=9.65×l04C.mol-1,列式計算),最多能產生的氯氣體積為 L(標準狀況)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一個U形管里盛有CuCl2溶液,并插入兩塊鋅片作電極,按如圖連接。
(1)如果把電鍵K接A,該裝置應是電解裝置,Zn①極是 極,電極反應式為 ,Zn②極是 極,電極反應式為 。
(2)上述反應進行5 min后,轉換電鍵K到C,則這個裝置是原電池裝置,Zn①極是 極,電極反應式為 。
(3)上述裝置進行2 min后,再轉換電鍵K到B,則Zn①極發(fā)生的化學反應為 ,Zn②極發(fā)生的有關電化學的反應為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如圖所示,用石墨電極電解氯化銅溶液。查閱資料可知,CuCl42—顯黃色,氯化銅溶液顯藍綠色或黃綠色;向體積相同濃度分別為0.01 mol/L、0.05 mol/L、0.1 mol/L、0.5 mol/L的氯化銅溶液中加入NaCl至飽和,對比發(fā)現(xiàn),溶液的顏色由黃綠色向藍綠色轉變。
請回答下列問題:
(1)陽極上的氣體呈________色,檢驗該氣體可用________________。
(2)寫出電解的離子方程式:________________。
(3)實驗時,裝置中陰極溶液顏色由藍綠色變?yōu)辄S綠色,原因是________。
(4)取出陰極的石墨棒,發(fā)現(xiàn)表面有淺藍色固體,試設計實驗探究此淺藍色固體的成分:
____________________________________________________。
(5)為什么要設計連接后面的裝置?
______________________________________________________________
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com