
Ž┬┴ąšfĘ©š²┤_Ą─╩ŪŻ© Ż®
| AŻ«ėąą®╬’┘|(zh©¼)╩Ūė╔įŁūėų▒Įėśŗ(g©░u)│╔Ż¼╚ń╦«Š¦ĪóĮäé╔░Ą╚Ż╗ėąą®╬’┘|(zh©¼)╩Ūė╔Ęųūėų▒Įėśŗ(g©░u)│╔Ż¼╚ńĖ╔▒∙Īó├„Ą\Ą╚Ż╗ėąą®╬’┘|(zh©¼)╩Ūė╔ļxūėų▒Įėśŗ(g©░u)│╔Ą─Ż¼╚ń®Ą\Īó├󎧥╚ |
| BŻ«BF3ĪóH2OĪóSiCl4ĪóPCl5╦─ĘNĘųūėųą╦∙ėąįŁūėČ╝ØMūŃūŅ═Ōīė8ļŖūėĮY(ji©”)śŗ(g©░u) |
| CŻ«ĘŪĮī┘č§╗»╬’▓╗Č╝╩Ū╦ßąįč§╗»╬’Ż╗Įī┘č§╗»╬’▓╗Č╝╩ŪēAąįč§╗»╬’ |
| DŻ«─“╦žĄ─╚█³c▒╚┤ū╦ߥ─╚█³cĖ▀Ż¼▀@╩Ūė╔ė┌Ū░š▀▒╚║¾š▀ėąĖ³┤¾Ą─ĘČĄ┬╚A┴”╦∙ų┬ |
 ╠ņ╠ņŽ“╔Žę╗▒Š║├ŠĒŽĄ┴ą┤░Ė
╠ņ╠ņŽ“╔Žę╗▒Š║├ŠĒŽĄ┴ą┤░Ė ąĪīW(xu©”)╔·10ĘųńŖæ¬(y©®ng)ė├Ņ}ŽĄ┴ą┤░Ė
ąĪīW(xu©”)╔·10ĘųńŖæ¬(y©®ng)ė├Ņ}ŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
╝ū═ķĘųūėŻ©CH4Ż®╩¦╚źę╗éĆHŻ½Ż¼ą╬│╔╝ū╗∙ĻÄļxūėŻ©CH3ŻŁŻ®Ż¼į┌▀@éĆ▀^│╠ųąŻ¼Ž┬┴ą├Ķ╩÷▓╗║Ž└ĒĄ─╩ŪŻ© Ż®
| AŻ«╠╝įŁūėĄ─ļs╗»ŅÉą═░l(f©Ī)╔·┴╦Ė─ūā |
| BŻ«╬ó┴ŻĄ─ą╬ĀŅ░l(f©Ī)╔·┴╦Ė─ūā |
| CŻ«╬ó┴ŻĄ─ĘĆ(w©¦n)Č©ąį░l(f©Ī)╔·┴╦Ė─ūā |
| DŻ«╬ó┴ŻųąĄ─µIĮŪ░l(f©Ī)╔·┴╦Ė─ūā |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ĻP(gu©Īn)ė┌╗»īW(xu©”)µIĄ─öó╩÷ųąŻ¼š²┤_Ą─╩Ū
| AŻ«ļxūė╗»║Ž╬’┐╔─▄║¼╣▓ārµI | BŻ«╣▓ār╗»║Ž╬’┐╔─▄║¼ļxūėµI |
| CŻ«ļxūė╗»║Ž╬’ųąų╗║¼ļxūėµI | DŻ«ļxūė╗»║Ž╬’ųąę╗Č©║¼ėąĮī┘ļxūė |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąĖ„ĘNšfĘ©ųąę╗Č©š²┤_Ą─╩Ū( )
| AŻ«▀^Č╔Įī┘Ą─įŁūė╗“ļxūėę╗░ŃČ╝ėąĮė╩▄╣┬ļŖūėī”Ą─┐š▄ēĄ└Ż¼ęūą╬│╔┼õ║Ž╬’ |
| BŻ«ųąą─įŁūė╗“ļxūė▓╔╚Īsp3ļs╗»▄ēĄ└ą╬│╔Ą─┼õļxūėŠ∙│╩š²╦─├µ¾wĮY(ji©”)śŗ(g©░u) |
| CŻ««ö(d©Īng)ųąą─įŁūė╗“ļxūėĄ─┼õ╬╗öĄ(sh©┤)×ķ6ĢrŻ¼┼õļxūėę╗Č©│╩░╦├µ¾wĮY(ji©”)śŗ(g©░u) |
| DŻ«║¼ėąā╔ĘN┼õ╬╗¾wŪę┼õ╬╗öĄ(sh©┤)×ķ4Ą─┼õļxūėę╗Č©┤µį┌ĒśĘ┤«Éśŗ(g©░u)¾w |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
▒▒Š®┤¾īW(xu©”)║═ųąć°┐ŲīW(xu©”)į║Ą─╗»īW(xu©”)╣żū„š▀ęč│╔╣”čąųŲ│÷ēAĮī┘┼cC60ą╬│╔Ą─Ū“╠╝¹}K3C60Ż¼īŹ“×£yų¬įō╬’┘|(zh©¼)ī┘ė┌ļxūė╗»║Ž╬’Ż¼Š▀ėą┴╝║├Ą─│¼ī¦(d©Żo)ąįĪŻŽ┬┴ąėąĻP(gu©Īn)Ęų╬÷š²┤_Ą─╩ŪŻ© Ż®
| AŻ«K3C60ųąų╗ėąļxūėµI |
| BŻ«K3C60ųą▓╗║¼╣▓ārµI |
| CŻ«įōŠ¦¾wį┌╚█╚┌ĀŅæB(t©żi)Ž┬─▄ī¦(d©Żo)ļŖ |
| DŻ«C60┼c12C╗ź×ķ═¼╦ž«Éą╬¾w |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
PH3╩Ūę╗ĘN¤o╔½äĪČŠÜŌ¾wŻ¼ŲõĘųūėĮY(ji©”)śŗ(g©░u)║═NH3ŽÓ╦ŲŻ¼Ą½PĪ¬HµIµI─▄▒╚NĪ¬HµIµI─▄Ą═ĪŻŽ┬┴ą┼ąöÓš²┤_Ą─╩Ū (ĪĪĪĪ)ĪŻ
| AŻ«PH3Ęųūė│╩ŲĮ├µ╚²ĮŪą╬ |
| BŻ«PH3Ęųūė╩ŪśOąįĘųūė |
| CŻ«PH3Ęą³cĄ═ė┌NH3Ęą³cŻ¼ę“×ķPĪ¬HµIµI─▄Ą═ |
| DŻ«PH3ĘųūėĘĆ(w©¦n)Č©ąįĄ═ė┌NH3ĘųūėŻ¼ę“×ķNH3Ęųūėų«ķg┤µį┌ÜõµI |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
H2O┼cH2SĮY(ji©”)śŗ(g©░u)ŽÓ╦ŲŻ¼Č╝╩ŪVą╬Ą─śOąįĘųūėŻ¼Ą½╩ŪH2OĄ─Ęą³c╩Ū100 ĪµŻ¼H2SĄ─Ęą³c╩ŪŻŁ60.7 ĪµŻ¼ę²Ų▀@ĘN▓Ņ«ÉĄ─ų„ę¬įŁę“╩ŪŻ© Ż®ĪŻ
| AŻ«ĘČĄ┬╚A┴” | BŻ«╣▓ārµI | CŻ«ÜõµI | DŻ«ŽÓī”Ęųūė┘|(zh©¼)┴┐ |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąĘ┤æ¬(y©®ng)▀^│╠ųąŻ¼═¼ĢrėąļxūėµIĪóśOąį╣▓ārµI║═ĘŪśOąį╣▓ārµIĄ─öÓ┴č║═ą╬│╔Ą─Ę┤æ¬(y©®ng)╩ŪŻ© Ż®ĪŻ
AŻ«NH4Cl NH3Ī³Ż½HClĪ³ NH3Ī³Ż½HClĪ³ |
| BŻ«NH3Ż½CO2Ż½H2O=NH4HCO3 |
| CŻ«2NaOHŻ½Cl2=NaClŻ½NaClOŻ½H2O |
| DŻ«2Na2O2Ż½2CO2=2Na2CO3Ż½O2 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW(xu©”) üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąšfĘ©š²┤_Ą─╩ŪŻ© Ż®ĪŻ
| AŻ«µIĮŪøQČ©┴╦ĘųūėĄ─ĮY(ji©”)śŗ(g©░u) |
| BŻ«╣▓ārµIĄ─µI─▄įĮ┤¾Ż¼╣▓ārµIįĮ└╬╣╠Ż¼║¼ėąįōµIĄ─ĘųūėįĮĘĆ(w©¦n)Č© |
| CŻ«CH4ĪóCCl4ųąµIķLŽÓĄ╚Ż¼µIĮŪ▓╗═¼ |
DŻ«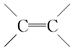 ųąĄ─µI─▄╩ŪCĪ¬CųąĄ─µI─▄Ą─ā╔▒Č ųąĄ─µI─▄╩ŪCĪ¬CųąĄ─µI─▄Ą─ā╔▒Č |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīW(xu©”)ąŻā×(y©Łu)▀x - ŠÜ┴Ģ(x©¬)āį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ō(li©ón)ŠW(w©Żng)▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW(w©Żng)╔Žėą║”ą┼Žó┼eł¾īŻģ^(q©▒) | ļŖą┼įp“_┼eł¾īŻģ^(q©▒) | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^(q©▒) | ╔µŲ¾ŪųÖÓ(qu©ón)┼eł¾īŻģ^(q©▒)
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com