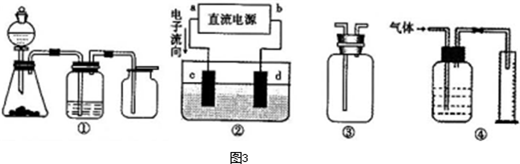
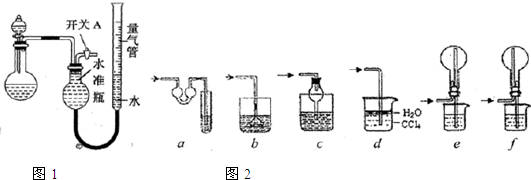
解答:解:(1)分液漏斗用于氣體發生器中控制加液,也常用于互不相溶的幾種液體的分離,加液時要注意內外空氣相通,壓強相等,液體才能順利流下,具體操作為:打開分液漏斗上口的活塞(或將活塞上的凹槽與瓶口上的小孔對齊),旋開分液漏斗的旋塞,緩慢滴加;
故答案為:打開分液漏斗上口的活塞(或將活塞上的凹槽與瓶口上的小孔對齊),旋開分液漏斗的旋塞,緩慢滴加;
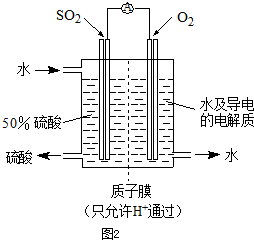
(2)一氧化氮與氧氣反應生成二氧化氮,二氧化氮可與水反應生成一氧化氮和硝酸;裝置Ⅰ中有空氣,一氧化氮會與裝置中的空氣反應,生成的二氧化氮溶于水并與水反應,使測得的一氧化氮體積不準,所以不可以通過實驗I收集并測量NO氣體的體積來探究銅樣品的純度,
故答案為:NO會與裝置中空氣反應,生成NO
2溶于水,使測得的NO氣體體積不準;
(3)實驗室用電石和水來制取乙炔,反應原理為:CaC
2+2H
2O→Ca(OH)
2+C
2H
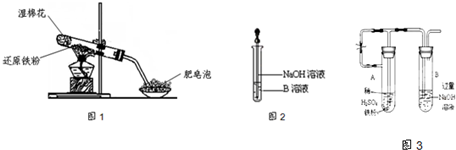
2↑,乙炔可以燃燒,乙炔燃燒時,火焰明亮并伴有濃烈的黑煙,這是因為乙炔中含碳的質量分數比乙烯高,碳沒有完全燃燒的緣故,
故答案為:CaC
2+2H
2O→Ca(OH)
2+C
2H
2↑;火焰明亮并伴有濃烈的黑煙;
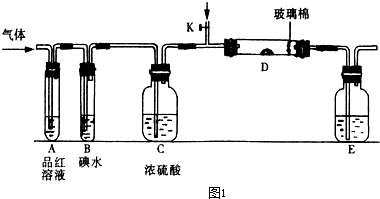
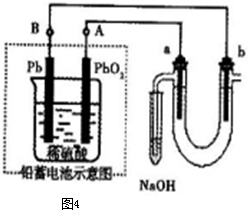
(4)氨氣為堿性氣體,極易溶于水,量氣管中的液體應該不含水且不與氨氣反應,濃NaOH溶液、氨水、氯化銨溶液中含有水,氨氣被水吸收,而氨氣不溶于煤油,所以量氣管中液體最好是煤油;
a、對于極易溶于水的氣體,吸收裝置中的導管外聯雙球狀導管內伸入到液體中,液體進入雙球內,防止進入前端裝置,能防止倒吸,故a正確;
b、吸收裝置中的導管下聯漏斗,漏斗口伸入液面以下,易吸收易溶性氣體,不能防止倒吸,故b錯誤;
c、對于極易溶于水的氣體,吸收裝置中的導管與干燥管連接,當水進入干燥管內,燒杯內液面下降低于導管口,液體又流落到燒杯中,能防止倒吸,故c正確;
d、氨氣極易溶于水,不溶于四氯化碳,所以導管通入四氯化碳中,氣泡向上到水層溶解,能防止倒吸,故d正確;
e、氨氣極易溶于水,導管插入溶液中形成噴泉,進氣管在燒瓶口,液體經進氣管倒流入前端裝置,產生倒吸,故e錯誤;
f、氨氣極易溶于水,導管插入溶液中形成噴泉,進氣管在燒瓶底部,液體不能流入前端裝置,能防止倒吸,故f正確;
所以能防倒吸的吸收裝置有acdf,
故答案為:c; a、c、d、f;
(5)根據PV=nRT,為保證測出來的氣體體積是當時大氣壓下的體積,在讀數時應注意:①將實驗裝置恢復到室溫,②使量氣管兩端液面相平,因為相平說明兩邊液面上的壓強是一樣的,這樣測出來的氣體體積才是當時大氣壓下的體積,③視線與凹液面最低處相平,俯視或仰視會造成誤差,
故答案為:使量氣管和水準瓶兩端液面相平;
(6)第2次測量數據誤差較大,可不用,鋁和氫氧化鈉反應生成氫氣的體積=
| (346.3-10.0)+(345.7-10.0) |
| 2 |
=336.0mL=0.336L
設生成0.336L氫氣,需鋁的質量為x
2Al+2NaOH+2H
2O═2NaAlO
2+3H
2↑
54g 3×22.4L
x 0.336L
=
,解之得:x=0.27g
鋁的質量分數=
×100%=27.0%,
故答案為:27.0%.



 世紀百通主體課堂小學課時同步達標系列答案
世紀百通主體課堂小學課時同步達標系列答案 世紀百通優練測系列答案
世紀百通優練測系列答案