
ĪŠŅ}─┐Ī┐Ė∙ō■ĄŌ┼cÜõÜŌĘ┤æ¬Ą─¤ß╗»īWĘĮ│╠╩ĮŽ┬┴ą┼ąöÓš²┤_Ą─╩Ū

AŻ«254g I2(g)ųą═©╚ļ2g H2(g)Ż¼Ę┤æ¬Ę┼¤ß9.48 kJ
BŻ«1 mol╣╠æBĄŌ┼c1 molÜŌæBĄŌ╦∙║¼Ą──▄┴┐ŽÓ▓Ņ17Ż«00 kJ
CŻ«Ę┤æ¬ó┘Ą─«a╬’▒╚Ę┤æ¬ó┌Ą─«a╬’ĘĆČ©
DŻ«Ę┤æ¬ó┌Ą─Ę┤æ¬╬’┐é─▄┴┐▒╚Ę┤æ¬ó┘Ą─Ę┤æ¬╬’┐é─▄┴┐Ą═
ĪŠ┤░ĖĪ┐D
ĪŠĮŌ╬÷Ī┐
įćŅ}Ęų╬÷Ż║ęčų¬Ż║ó┘I2(g)+H2(g)2HI(g)Ī„H=-9.48kJmol-1Ż╗ó┌I2(s)+H2(g)2HI(g)Ī„H=+26.48kJmol-1Ż¼└¹ė├╔w╦╣Č©┬╔īóó┘-ó┌┐╔Ą├I2(g)=I2(s)Ī„H=-9.48kJmol-1-26.48kJmol-1=-35.96kJmol-1ĪŻAŻ«n(I2)=1moLŻ¼n(H2)=1molŻ¼ė╔ė┌įōĘ┤æ¬×ķ┐╔─µĘ┤æ¬Ż¼ätĘ┼│÷Ą─¤ß┴┐ąĪė┌9.48kJŻ¼╣╩AÕeš`Ż╗BŻ«ė╔I2(g)=I2(s)Ī„H=-35.96kJmol-1Ż¼┐╔ų¬1mol╣╠æBĄŌ┼c1molÜŌæBĄŌ╦∙║¼Ą──▄┴┐ŽÓ▓Ņ35.96kJŻ¼╣╩BÕeš`Ż╗CŻ«Ę┤æ¬ó┘Īóó┌Ą─«a╬’Č╝╩ŪHIŻ¼ĀŅæBŽÓ═¼Ż¼ĘĆČ©ąįŽÓ═¼Ż¼╣╩CÕeš`Ż╗DŻ«ė╔I2(g)=I2(s)Ī„H=-35.96kJmol-1Ż¼┐╔ų¬I2(g)─▄┴┐┤¾ė┌I2(s)Ż¼╣╩Dš²┤_Ż╗╣╩▀xDĪŻ


 ķåūx┐ņ▄接┴ą┤░Ė
ķåūx┐ņ▄接┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ęčų¬╦ßąįK2Cr2O7╚▄ę║┐╔┼cFeSO4Ę┤æ¬╔·│╔Fe3Ż½║═Cr3Ż½ĪŻ¼Fīó┴“╦ß╦ß╗»Ą─K2Cr2O7╚▄ę║┼cFeSO4╚▄ę║╗ņ║ŽŻ¼│õĘųĘ┤æ¬║¾į┘Ž“╦∙Ą├╚▄ę║ųą╝ė╚ļKI╚▄ę║Ż¼╗ņ║Ž╚▄ę║ųąFe3Ż½Ą─╬’┘|Ą─┴┐ļS╝ė╚ļĄ─KIĄ─╬’┘|Ą─┴┐Ą─ūā╗»ĻPŽĄ╚ńłD╦∙╩ŠŻ¼Ž┬┴ąšfĘ©ųą▓╗š²┤_Ą─╩Ū( )
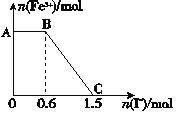
AŻ«łDųąABČ╬Ą─č§╗»ä®×ķK2Cr2O7
BŻ«łDųąBCČ╬░l╔·Ą─Ę┤æ¬×ķ2Fe3Ż½Ż½2IŻŁŻĮ2Fe2Ż½Ż½I2
CŻ«ķ_╩╝╝ė╚ļĄ─K2Cr2O7×ķ0.15 mol
DŻ«K2Cr2O7┼cFeSO4Ę┤æ¬Ą─╬’┘|Ą─┴┐ų«▒╚×ķ1Ī├6
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐I2į┌KI╚▄ę║ųą┤µį┌Ž┬┴ąŲĮ║ŌŻ║I2(aq)+I-(aq) ![]() I3-(aq)Ż¼─│I2ĪóKI╗ņ║Ž╚▄ę║ųąŻ¼I3-Ą─╬’┘|Ą─┴┐ØŌČ╚c(I3-)┼c£žČ╚TĄ─ĻPŽĄ╚ńłD╦∙╩Š(Ū·ŠĆ╔Ž╚╬║╬ę╗³cČ╝▒Ē╩ŠŲĮ║ŌĀŅæB)ĪŻŽ┬┴ąšfĘ©š²┤_Ą─╩Ū( )
I3-(aq)Ż¼─│I2ĪóKI╗ņ║Ž╚▄ę║ųąŻ¼I3-Ą─╬’┘|Ą─┴┐ØŌČ╚c(I3-)┼c£žČ╚TĄ─ĻPŽĄ╚ńłD╦∙╩Š(Ū·ŠĆ╔Ž╚╬║╬ę╗³cČ╝▒Ē╩ŠŲĮ║ŌĀŅæB)ĪŻŽ┬┴ąšfĘ©š²┤_Ą─╩Ū( )
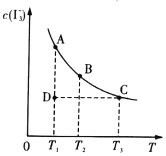
AŻ«I2(aq)+I-(aq) ![]() I3-(aq)Ą─Ī„HŻŠ0
I3-(aq)Ą─Ī„HŻŠ0
BŻ«╚¶£žČ╚T1Ż¼T2Ą─ŲĮ║Ō│ŻöĄĘųäe×ķK1Ż¼K2Ż¼ätK1ŻŠK2
CŻ«Ę┤æ¬▀MąąĄĮĀŅæBDĢrŻ¼ę╗Č©ėąVš²>V─µ
DŻ«ĀŅæBA┼cĀŅæBBŽÓ▒╚Ż¼ĀŅæBAĄ─c(I2)┤¾
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąĻPė┌╬ó┴┐į¬╦ž║═┤¾┴┐į¬╦žĄ─šfĘ©,š²┤_Ą─╩Ū(ĪĪĪĪ)
A. Č╝ī┘ė┌╔·├³╗ŅäėĄ─▒žąĶį¬╦ž
B. Č╝ī┘ė┌╔·├³╗ŅäėĄ─ų„ę¬į¬╦ž
C. Ū░š▀╩Ū╝Ü░¹╠žėąĄ─,║¾š▀╩Ū╝Ü░¹┼cĘŪ╔·╬’Įń╣▓ėąĄ─
D. ā╔š▀Č╝╩Ū╝Ü░¹ūį╔Ē║Ž│╔Ą─
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ĻPė┌ŃUąŅļŖ│žPb+PbO2+2H2SO4![]() PbSO4+2H2OĄ─šfĘ©š²┤_Ą─╩Ū
PbSO4+2H2OĄ─šfĘ©š²┤_Ą─╩Ū
AŻ«į┌Ę┼ļŖĢrŻ¼š²śO░l╔·Ą─Ę┤æ¬╩ŪPb(s)+SO42Ī¬(aq)=PbSO4(s)+2eĪ¬
BŻ«į┌Ę┼ļŖĢrŻ¼įōļŖ│žĄ─žōśO▓─┴Ž╩ŪŃU░Õ
CŻ«į┌│õļŖĢrŻ¼ļŖ│žųą┴“╦ߥ─ØŌČ╚▓╗öÓūāąĪ
DŻ«į┌│õļŖĢrŻ¼Ļ¢śO░l╔·Ą─Ę┤æ¬╩ŪPbSO4(s)+2e-=Pb(s)+SO42-(aq)
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐┼cHCl▒╚Ż¼HI
A. Ņü╔½Ė³╔Ņ B. Ęą³cĖ³Ą═ C. ▀ĆįŁąįĖ³ÅŖ D. ĘĆČ©ąįĖ³ÅŖ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąĖ„ĮM╬’┘|Ą─╚█³cŠ∙┼c╦∙║¼╗»īWµIĄ─µI─▄ėąĻPĄ─╩Ū
A. CaCl2ĪóSiO2 B. NaClĪóHCl C. CaOĪóCO2 D. Cl2ĪóI2
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐į┌ę╗Č©Śl╝■Ž┬Ż¼╝tūž╔½Ą─NO2┐╔ęį░l╔·╚ńŽ┬Ę┤æ¬Ż║2NO2(g)![]() 2NO(g)+O2(g)Ī„HŻŠ0Ż¼Ž┬┴ąöó╩÷ųąš²┤_Ą─╩Ū
2NO(g)+O2(g)Ī„HŻŠ0Ż¼Ž┬┴ąöó╩÷ųąš²┤_Ą─╩Ū
A. ║Ń£ž║Ń╚▌Ż¼│õ╚ļNO2ÜŌ¾wŻ¼Ųõ▐D╗»┬╩į÷┤¾
B. ╝ėē║Ż¼ŲĮ║ŌŽ“─µĘ┤æ¬ĘĮŽ“ęŲäėŻ¼╗ņ║ŽÜŌ¾wŅü╔½ūā╔Ņ
C. ╚¶ŲĮ║Ō│ŻöĄį÷┤¾Ż¼ät┐╔─▄╩Ū╔²Ė▀┴╦£žČ╚╗“£pąĪ┴╦¾wŽĄĄ─ē║ÅŖ
D. «ö2vš²(NO)=v─µ(O2)ĢrŻ¼Ę┤æ¬▀_ĄĮ╗»īWŲĮ║ŌĀŅæB
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐į┌¾wĘe×ķVLĄ─┴“╦ßõX╚▄ę║ųą╝ė╚ļūŃ┴┐Ą─░▒╦«Ż¼▀^×VĄ├│┴ĄĒŻ¼īó│┴ĄĒŽ┤ā¶║¾ūŲ¤²ų┴┘|┴┐▓╗į┘ūā╗»Ģr└õģsĪóĘQ┴┐Ż¼Ą├mg░ū╔½╣╠¾wĪŻįŁ╚▄ę║ųąc Ż©SO42-Ż®×ķŻ© Ż®
AŻ«![]() molĪżL-l BŻ«
molĪżL-l BŻ«![]() molĪżL-l CŻ«
molĪżL-l CŻ«![]() molĪżL-l DŻ«
molĪżL-l DŻ«![]() molĪżL-l
molĪżL-l
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com