
在t ℃時,將a g NH3完全溶于水,得到V mL溶液,假設該溶液的密度為ρ g·mL-1,質量分數為w,其中含有NH4+的物質的量是b mol,下列敘述正確的是( )
A.溶質的質量分數w=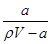 ×100% ×100% |
B.溶質的物質的量濃度c= mol·L-1 mol·L-1 |
C.溶液中c(OH-)=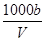 mol·L-1+c(H+) mol·L-1+c(H+) |
| D.向上述溶液中加入V mL水,所得溶液的質量分數大于0.5w |
C
解析試題分析:A、氨水溶液溶質為氨氣,該溶液的密度為ρg·mL-1,體積為VmL,所以溶液質量為ρVg,溶質氨氣的質量為ag,溶質的質量分數為 ×100%,故A錯誤;B、a g NH3的物質的量為
×100%,故A錯誤;B、a g NH3的物質的量為 =
=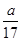 mol,溶液體積為VmL,所以溶液的物質的量濃度為
mol,溶液體積為VmL,所以溶液的物質的量濃度為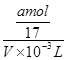 =
= mol·L-1,故B不正確;C、V mL飽和溶液中n(OH-)=n(H+)+n(NH4+)=[c(H+)×10-3+b]mol,所以
mol·L-1,故B不正確;C、V mL飽和溶液中n(OH-)=n(H+)+n(NH4+)=[c(H+)×10-3+b]mol,所以 ,C正確;D、混合前后溶質的質量不變為ag,水的密度比氨水的密度大,即ρg·cm-3<ρ水,等體積Vml混合,混合后溶液的質量大于2ρvg,所以混合后質量分數小于0.5ω,故D不正確.選C。
,C正確;D、混合前后溶質的質量不變為ag,水的密度比氨水的密度大,即ρg·cm-3<ρ水,等體積Vml混合,混合后溶液的質量大于2ρvg,所以混合后質量分數小于0.5ω,故D不正確.選C。
考點:物質的量濃度的相關計算;溶液中溶質的質量分數及相關計算


科目:高中化學 來源: 題型:單選題
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成兩份。向其中一份中逐漸加入銅粉,最多能溶解19.2 g(已知硝酸只被還原為NO氣體)。向另一份中逐漸加入鐵粉,產生氣體的量隨鐵粉質量增加的變化如圖所示。下列分析或結果不正確的是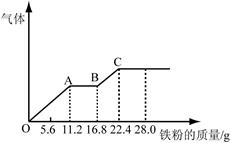
| A.混合酸中HNO3物質的量濃度為2 mol·L-1 |
| B.原混合酸中H2SO4物質的量為0.4 mol |
| C.OA段產生的是NO,AB段的反應為Fe+2Fe3+=3Fe2+,BC段產生氫氣 |
| D.第二份溶液中最終溶質為FeSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
向mg鎂和鋁的混合物中加入適量的稀硫酸,恰好完全反應生成標準狀況下的氣體bL。向反應后的溶液中加入cmol/L氫氧化鉀溶液VmL,使金屬離子剛好沉淀完全,得到的沉淀質量為ng。再將得到的沉淀灼燒至質量不再改變為止,得到固體pg。則下列關系不正確的是
| A.c=1000b/11.2V | B.p=m+Vc/125 | C.n=m+17Vc | D.5/3m<p<17/9m |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
NA為阿伏加德羅常數的數值,下列說法中正確的是
| A.在密閉容器中加入1.5molH2和0.5molN2,充分反應后可得NH3分子數目為NA |
| B.1.0L 0.1mol?L—1Na2CO3溶液中含有的CO32—離子數目為0.1NA |
| C.一定條件下,2.3gNa完全與O2反應生成3.6g產物時失去電子數目為0.1NA |
| D.在標準狀況下,2.24L的CH3CH2OH含有NA個分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
設NA為阿伏加德羅常數的值,下列說法正確的是
| A.標準狀況下,224mL水含有的電子數為0.1NA |
| B.1L 0.1mol/L硅酸鈉溶液中含有0.1NA個SiO32- |
| C.足量的鐵粉與lmolCl2在加熱條件下充分反應,轉移的電子數為3NA |
| D.標準狀況下,11.2LCO2和SO2混合氣體中含NA個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
單質碳和氧化銅在一定溫度下反應時,氧化銅可被還原為Cu2O、Cu。現將2.00g C與16.0g CuO的混合物,隔絕空氣加熱一段時間后,將生成的氣體通過足量的澄淸石灰水,共收集到1.12 L氣體(標準狀況),生成沉淀的質量為5.00 g。下列說法錯誤的是
| A.反應后的固體混合物中還含有碳 |
| B.反應后的固體混合物中Cu的質量為12.8 g |
| C.反應后的固體混合物總質貴為14.4 g |
| D.反應后的固體混合物中氧化物的物質的量為0.05mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
FeS2在空氣中充分燃燒的化學方程式為4FeS2 + 11O2 2Fe2O3 + 8SO2,若agFeS2在空氣中充分燃燒,并轉移N個電子,則阿伏加德羅常數(NA)可表示為
2Fe2O3 + 8SO2,若agFeS2在空氣中充分燃燒,并轉移N個電子,則阿伏加德羅常數(NA)可表示為
| A.120N/a | B.120a/11N | C.11a/120N | D.120N/11a |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com