
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是( )
A. 標準狀況下,22.4LCl2通入足量的NaOH溶液充分反應,有NA個電子轉移
B. 100 mL 1 mol·L1FeCl3溶液中所含Fe3+的數目為0.1NA
C. lmolSO2與足量O2在一定條件下反應生成SO3,共轉移2NA個電子
D. 84gNaHCO3固體含有CO32-離子的數目為NA
 應用題天天練四川大學出版社系列答案
應用題天天練四川大學出版社系列答案科目:高中化學 來源: 題型:
【題目】丙烯是重要的有機化工原料。以丁烯和乙烯為原料反應生成丙烯的方法被稱為“烯烴歧化法”,主要反應為![]()
![]()
![]()
已知相關燃燒熱數據:
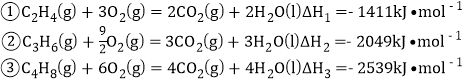
下列說法不正確的是 ( )
A. 消耗等物質的量的原料,反應③的放熱最顯著
B. 放出相等的熱量,反應①產生的![]() 最少
最少
C. “烯烴歧化“反應中消耗![]() ,放熱
,放熱![]()
D. “烯烴歧化”反應中斷鍵吸收的能量比成鍵放出的能量多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某強酸性溶液X中僅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一種或幾種,取該溶液進行連續實驗,實驗過程如下:下列有關推斷合理的是()
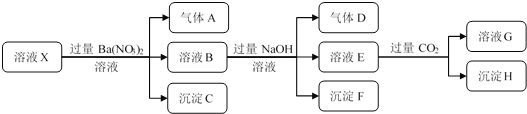
A. 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl-
B. 根據上述連續實驗不能確定溶液X中是否含有Fe3+
C. 沉淀H為Al(OH)3、BaCO3的混合物
D. 若溶液X為100mL,產生的氣體A為112ml(標況),則X中c(Fe2+)=0.05mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.分別取一定質量的甲烷、乙炔、苯、己烯、甲苯,完全燃燒后都生成m mol CO2和n mol H2O。(1)若m=n,該烴是____(2)若m=2n,該烴是____(3)若4m=7n,該烴是____
II.蒽(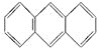 )與苯炔(|
)與苯炔(|![]() )反應生成化合物X(立體對稱圖形),如下圖所示:
)反應生成化合物X(立體對稱圖形),如下圖所示:
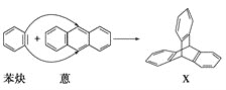
(1)蒽與X都屬于(填字母)__________a.環烴 b.烴 c.不飽和烴
(2)苯炔不具有的性質是(填字母)_______
a.能溶于水 b.能發生氧化反應 c.能發生加成反應 d.常溫常壓下為氣體
(3)下列屬于苯的同系物的是(填字母,下同)____

(4)下列物質中,能發生加成反應,也能發生取代反應,同時能使溴水因加成反應而褪色,還能使酸性高錳酸鉀溶液褪色的是____

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式正確的是( )
A.鐵粉與稀鹽酸反應:2Fe+6H+=2Fe3++3H2↑
B.碳酸鎂溶于醋酸的反應:MgCO3+2H+=Ca2++CO2↑+H2O
C.在澄清石灰水中通入少量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O
D.向沸水中滴加FeCl3溶液制備Fe(OH)3膠體:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯和溴的取代反應的實驗裝置如圖所示,其中A為具支試管改制成的反應容器,在其下端開了一小孔,塞好石棉絨,再加入少量鐵屑。
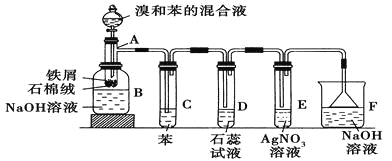
填寫下列空白:
(1)向反應容器A中逐滴加入溴和苯的混合液,幾秒鐘內就發生反應。寫出A中所發生反應的化學方程式(有機物寫結構簡式):________________________。
(2)試管C中苯的作用是 。反應開始后,觀察D和E兩試管,看到的現象分別為 、 。
(3)反應2~3 min后,在B中的NaOH溶液里可觀察到的現象是 。
(4)在上述整套裝置中具有防倒吸作用的儀器有 (填字母)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組按如下流程探究碘的制取,甲乙兩種制取方案如下:
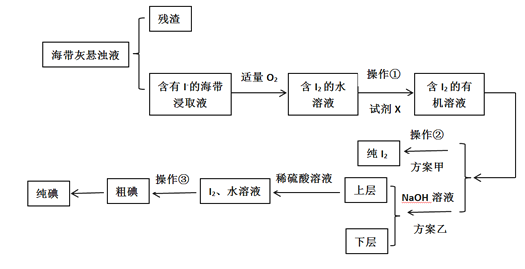
已知:3I2+6OH-=5I-+IO3-+3H2O;5I-+IO3-+6H+=3I2 +3H2O;酸性條件下,I2在水溶液中的溶解度極小。
(1)灼燒海帶時,除需要三腳架,泥三角外,還需要用到的實驗儀器為___。
A.燒杯 B.表面皿 C.坩堝 D.酒精燈
(2)指出提取碘的過程中有關的實驗操作名稱:①___;②___;③___。
(3)有機試劑X可以是___(填序號)
A.四氯化碳 B.乙醇 C.醋酸
(4)下列關于加入NaOH溶液操作的說法,正確的是___。
A.應控制NaOH溶液的濃度和體積 B.將碘轉化成離子進入水層
C.主要是除浸取原液中的雜質 D.NaOH溶液可由乙醇代替
(5)方案甲中采用操作②會導致碘的損失,原因是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉晶體(![]() ,
,![]() )可用作還原劑。回答下列問題:
)可用作還原劑。回答下列問題:
(1)已知:![]() ,
,![]() 都是難溶于水的固體。市售硫代硫酸鈉中常含有硫酸根雜質,選用下列試劑設計實驗方案進行檢驗:
都是難溶于水的固體。市售硫代硫酸鈉中常含有硫酸根雜質,選用下列試劑設計實驗方案進行檢驗:
試劑:稀鹽酸、稀![]() 、
、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液
溶液
實驗步驟 | 現象 |
①取少量樣品,加入除氧蒸餾水 | ②固體完全溶解得無色澄清溶液 |
③取少量溶液溶于鹽酸 | ④出現乳黃色渾濁,_____ |
⑤靜置,________ | ⑥_______ |
(2)利用![]() 作為標準溶液定量測定硫代硫酸鈉的純度。測定步驟如下:
作為標準溶液定量測定硫代硫酸鈉的純度。測定步驟如下:
①溶液配制;稱取1.270g純凈的![]() ,在盛有KI溶液的____(填儀器名稱,下同)中溶解(反應為
,在盛有KI溶液的____(填儀器名稱,下同)中溶解(反應為![]() ,
,![]() 能夠充分反應),完全溶解后,全部轉移至100 mL的____中,加蒸餾水至刻度線,此時
能夠充分反應),完全溶解后,全部轉移至100 mL的____中,加蒸餾水至刻度線,此時![]() 溶液的物質的量濃度為____
溶液的物質的量濃度為____![]() ;再取
;再取![]() 樣品配制成溶液,備用。
樣品配制成溶液,備用。
②滴定:利用發生反應:![]() ,對上述配制的
,對上述配制的![]() 溶液進行滴定,終點時消耗標準溶液20.00 mL,則樣品純度為___%(保留1位小數。
溶液進行滴定,終點時消耗標準溶液20.00 mL,則樣品純度為___%(保留1位小數。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把鎂條直接投入到盛有鹽酸的敞口容器中,產生H2的速率如圖所示,
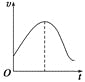
在下列因素中,影響反應速率的因素是
①鹽酸的濃度 ②鎂條的表面積 ③溶液的溫度 ④Cl-的濃度
A. ①④B. ③④C. ①②③D. ②③
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com