
【題目】A和a是生活中常見的兩種有機物,可用于制備安眠藥苯巴比妥Q,合成過程如下:
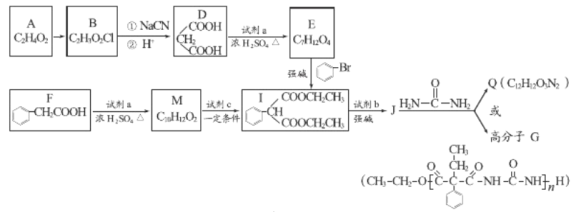
已知: 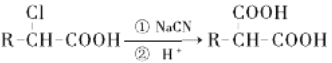
(1)A的官能團名稱為_________。
(2)A→B的反應類型為_________。
(3)D→E的反應方程式為_________________________。
(4)寫出F符合下列條件的同分異構體的結構簡式_________。
①遇Fe3+溶液顯紫色 ②發生銀鏡反應 ③苯環上的一溴代物有兩種
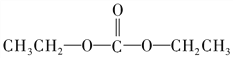
(5)J與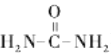 在催化劑作用下既可以生成Q,又可以生成G,寫出生成G的化學方程式 _________________________________。
在催化劑作用下既可以生成Q,又可以生成G,寫出生成G的化學方程式 _________________________________。
(6)下列說法正確的是 _________。
a.E與M互為同系物
b.B水解酸化后的產物可以發生加聚反應
c.用試劑b制備乙烯的條件是NaOH的醇溶液、加熱
d.Q的結構簡式是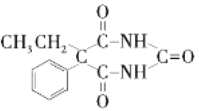
(7)試劑c為酯類,核磁共振氫譜有兩組吸收峰,與M反應生成I和a,此反應為取代,則試劑c的結構簡式為 _________。
(8)寫出以CH2=CH-CH=CH2和E為主要原料制備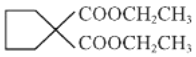 的流程_____________________________________________________________。
的流程_____________________________________________________________。
(無機試劑自選)
【答案】 羧基 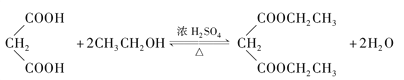 取代反應
取代反應 ![]()
 c d
c d 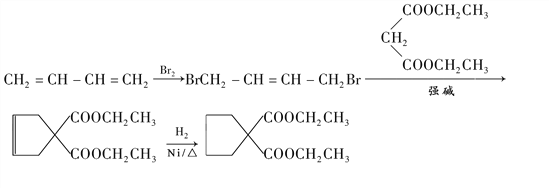
【解析】試題分析:根據D逆推,B是
,A是乙酸;根據I逆推E為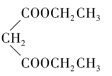 ,試劑a為乙醇;根據F可推M是苯乙酸乙酯;根據高分子G,可推J為
,試劑a為乙醇;根據F可推M是苯乙酸乙酯;根據高分子G,可推J為
;試劑c為酯類,核磁共振氫譜有兩組吸收峰,與M反應生成I和乙醇,此反應為取代,則C是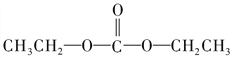 ;根據J和尿素反應生成Q及Q的分子式,可知Q為
;根據J和尿素反應生成Q及Q的分子式,可知Q為 ;
;
解析:根據以上分析,(1)乙酸的官能團名稱為羧基。
(2)乙酸→ 氯原子代替乙酸中氫原子,反應類型為取代反應。
氯原子代替乙酸中氫原子,反應類型為取代反應。
(3)![]() 與乙醇生成→
與乙醇生成→![]() 的反應方程式為
的反應方程式為 。
。
(4)①遇Fe3+溶液顯紫色,說明含有酚羥基; ②發生銀鏡反應,說明含有醛基; ③苯環上的一溴代物有兩種,說明酚羥基與醛基位置對稱,符合以上條件的F的同分異構體有![]() ;
;
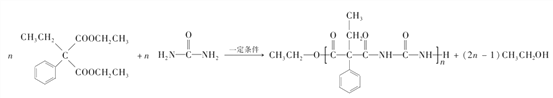
(5) 與
與 ![]() 在催化劑作用縮聚生成G,生成G的化學方程式
在催化劑作用縮聚生成G,生成G的化學方程式 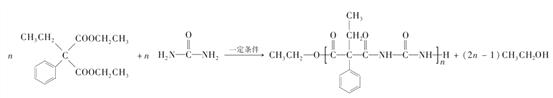 。
。
(6)下列說法正確的是 _________。
a. E與M酯基數目不同,不是同系物,故a錯誤; b.  水解酸化后生成羥基乙酸,可以發生加聚反應,故b正確;
水解酸化后生成羥基乙酸,可以發生加聚反應,故b正確;
c.用試劑乙醇制備乙烯的條件是濃硫酸、加熱,故c錯誤;
d. Q的結構簡式是 ,故d正確。
,故d正確。
(7)試劑c為酯類,核磁共振氫譜有兩組吸收峰,與M反應生成I和乙醇,此反應為取代,故c的結構簡式為 ![]() 。
。
(8)以CH2=CH-CH=CH2與溴水發生1,4加成反應,結合題干流程,料制備![]() 的流程為
的流程為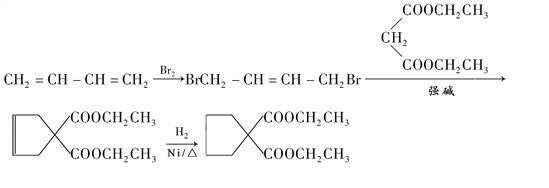


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】標準狀況下,使NO2和O2按4:1體積比充滿干燥燒瓶,將燒瓶倒置于水中,瓶內液面逐漸上升,假設燒瓶內溶液不擴散,則最終該溶液中溶質的物質的量濃度為( )
A. 1/14mol/L B. 4/5mol/L C. 1/28mol/L D. 1/42mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A. 漂白粉在潮濕空氣中易變質
B. 光導纖維的主要成分是硅單質
C. 貯氫合金的發現和應用,開辟了解決氫氣貯存、運輸難題的新途徑
D. 鋼鐵在潮濕空氣里比在干燥空氣里更易被腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)納米技術制成的金屬燃料、非金屬固體燃料、氫氣等已應用到社會生活和高科技領域。單位質量的A和B單質燃燒時均放出大量熱,可用作燃料。已知A和B為短周期元素,其原子的第一至第四電離能如下表所示:

①某同學根據上述信息,推斷B的核外電子排布如下圖所示,該同學所畫的電子排布圖違背_________,B元素位于周期表五個區域中的__________________區。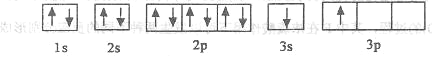
② ACl2分子中A的雜化類型為_________,ACl2的空間構型為_________。
(2)Fe原子或離子外圍有較多能量相近的空軌道能與一些分子或離子形成配合物。
①以體心立方堆積形成的金屬鐵中,其原子的配位數為__________________。
②寫出一種與CN—互為等電子體的單質的電子式____________。
③六氰合亞鐵離子[Fe(CN)6]4—中不存在__________________。
A.共價鍵 B.非極性鍵 C.配位鍵 D.σ鍵 E.π鍵
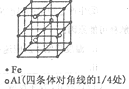
(3)一種Al-Fe合金的立體晶胞如右圖所示。請據此回答下列問題:
①確定該合金的化學式__________________。
②若晶體的密度=ρg/cm3,則此合金中最近的兩個Fe原子之間的距離(用含ρ的代數式表示,不必化簡)為______cm。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以石墨為電極,電解KI溶液(其中含有少量酚酞)。下列說法正確的是( )
A. 陰極逸出氣體 B. 陽極附近溶液呈紅色
C. K+向陽極遷移 D. 溶液的pH逐漸變小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列情況會對人體健康造成較大危害的是
A. 使用SO2漂白銀耳
B. 自來水中通入少量Cl2進行消毒殺菌
C. 用食醋清洗熱水瓶膽內壁附著的水垢
D. 用小蘇打焙制糕點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出[Ag(NH3)2]OH的中心離子的核外電子排布式________、配位體的電子式________、配位體的雜化方式是________寫出[Ag(NH3)2]OH電離的離子方程式________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列示意圖中,白球代表氫原子,黑球代表氦原子,方框代表容器,容器中間有一個可以上下滑動的隔板(其質量忽略不計)。其中能表示等質量的氫氣與氦氣的是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【山東省實驗中學2017屆下學期第二次模擬考試】(14分〕某化學興趣小組欲探究含硫物質的性質及制備。
【探究一】用下面的裝置和藥品探究亞硫酸與次氯酸的酸性強弱:
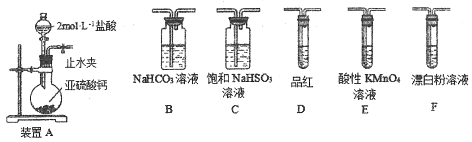
裝置連接順序為_________(用字母表示),其中裝置C的作用是___________。
【探究二】
(1)某小組同學為探究SO2的漂白性性質,用下圖所示裝置進行實驗,
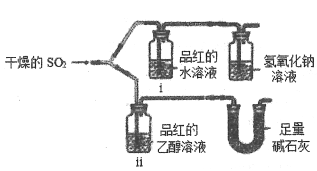
觀察到如下現象:i中紅色褪去;ii中無變化.堿石灰的作用除了吸收尾氣外還有_______的作用。從實驗中可知使品紅的水溶液褪色的微粒可能是____________。
(2)該小組同學又對SO2與氯水的反應進行探究。
①用注射器吸入一定量的飽和氯水和SO2,振蕩,靜置,再吸入少量品紅溶液,發現品紅溶液不褪色。②改變氯水用量,重復①操作,發現品紅溶液紅色褪去,你認為②中品紅溶液褪色的原因可能是__________。 設計一個實驗(說明操作方法、現象及結論)來驗證你的假設________。
【探究三】連二亞硫酸鈉(Na2S2O4)俗稱保險粉,廣泛用于紡織工業的還原性染色、清洗、印花、脫色以及織物的漂白等。制取保險粉通常需要二氧化硫。
(1)制取Na2S2O4常用甲酸鈉法。控制溫度70-80℃,在甲醇溶液(溶劑)中溶解甲酸鈉(HCOONa),再滴加Na2CO3溶液同時通SO2維持溶液酸性,即可生成Na2S2O4,反應的離子方捏式________。
(2)測定保險粉純度。Na2S2O4屬于強還原劑,暴露于空氣中易被氧氣氧化。Na2S2O4遇KMnO4酸性溶液發生反應:5Na2S2O4+6KMnO4+4H2SO4=5Na2SO4+3K2SO4+6MnSO4+4H2O。稱取5.0g Na2S2O4樣品溶于冷水中,配成100mL溶液,取出10mL該溶液于錐形瓶中,用0.10mol·L-1的KMnO4溶液滴定。重復上述操作2次,平均消耗KMnO4溶液21.00mL.則該樣品中Na2S2O4的質量分數為______ (雜質不參與反應)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com