
能在水溶液中大量共存的一組離子是
| A.Na+、Mg2+、I-、ClO- | B.Al3+、NH4+、SO42-、Cl- |
| C.K+、Ag+、NO3-、Cl- | D.NH4+、Na+、OH-、SiO32- |
B
解析試題分析:鎂離子與次氯酸根離子都能水解,相互促進對方的水解,可以發生雙水解反應,生成氫氧化鎂沉淀和次氯酸,碘離子與次氯酸根離子在酸性條件下容易發生氧化還原反應,生成單質碘、氯離子和水,即Mg2++2ClO-+2H2O=Mg(OH)2↓+2HClO、2I-+ClO-+2H+=I2+2Cl-+H2O,故A錯誤;Al3+、NH4+、SO42-、Cl-之間不能發生化學反應,故B正確;銀離子與氯離子反應,生成氯化銀沉淀,故C錯誤;銨根離子與硅酸根離子在水溶液中發生雙水解反應,生成硅酸沉淀、氨氣和水,銨根離子與氫氧根離子反應,生成一水合氨或氨氣和水,故D錯誤。
考點:考查離子共存,涉及亞鐵離子與硝酸的氧化還原反應、可溶性銀鹽與可溶性碳酸鹽的復分解反應、鋁鹽溶液與偏鋁酸鹽溶液的雙水解反應等。


科目:高中化學 來源: 題型:單選題
常溫下,下列各組離子在指定溶液中一定能大量共存的是
| A.無色溶液中:K+、Na+、Cu2+、SO42- |
| B.c(OH-)=10-13 mol·L-1的溶液中:Al3+、NO3-、I-、Cl- |
| C.水電離產生的c(H+)=10-13 mol·L-1的溶液中:Na+、Cl-、NO3-、SO42- |
| D.0.1 mol·L-1FeSO4溶液中:K+、NH4+、MnO4-、ClO- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列表示對應化學反應的離子方程式正確的是
| A.足量Cl2通入FeBr2溶液中:Br-+ Cl2 = Br2 +2Cl- |
| B.用NaClO除去水體中CO(NH2)2產生CO2和N2:3ClO +CO(NH2)2=3Cl- +CO2↑+N2↑+2H2O |
| C.過量CO2通入Na2SiO3溶液中:Si032-+CO2+H2O = H2SiO3↓+CO32- |
| D.Ca(HCO3)2溶液中加入過量NaOH溶液:Ca2+ +HCO3-+OH-= CaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
室溫下,下列各組離子在指定溶液中一定能大量共存的是
| A.飽和氯水中:Cl-、NO3-、Na+、SO32- |
B.c(H+)=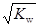 的溶液中:K+、Fe3+ 、Cl-、SO42- 的溶液中:K+、Fe3+ 、Cl-、SO42- |
| C.澄清透明的溶液中:Cu2+、NH4+、NO3-、ClO4- |
| D.使紅色石蕊試紙變藍的溶液中:CH3COO-、HCO3-、Na+、K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在溶液中能大量共存的一組離子或分子是
| A.K+、Al3+、SO42―、NH3·H2O | B.NH4+、H+、NO3―、HCO3― |
C.Na+、CH3COO―、CO32―、OH― | D.Na+、K+、SO32―、Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列各組離子在溶液中能夠大量共存的是
| A.NH4+、Ca2+、OHˉ、CO32ˉ |
| B.Ag+、H+、SO32ˉ、ClOˉ |
| C.NH4+、Brˉ、Na+、SO42ˉ |
| D.H+、Clˉ、Fe2+、NO3ˉ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
能在水溶液中大量共存的一組離子是
| A.H+、Fe3+、I-、SO42- |
| B.Al3+、Mg2+、HCO3-、Cl- |
| C.K+、Ca2+、NO3-、SiO32- |
| D.K+、Na+、OH-、AlO2- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列離子或分子在溶液中能大量共存,但通入NO2后不能大量共存,且不會生成沉淀的一組是( )
| A.K+、Na+、NO3-、SiO32- | B.Al3+、K+、SO42-、S2- |
| C.Ag+、Na+、NH3·H2O、NO3- | D.Cu2+、Fe2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(18分)高鐵酸鉀(K2FeO4)是一種集氧化、吸附、絮凝于一體的新型多功能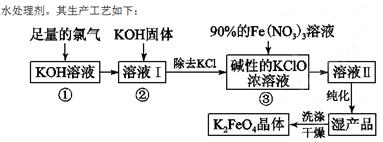
(1)反應①應在溫度較低的情況下進行。因在溫度較高時KOH與Cl2反應生成的是KClO3。寫出在溫度較高時KOH與Cl2反應的化學方程式 ,該反應的氧化產物是 。
(2)在溶液Ⅰ中加入KOH固體的目的是 (填編號)。
| A.與溶液Ⅰ中過量的Cl2繼續反應,生成更多的KClO |
| B.KOH固體溶解時會放出較多的熱量,有利于提高反應速率 |
| C.為下一步反應提供堿性的環境 |
| D.使KClO3轉化為KClO |
 +____H2O — ____Fe(OH)3(膠體)+____O2↑+____OH-。
+____H2O — ____Fe(OH)3(膠體)+____O2↑+____OH-。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com