
在下列給定條件的溶液中,一定能大量共存的離子組是( )
| A.無色溶液:Ca2+、Fe3+、Cl-、NO3- |
| B.能使pH試紙呈紅色的溶液:Na+、NH4+、I-、NO3- |
| C.FeCl3溶液:K+、Na+、SO42-、AlO2- |
D. mol/L的溶液:Na+、K+、SiO32-、NO3- mol/L的溶液:Na+、K+、SiO32-、NO3- |
D
解析試題分析:離子間如果發生化學反應,則不能大量共存,反之是可以的。A中鐵離子在溶液中顯棕黃色,不能大量共存,A不正確;能使pH試紙呈紅色的溶液顯酸性,在酸性溶液中,NO3-能氧化I-,不能大量共存,B不正確;C中Fe3+和AlO2-水解相互促進,不能大量共存,C不正確、D中根據水的離子積常數可知,溶液中c(OH-)=0.1mol/L,即溶液顯堿性,可以大量共存,答案選D。
考點:考查離子共存的正誤判斷
點評:該題是高考中的高頻題,屬于中等難度的試題,側重對學生基礎知識的訓練和檢驗。有利于培養學生的邏輯推理能力,提高學生靈活運用基礎知識解決實際問題的能力。該題需要明確離子不能大量共存的一般情況,即(1)能發生復分解反應的離子之間;(2)能生成難溶物的離子之間;(3)能發生氧化還原反應的離子之間;(4)能發生絡合反應的離子之間(如 Fe3+和 SCN-);解決離子共存問題時還應該注意題目所隱含的條件,題目所隱含的條件一般有:(1)溶液的酸堿性,據此來判斷溶液中是否有大量的 H+或OH-;(2)溶液的顏色,如無色時可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色離子的存在;(3)溶液的具體反應條件,如“氧化還原反應”、“加入鋁粉產生氫氣”;(4)是“可能”共存,還是“一定”共存等。


 亮點激活精編提優100分大試卷系列答案
亮點激活精編提優100分大試卷系列答案科目:高中化學 來源: 題型:單選題
下列解釋相關問題或實驗的離子方程式不正確的是
A.NaClO溶液呈堿性:ClO—+H2O HClO+OH- HClO+OH- |
| B.向沸水中滴加飽和FeCl3溶液制膠體:Fe3++3 H2O=Fe(OH)3(膠體)+3 H+ |
| C.粗鹽提純中除去Mg2+:Mg2++2OH—=Mg(OH)2↓ |
| D.工業上精煉粗銅的陰極反應:Cu—2e—=Cu2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列離子方程式中錯誤的是
| A.稀氨水吸收足量SO2:NH3·H2O + SO2= NH4++ HSO3- |
| B.向Ca(ClO)2溶液中通入過量二氧化碳:ClO-+ H2O + CO2=" HClO" + HCO3- |
| C.稀硝酸中加入鐵粉:2Fe + 6H+= 2Fe3++ 3H2↑ |
| D.過氧化鈉與冷水反應:2Na2O2+ 2H2O = 4Na++ 4OH-+ O2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知250C時某溶液中含有大量Na+、H+、Fe3+、HC03-、OH-、I-中的幾種,并且水電離出的c(H+) = 1×10-13mol/L。當向該溶液中緩慢通入一定量的Cl2后,溶液由無色變為黃色。下列有關分析正確的是
A.溶液的PH=1或13
B.溶液中一定沒有Fe3+,Na+
c.溶液中陰離子有I-,不能確定HCO3-
D.當Cl2過量,所得溶液只含有兩種鹽
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列反應的離子方程式中,書寫正確的是
| A.氯氣溶于水:H2O + C12=2H+ + ClO- + Cl- |
| B.將鋁粉投入氫氧化鈉溶液中:2Al + 2OH-=2AlO2- + H2↑ |
| C.鐵粉與氯化鐵溶液反應:Fe + Fe3+=2Fe2+ |
| D.過氧化鈉與水反應:2Na 2O2+ 2H2O=4Na+ + 4OH-+ O2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列反應的離子方程式正確的是
| A.氯氣與水反應:Cl2+H2O=2H++Cl-+ClO- |
| B.在稀氨水中通入過量CO2:NH3·H2O+CO2=NH4++HCO3- |
| C.用氯化鐵溶液腐蝕電路板:Fe3++Cu=Fe2++Cu2+ |
| D.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列化學反應的離子方程式不正確的是
| A.Na2S溶液中加入少量FeCl3溶液:2Fe3++S2- = 2Fe2++S↓ |
| B.向NaOH溶液中滴加碳酸氫鈣溶液至OH-恰好完全反應:Ca2++2OH-+2HCO3- = CaCO3↓+2H2O+CO32- |
| C.向NaClO溶液中通入少量SO2氣體:ClO-+SO2+H2O = SO42-+Cl-+2H+ |
D.Na2CO3溶液中滴入少量鄰羥基苯甲酸溶液: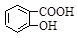 +CO32- +CO32- 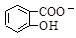 +HCO3- +HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(12分)鹵化物和鹵酸鹽在工業生產中有著重要的作用。某小組為探究其中一些鹽的性質,查閱資料并進行實驗。
查閱資料如下:
①BrO3-+ 6I-+ 6H+ = 3I2 + Br-+ 3H2O ② 2BrO3-+ I2 = 2IO3-+ Br2
③ IO3-+ 5I-+ 6H+ = 3I2 + 3H2O ④ 2IO3-+ 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
實驗如下:
| 步 驟 | 現 象 |
| ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的錐形瓶中依次滴入幾滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 隨著KBrO3溶液滴入,溶液由無色變為藍色并逐漸加深,最終保持不變 |
| ⅱ.繼續向上述溶液中滴入KBrO3溶液 | 溶液的藍色逐漸褪去 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某無色溶液只可能含有以下幾種離子:①Mg2+、②Al3+、③Fe2+、④H+、⑤ 、⑥Cl-、⑦OH-。向其中緩慢地滴入NaOH溶液至過量,產生沉淀的質量與加入NaOH溶液的體積的關系如圖所示,由此可確定原溶液中一定含有的離子是
、⑥Cl-、⑦OH-。向其中緩慢地滴入NaOH溶液至過量,產生沉淀的質量與加入NaOH溶液的體積的關系如圖所示,由此可確定原溶液中一定含有的離子是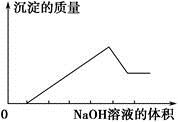
| A.①②⑤ | B.①③④ | C.②⑥⑦ | D.①②④⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com