
【題目】下表是元素周期表的一部分,回答下列問題。

(1)⑨在周期表中的位置是_______________,其原子結構示意圖為______________。
(2)⑤⑥⑦的簡單離子半徑最小的是______(填離子符號),原子半徑最小的是_______(填化學式),⑤⑥⑨三種元素的氣態氫化物最穩定的是______(用化學式表示)。
(3)⑥對應的氣態氫化物沸點高于同主族元素對應的氣態氫化物,原因是_____________。
(4)①⑤兩元素可以形成原子個數比1︰1和2︰1的化合物X和Y,其中X的電子式為___________,用電子式表示Y的形成過程____________________________________。
(5)由①③⑤三種元素組成的化合物之一Z,是生活中常見的有機化合物,它具有特殊的香味,寫出Z與⑦的反應方程式:___________________________________。
【答案】 第三周期ⅦA族 ![]() Na+ F HF HF分子間存在氫鍵,氫鍵強于范德華力
Na+ F HF HF分子間存在氫鍵,氫鍵強于范德華力 ![]()
![]() 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
【解析】根據元素在周期表中的相對位置可知①~⑩分別是H、Be、C、N、O、F、Na、Al、Cl、Ar。
(1)Cl的質子數是17,在周期表中的位置是第三周期ⅦA族,其原子結構示意圖為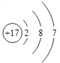 。(2)離子的核外電子層數越多,離子半徑越大,核外電子排布相同時離子半徑隨原子序數的增大而減小,則⑤⑥⑦的簡單離子半徑最小的是Na+。同周期自左向右原子半徑逐漸減小,同主族從上到下原子半徑逐漸增大,所以原子半徑最小的是F;⑤⑥⑨三種元素中F的非金屬性最強,則氣態氫化物最穩定的是HF。(3)由于HF分子間存在氫鍵,氫鍵強于范德華力,所以F對應的氣態氫化物沸點高于同主族元素對應的氣態氫化物。(4)①⑤兩元素可以形成原子個數比1︰1和2︰1的化合物X和Y分別是雙氧水和水,其中雙氧水的電子式為
。(2)離子的核外電子層數越多,離子半徑越大,核外電子排布相同時離子半徑隨原子序數的增大而減小,則⑤⑥⑦的簡單離子半徑最小的是Na+。同周期自左向右原子半徑逐漸減小,同主族從上到下原子半徑逐漸增大,所以原子半徑最小的是F;⑤⑥⑨三種元素中F的非金屬性最強,則氣態氫化物最穩定的是HF。(3)由于HF分子間存在氫鍵,氫鍵強于范德華力,所以F對應的氣態氫化物沸點高于同主族元素對應的氣態氫化物。(4)①⑤兩元素可以形成原子個數比1︰1和2︰1的化合物X和Y分別是雙氧水和水,其中雙氧水的電子式為![]() ,水的形成過程可表示為
,水的形成過程可表示為![]() 。(5)由①③⑤三種元素組成的化合物之一Z是生活中常見的有機化合物,它具有特殊的香味,Z是乙醇,乙醇與鈉反應的方程式為2CH3CH2OH+2Na→2CH3CH2ONa+H2↑。
。(5)由①③⑤三種元素組成的化合物之一Z是生活中常見的有機化合物,它具有特殊的香味,Z是乙醇,乙醇與鈉反應的方程式為2CH3CH2OH+2Na→2CH3CH2ONa+H2↑。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】常溫下,在20mL0.1mol/L HR 溶液中滴加0.1000mol/LNaOH溶液,混合溶液的PH與所加NaOH溶液體積的關系如圖所示。下列推斷正確的是

A. ①、②、③三點中,③對應的溶液中c水(H+)·c水(OH-)最大
B. HR溶液中只存在H+、R-、OH-、H2O四種微粒
C. ②點溶液中一定存在c(Na+)>c(R-)>c(H+)=c(OH-)
D. NaR的水解常數Ka和水解程度:③>②>①
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】類推思維是化學解題中常用的一種思維方法,下列有關反應方程式的類推正確的是
已 知 | 類 推 | |
A | 將鐵粉投入稀硫酸中 Fe+H2SO4(稀)= FeSO4+H2↑ | 將鐵粉投入稀硝酸中 Fe+2HNO3(稀)= Fe(NO3)2+H2↑ |
B |
|
|
C | 將乙烯通入溴水中 CH2=CH2+Br2→CH2BrCH2Br | 將丙烯通入溴水中 CH3CH=CH2+Br2→CH3CHBrCH2Br |
D | 乙烯在適當條件下制聚乙烯 nCH2=CH2 | 丙烯在適當條件下制聚丙烯 nCH3CH=CH2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)已知在2L的容器中進行下列可逆反應,各物質的有關數據如下:
aA (g)+ bB (g)![]() 2C(g)
2C(g)
起始物質的量濃度(mol/L): 1.5 1 0
2s末物質的量濃度(mol/L): 0.9 0.8 0.4
則:①該可逆反應的化學方程式可表示為 ;
②0到2s用物質B來表示的反應速率為 ;
③從反應開始到2s末,A的轉化率為 ;
④下列事實能夠說明上述反應在該條件下已經達到化學平衡狀態的是 。
A.容器內氣體的密度不變
B.vA︰vB︰vC=3︰2︰2
C.vB(反應)= vC(生成)
D.容器內氣體的總壓強保持不變
E.容器內氣體C的物質的量分數保持不變
(2)①鋅電池有望代替鉛蓄電池,它的構成材料是鋅、空氣、某種電解質溶液,發生的總反應式是:
2Zn+O2=2ZnO。則該電池的負極材料是 ;當導線中有1 mol電子通過時,理論上消耗的O2在標準狀況下的體積是 。
②瑞典ASES公司設計的曾用于驅動潛艇的液氨-液氧燃料電池示意圖如下,該燃料電池工作時,外電路中電子的流動方向是從電極 到電極 ;電池的總反應為 。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯及其化合物在生產、生活中有很多用途。
Ⅰ二氧化錳與濃鹽酸在加熱條件下反應制氯氣,氯氣與鐵反應制取氯化鐵,其裝置如下(所通氣休過量并充分反應)

請回答下列問題:
(1)裝置A中發生反應的離了方程式為_____________。
(2)裝置B中的試劑為______,裝置C的作用是_____________。
(3)反應開始后,裝置D中玻璃管內的現象為______;可以檢驗生成物中Fe3+的試劑是_____。
(4)某同學猜測鐵與氯氣反應可能還會生成氯化亞鐵,為了探究生成物中是否氯化亞鐵(假設鐵已完全反應)。請你設計實驗方案:______
Ⅱ.二氧化氯(ClO2)是一種高效消毒劑,可用鹽酸或雙氧水還原氯酸鈉制備ClO2,其中用H2O2作還原劑制備ClO2更環保,主要原因是____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無色溶液中能夠大量存在的離子是( )
A.K+ H+ SO42- OH- B.Na+ Ca2+ CO32- NO3-
C.Mg2+ Fe3+ NO3- SO42- D.Na+ Mg2+ Cl- SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用0.1000mol·L-1的鹽酸滴 0.1000mol·L-1Na2CO3溶液25.00mL。用pH傳感器測得混合溶液的pH變化曲線如圖,下列說法正確的是

A. c→d點發生的主要離子反應:HCO3-+H+=H2O+CO2
B. 在b點時,c(CO32-)>c(HCO3-)>c(OH-)
C. 在d點時, c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D. 在e點時, c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】保護環境已成為人類的共識。下列物質與所對應的環境問題沒有關系的是
A | B | C | D |
建筑垃圾 | 二氧化碳 | 鹵代烷烴 | 二氧化硫 |
白色污染 | 溫室效應 | 臭氧層受損 | 酸雨 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“漆器”是中國古代在化學工藝及工藝美術方面的重要發明,所用生漆是從我國特產漆樹割取的天然液汁。生漆主要成分是漆酚![]() ,—C15H27為鏈烴基,則漆酚不應具有的化學性質是
,—C15H27為鏈烴基,則漆酚不應具有的化學性質是
A. 可以跟FeCl3溶液發生顯色反應 B. 可以使酸性KMnO4溶液褪色
C. 可以跟Na2CO3溶液反應放出CO2 D. 可以發生取代反應和加成反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com