
【題目】國際計量大會第26屆會議新修訂了阿伏加徳羅常數(NA=6.02214076×1023mol-1),并于2019年5月20日正式生效。下列說法中正確的是
A.12g金剛石中含有化學鍵的數目為4NA
B.將7.1g Cl2溶于水制成飽和氯水,溶液中Cl-、ClO-和HC1O的微粒數之和為0.1NA
C.標準狀況下,11.2L NO和11.2L O2混合后,氣體的分子總數為0.75NA
D.20g的D2O中含有的質子數為10NA
【答案】D
【解析】
A、金剛石屬于原子晶體,1mol金剛石中含有2mol C-C,即12g金剛石中含有C-C鍵物質的量為![]() ×2=2mol,故A錯誤;
×2=2mol,故A錯誤;
B、氯氣溶于水,部分氯氣與水發生反應,溶液中含有氯元素的微粒有Cl2、Cl-、ClO-、HClO,溶液中Cl-、ClO-、HClO微粒物質的量之和小于0.1mol,故B錯誤;
C、NO與O2發生2NO+O2=2NO2,根據所給量,NO不足,O2過量,反應后氣體物質的量和為0.75mol,但2NO2![]() N2O4,因此反應后氣體物質的量小于0.75mol,故C錯誤;
N2O4,因此反應后氣體物質的量小于0.75mol,故C錯誤;
D、D2O為2H2O,其摩爾質量為20g·mol-1,20g D2O中含有質子物質的量為![]() ×10=10mol,故D正確;
×10=10mol,故D正確;
答案選D。


 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源: 題型:
【題目】下列實驗操作完全正確的是()
編號 | 實驗 | 操作 |
A | 用濃硫酸配制一定濃度的稀硫酸 | 準確量取濃硫酸,將濃硫酸溶于水后,立刻轉移到容量瓶中。 |
B | 制取氫氧化亞鐵沉淀 |
|
C | 量取鹽酸溶液 | 用50 mL量筒量取4.0 mol/L的鹽酸5.62 mL |
D | 取出分液漏斗中所需的上層液體 | 下層液體從分液漏斗下端管口放出,關閉活塞,換一個接收容器,上層液體繼續從分液漏斗下端管口放出 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在盛有溴水的三支試管中分別加入汽油、四氯化碳和酒精,振蕩后靜置,出現如圖所示的現象。下列說法正確的是( )

A.①加入的是CCl4,②加入的是汽油,③加入的是酒精
B.①加入的是酒精,②加入的是CCl4,③加入的是汽油
C.①加入的是汽油,②加入的是酒精,③加入的是CCl4
D.①加入的是汽油,②加入的是CCl4,③加入的是酒精
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值,下列說法錯誤的是( )
A.常溫常壓下,48gO2含有的氧原子數為3NA
B.1L0.1 mol/L CH3CH2OH水溶液中含H原子數目為0.6NA
C.標準狀況下,11.2L氦氣和氫氣的混合氣含有的分子數為0.5NA
D.1.7g NH3含有的質子數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定質量的某鐵的氧化物FexOy,與足量的4 mol·L-1硝酸溶液充分反應,消耗硝酸溶液700 mL,生成2.24 L NO(標準狀況)。則該鐵的氧化物的化學式為( )
A.FeOB.Fe2O3C.Fe3O4D.Fe4O5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室中用下列裝置測定SO2催化氧化為SO3的轉化率(部分夾持裝置已省略,已知SO3的熔點為16.8℃,假設氣體進入裝置時均被完全吸收,且忽略空氣中CO2的影響),下列說法不正確的是( )
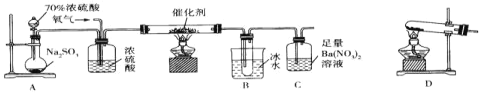
A.A裝置燒瓶中發生的反應可以表示為SO32-+2H+=SO2↑+H2O
B.用D裝置制備氧氣,試管中的藥品可以是KClO3
C.當停止通入SO2,熄滅酒精燈后,需要繼續通一段時間的氧氣
D.C中產生的白色沉淀是BaSO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為研究廢舊電池的再利用,實驗室利用舊電池的銅帽(主要成分為Zn和Cu)回收Cu并制備ZnO的部分實驗過程如圖所示。下列敘述錯誤的是
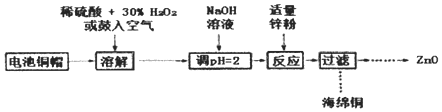
A.“溶解”操作中溶液溫度不宜過髙
B.銅帽溶解的反應可能有H2O2+Cu+2H+=Cu2++2H2O
C.與鋅粉反應的離子可能是Cu2+、H+
D.“過濾”操作后,將濾液蒸發結晶、過濾、洗滌、干燥后高溫灼燒即可得純凈的ZnO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C為中學常見單質,其中一種為金屬;通常情況下,A為固體,B、C均為氣體。D、E、F、G、H、X均為化合物,其中X是一種無氧強酸、E為黑色固體,H在常溫下為液體。它們之間的轉化關系如圖所示(其中某些反應條件和部分反應物已略去)。
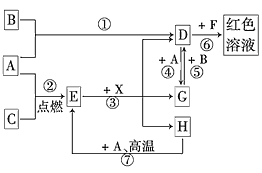
(1)在反應①~⑦中,不屬于氧化還原反應的是________(填編號)。
(2)寫出③的離子方程式:________________
(3)反應⑦的化學方程式為____;該反應中每消耗0.3 mol的A,可轉移電子_________mol。在解決此題時的關鍵一步是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室需配制500mL 0.2mol/L Na2SO4溶液,實驗操作步驟為:
A.把制得的溶液小心地轉移至容量瓶中。
B.在天平上稱取14.2g 硫酸鈉固體,把它放在燒杯中,用適量的蒸餾水將它完全溶解并冷卻至室溫。
C.繼續向容量瓶中加蒸餾水至液面距刻度1~2cm處,改用膠頭滴管小心滴加蒸餾水至溶液凹液面底部與刻度線相切。
D.用少量蒸餾水洗滌燒杯和玻璃棒2~3次,每次洗滌的液體都小心注入容量瓶,并輕輕振蕩。
E.將容量瓶塞塞緊,充分搖勻。
請填寫下列空白:
(1)操作步驟的正確順序為_______________(填序號)。
(2)本實驗用到的基本儀器除燒杯、天平(砝碼、鑷子)、玻璃棒外,還有__________
(3)下列情況中,會使所配溶液濃度偏低的是________________。
A.某同學觀察液面時仰視 B.沒有進行上述的操作步驟D
C.加蒸餾水時,不慎超過了刻度線 D.容量瓶使用前內壁沾有水珠
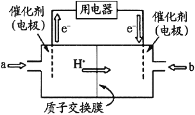
(4)甲醇燃料電池(簡稱DMFC)由于結構簡單、能量轉化率高、對環境無污染,可作為常規能源的替代品而越來越受到關注。DMFC工作原理如圖所示:通入a氣體的電極是原電池的_______極(填 “正”或“負”),其電極反應式為__________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com