
【題目】某興趣小組同學利用氧化還原反應:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O設計如下原電池,鹽橋中裝有飽和溶液.下列說法正確的是( ) 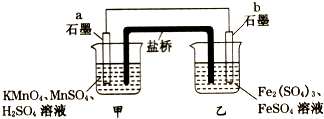
A.a電極上發生的反應為:MnO4﹣+8H++5e﹣═Mn2++4H2O
B.外電路電子的流向是從a到b
C.電池工作時,鹽橋中的SO42﹣移向甲燒杯
D.b電極上發生還原反應
【答案】A
【解析】解:A、甲燒杯中發生還原反應,Mn元素的化合價降低,電極反應為MnO4﹣+8H++5e﹣═Mn2++4H2O,故A正確; B、由上述分析可知,a為正極,電子由負極流向正極,即從b流向a,故B錯誤;
C、陰離子向負極移動,則鹽橋中的SO42﹣移向乙燒杯中,故C錯誤;
D、b為負極,負極發生氧化反應,故D錯誤;
故選A.
由2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O可知,Mn元素的化合價降低,得到電子,Fe元素的化合價升高,失去電子,則b為負極,a為正極,結合原電池中負極發生氧化反應,電流從正極流向負極,陰離子向負極移動來解答.


科目:高中化學 來源: 題型:
【題目】用以下三種途徑來制取等質量的硝酸銅。
①銅與稀硝酸反應;②銅與濃硝酸反應;③銅先與氧氣反應生成氧化銅,氧化銅再與硝酸反應。以下敘述不正確的是
A. 三種途徑所消耗銅的質量相等
B. 三種途徑所消耗硝酸的物質的量是①>②>③
C. 途徑③的制備方法最符合“綠色化學“理念
D. 途徑①中還原劑與氧化劑的物質的量之比是3: 8
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫﹣氨熱化學循環制氫示意圖如下: 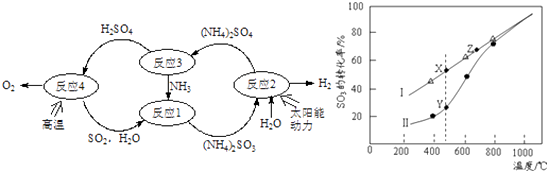
(1)反應1的離子方程式為 .
(2)反應2能量轉化主要方式為 .
(3)反應3中控制反應條件很重要,不同條件下硫酸銨分解產物不同.若在400℃時分解,產物除水蒸氣外還有A、B、C三種氣體,A是空氣中含量最多的單質,B能使濕潤的紅色石蕊試紙變藍,C能使品紅溶液褪色.則400℃時硫酸銨分解的化學方程式為 .
(4)反應4是由(a)、(b)兩步反應組成:
H2SO4(l)=SO3(g)+H2O(g),△H=+177kJmol﹣1…(a)
2SO3(g)2SO2(g)+O2(g),△H=+196kJmol﹣1…(b)
①則H2SO4(l)分解為SO2(g)、O2(g)及H2O(g)的熱化學方程式為: .
②在恒溫密閉容器中,控制不同溫度進行SO3分解實驗.以SO3起始濃度均為cmolL﹣1 , 測定SO3的轉化率,結果如圖2,圖中Ⅰ曲線為SO3的平衡轉化率與溫度的關系,Ⅱ曲線表示不同溫度下反應經過相同反應時間且未達到化學平衡時SO3的轉化率.
(i)圖中點X與點Z的平衡常數K:
K(X)K(Z)(選填:>,<,=);
(ii)Y點對應溫度下的反應速率:
v(正)v(逆)(選填:>,<,=);
(iii)隨溫度的升高,Ⅱ曲線逼近Ⅰ曲線的原因是: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據要求填空
(1)按系統命名法命名:
①  ,寫出它和氯氣發生一取代反應的方程式
,寫出它和氯氣發生一取代反應的方程式
②  ;它的一氯代物具有不同沸點的產物有 種
;它的一氯代物具有不同沸點的產物有 種
(2)寫出下列各有機物的結構簡式:
①2,3﹣二甲基﹣4﹣乙基已烷: ;
②支鏈只有一個乙基且相對分子質量最小的烷烴: ;
(3)羥基的電子式 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X,Y,Z三種物質中含同種元素,在一定條件下可以實現如圖所示轉化,下列推斷不正確的是( ) 
A.若Y為氧化鋁,則Y 生成X的條件是“通電”
B.若X為硫單質,則Y 可能為硫化氫
C.若Z為硝酸,則X可能為一氧化氮
D.若Z為硝酸鐵,則Y一定為鐵單質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列對有關實驗寧實的說明或解釋正確的是
A. 用坩堝鉗夾住一小塊用砂紙打磨過的鋁箔在灑精燈上加熱,鋁熔化但不滴落,說明Al2O3的熔點高于Al
B. 向某溶液中先淌加Ba(NO3)2溶液,出現白色沉淀,再滴加稀硝酸,沉淀不溶解,說明原溶液中一定含有SO42-
C. 向新制氯水中加入少量NaHCO3固體,出現較多氣體,說明HClO的酸性強于H2CO3
D. 向某溶液中先滴加KSCN溶液,溶液不變紅,再滴加雙氧水,溶液變紅,說明原溶液中一定含有Fe2+
【答案】AD
【解析】A、加熱打磨過后的鋁箔,鋁表面生成氧化鋁薄膜,鋁熔化說明鋁熔點低,但鋁不滴落,說明氧化鋁熔點非常高,故A正確;B、溶液中也可能存在的SO32-,Ba2+與SO32-反應生成白色的BaSO3沉淀,SO32-有強還原性,再加硝酸,硝酸將BaSO3氧化為不溶于硝酸的BaSO4,所以無法判斷原溶液中是否含有SO42-,故B錯誤;C、氯氣與水反應生成鹽酸和次氯酸,加入NaHCO3固體,產生CO2,只能說明氯水酸性強于H2CO3,并不能說明HClO酸性強于碳酸,故C錯誤;D、向溶液中先滴加KSCN溶液,溶液不變紅,則證明溶液中不含Fe3+,再加雙氧水,溶液變紅,說明原溶液中一定含有Fe2+被雙氧水氧化為Fe3+,故D正確。故選AD。
【題型】多選題
【結束】
21
【題目】某種制取純堿的方法如下:
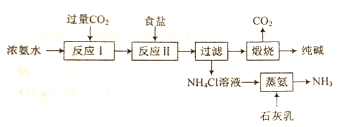
(1)寫出“反應I ”的化學方程式:__。
(2)“反應Ⅱ”為復分解反應,反應中所涉及物質的溶解度如圖所示。寫出“反應Ⅱ”的化學方程式:__。

(3)寫出“煅燒”反應的化學方程式:__。
(4) “蒸氨”時需要加熱,寫出“蒸氨”時反應的化學方程式:___。
(5)寫出將“蒸氨”產生的氨氣通入Al2(SO4)3溶液中時反應的離子方程式: __。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】描述CH3﹣CH=CH﹣C≡C﹣CF3分子結構的下列敘述中,正確的是( )
A.6個碳原子有可能都在一條直線上
B.6個碳原子不可能都在一條直線上
C.6個碳原子有可能都在同一平面上
D.6個碳原子不可能都在同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有m g某氣體,它的摩爾質量為M g·mol-1。若阿伏加德羅常數用NA表示,則:
(1)該氣體的物質的量為________mol。
(2)該氣體在標況下的密度為__________g/L。
(3)該氣體在標準狀況下的體積為____________L。
(4)該氣體溶于0.1L水中(水的密度:1g·mL-1,且不考慮反應),其溶液中溶質的質量分數為_____。
(5)該氣體溶于水后形成VL溶液,其溶液的物質的量濃度為_____mol/L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com